© The Korean Society for Bio-Environment Control. All rights reserved.
ABSTRACT
서 론
사과(Malus domestica Borkh.)는 전세계적에서 생산되 는 온대과수 중 하나로 우리나라에서 생산량은 두 번째 이며 재배면적이 가장 넓은 과수로, 사과 품종 재배면적 은 ‘후지’(70.1%), ‘홍로’(14.5%), ‘쓰가루’(5.0%), 기타 (10.4%)의 순으로 중생종으로는 ‘홍로’의 비율이 높은 편이다(KOSAT, 2014). 사과는 내외부의 스트레스로 인 해 생산성이 감소하거나 품질의 저하 등의 부정적인 영 향을 받는다. 사과에서 과피색과 가용성 고형물 함량은 과실품질을 결정하는 중요한 요소이며, 동일한 장소에서 오랜 기간 생육하므로 기후 또는 미기상 조건의 영향을 크게 받는다(Seo와 Park, 2003). 과실의 품질은 생장시 기에의 광합성활동에 의해 결정되고 온도 조건의 영향을 받는다(Saure, 1990;Song 등, 2003;Tomana와 Yamada, 1988a). 최근에 국내에서는 지구온난화로 인한 기온 상 승으로 남부지방에서는 고품질 과실의 재배가 어려워짐 으로 주요 재배지역이 중북부지방으로 이동하고 있다 (Kim 등, 2010).
사과 과실의 품질에 영향을 끼치는 여러 가지 특성 중 과피의 붉은색은 농산물 시장 가격을 결정하는 중요한 요소이다. 과실의 과피색을 결정하는 색소는 다양하게 존재하지만 안토시아닌의 양과 조성, 플라보노이드의 종 류는 사과 과실의 과피색을 결정하는 주요 요인이다 (Honda 등, 2002;Lancaster, 1992). 또한 과피의 색소는 과실의 영양학적 가치와도 연관이 있다(Honda 등, 2002). 사과에서 시아니딘과 UDP당의 축적은 고온에 의 해 억제가 되는 반면에 과피의 색을 변화시키는 안토시 아닌의 축적은 고온에서 급격히 억제되는 것으로 보고되 어 있다(Ban 등, 2009;Steyn 등, 2005). 지구온난화 및 도시화에 의해 생장기의 평균 기온이 15°C이상 높아지 면 착색은 불량해지고 과실의 생장 및 성숙이 지연되거 나 억제된다(Lee, 1999;Tomana와 Yamada, 1988b;Warrington 등, 1999;Yamada 등, 1988, 1944).
포도 과실의 생장과 성숙에 유리한 기후 조건인 온대 지역에서도 과피의 착색불량이 발생하지만, 고온에서 특 히 과피의 착색이 억제되거나 지연되는 것으로 보고되었 다(Lee 등, 1979). 또한 착색불량의 원인구명을 위하여 사과 과실의 발육단계에 따른 안토시아닌 생합성 유전자 의 발현 수준을 연구하였고, 과피 색소 축적에 따른 안 토시아닌 농도와 유전자 발현 양상을 확인하였다(Honda 등, 2002;Kondo 등, 2002).
최근 도시화와 산업화로 인한 온도 상승은 사과 과실 의 성장 지연, 당함량 감소, 착색과 형태 불량, 과실의 저장수명 단축 등으로 고품질의 사과 생산과 농가 수익 에 부정적인 영향을 끼친다(Hulme 등, 1994). 기후 변화 와 지구온난화에 의한 지속적인 고온은 과실 생장에 부 정적인 영향을 미치고, 생리장해의 한 종류인 밀증상도 생육기의 저온보다는 고온에서 발생률 및 발생 정도가 심한 것으로 보고되어 있다(Park 등, 2009).
본 연구에서는, β-amylase (BMY), phenylalanine ammonia-lyase (PAL)와 flavanone 3-hydroxylase (F3H) 등을 포함한 안토시아닌 생합성과 당축적과 관련된 유전 자의 발현 정도를 확인하고 고온에 의해 나타나는 현상 을 분자생물학적 수준에서 분석하고자 고온에 노출된 사 과 과실의 전사체를 분석하기 위한 기초자료로 제공하고 자 실시하였다.
재료 및 방법
1. 식물 재료 및 온도처리
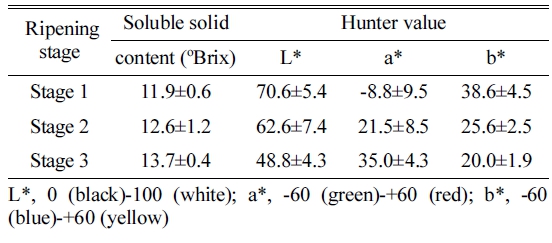
본 실험에 사용한 사과 과실은 충청북도 충주시 충청 대로 소재의 농가에서 재배되는 12년생 ‘홍로’(M.9대목) 과수에서 2014년 9월 2일에 수확한 후 과피의 착색과 당함량을 기준으로 3단계로 구분하여 시험에 사용하였다 (Table 1). 빛이 16:8(광/암)시간으로 조사되는 생육상 (Ilshin Tech., Daejeon, Korea)에서 온도(25, 30, 35°C)를 처리하였다. 과실은 0, 6, 12, 24, 48시간 처리 후 액체 질소에서 동결 시킨 후 -80°C에 보관하면서 사용하였다.
Table 1.
Fruit characteristics of ‘Hongro’ apples in 3 ripening stages used in this study.
2. RNA분리 및 Real-time PCR
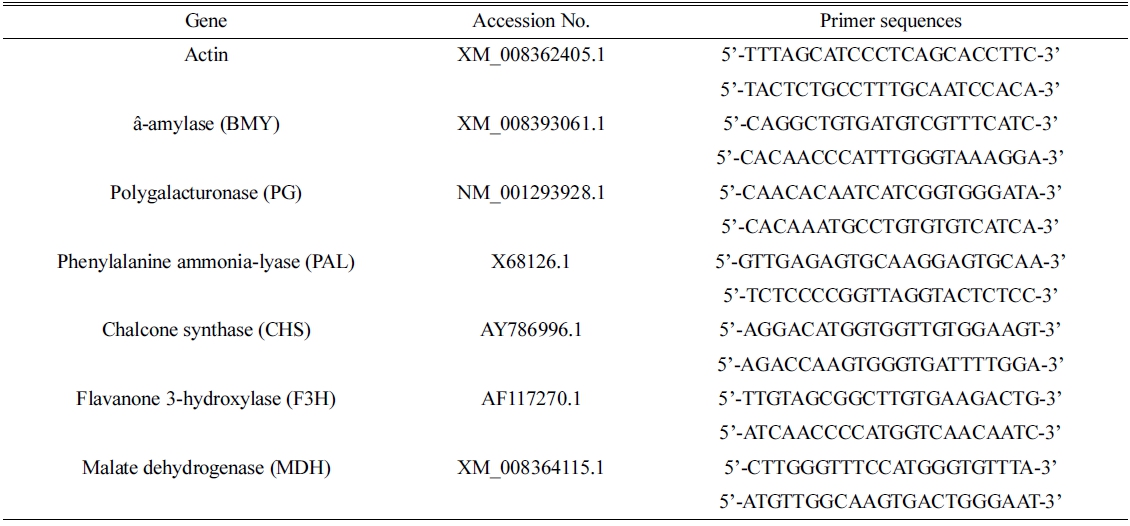
처리구별로 고온처리 한 후 과실을 Chang 등(1993)의 방법으로 일부 변형하여 RNA를 분리하였다. 과육과 과피 를 포함한 사과 과실 조직 2g을 막자사발과 액체질소를 사용하여 곱게 마쇄한 후 15mL의 RNA추출액[2% CTAB, 100mM Tris-HCl(pH 8.0), 25mM EDTA, 2% PVP K30, 2M NaCl, 0.05% spermidine, 10% ß-mercaptoethanol]을 첨가하여 녹인 후 동량의 chloroform:isoamyl alcohol(24:1) 을 섞은 후 상온에서 원심분리(UNION 32R, Hanil Science Inc., Korea)를 2,170×g로하여 상징액을 분리하 였다. 1/4부피의 10M LiCl을 첨가하고 4°C에서 6시간이 상 보관한 후 2,170×g로 20분동안 원심분리하여 RNA 침전물을 얻었다. RNA침전물은 500mL의 SSTE용액 [1M NaCl, 0.5% SDS, 10mL Tris HCL(pH 8.0), 1mM EDTA]에 녹여 동량의 chloroform:isoamyl alcohol(24:1) 을 섞은 후 상온에서 원심분리(Legend Micro17, Thermo Fisher Scientific Inc., USA)를 13,800¥g로하여 상징액을 분리하였고, 1/10부피의 3M NaOAc와 2배의 에탄올을 첨 가하여 -80°C에서 30분이상 보관한 후 13,800×g로 20분동 안 원심분리하여 RNA를 분리하였다. 분리한 RNA는 1% agarose gel에서 전기영동 하여 확인하고 Nano Drop spectrophotometer(ND-1000, Technologies Inc., USA)를 이용하여 260, 280nm 흡광도에서 농도를 측정하고 최종 RNA농도를 500ng/mL로 정량하였다. 분리한 RNA(1mg) 로부터 PrimeScriptTM1st strand cDNA synthesis kit(TaKaRa Bio Inc., Japan)를 이용하여 1st cDNA를 합 성하고 real-time PCR 반응을 위한 주형으로 사용하였다. Real-time PCR의 조건은 다음과 같다: initial denaturation, 95°C-30초; denaturation, 95°C-5초; annealing, 60°C-30초; 40cycle 반복. Internal standard로는 actin 유전자를 표준 시료로는 무처리 과실을 이용하였다. 각 유전자는 표준 시료와 비교하였으며 최종 결과는 log값으로 나타내었다. 유전자 특이적인 프라이머는 Primer3(http://frodo.wi.mit. edu/primer3)를 이용하여 제작하였으며 염기서열은 Table 2에 나타내었다.
Table 2.
NCBI gene accession numbers and sequences of gene primers used for quantitative real-time PCR analysis.
결과 및 고찰
‘홍로’ 사과 과실의 고온에 따른 과피의 착색에 관여 하는 안토시아닌 합성 관련 유전자와 과실의 당축적에 관 여하는 유전자의 발현 변화를 분석하였다. 변색기의 ‘홍 로’ 사과 과실을 변색수준에 따라 3단계로 구분하여 고온 에 노출시키킨 후, β-amylase (BMY), polygalacturonase (PG), phenylalanine ammonia-lyase (PAL), chalcone synthase (CHS), flavanone 3-hydroxylase (F3H)와 malate dehydrogenase (MDH) 유전자의 발현을 real-time PCR을 이용하여 분 석하였다.
변색 초기와 중간단계에서 BMY의 발현은 온도에 따 른 발현양의 차이는 나타나지 않았고, 서서히 감소하였 다가 온도처리 후 24시간에 증가하였다. 변색기 마지막 단계인 3단계에서는 유전자의 발현이 꾸준히 증가하는 양상을 나타내었으며 30~35°C의 고온에서 보다 25°C에 서 많이 발현되었다(Fig. 1). PG 유전자도 과실이 성숙 단계가 진행될수록 발현이 증가하여 변색기 후반기에서 발현이 많았으나, 온도간의 뚜렷한 차이는 나타나지 않 았다.
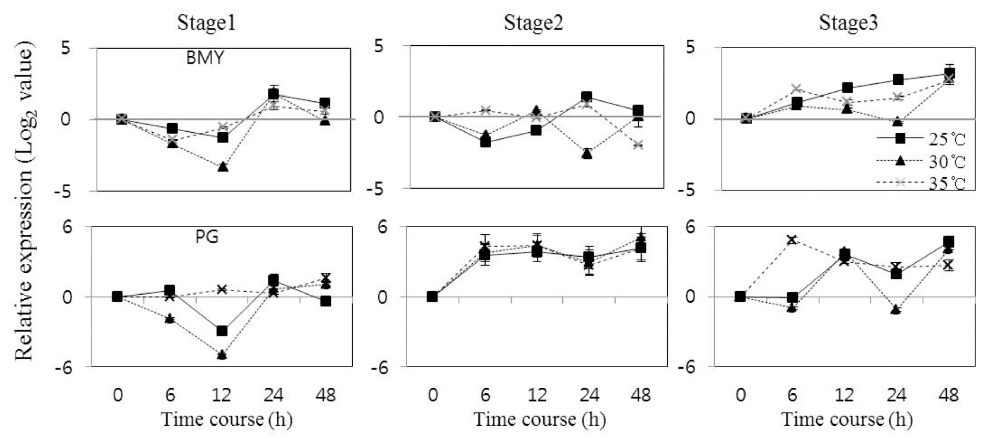
Fig. 1
Expression of beta-amylase (BMY) and polygalacturonase (PG) genes by different temperatures in the fruits of apple. The error bars represent the standard error of the means of three replicates. Stage 1, initial ripening stage; Stage 2, middle ripening stage; Stage 3, late ripening stage.
과피색의 착색에 관여하는 PAL, CHS, F3H, MDH 유 전자의 발현은 변색 초기단계에서 발현양이 많지 않았으 며, 30~35°C에 노출된 과실은 25°C에 비해 발현양이 감 소하였으며, 특히 MDH 유전자는 현저하게 감소하였다 (Fig. 2). 변색 중간단계인 과실에서는 모든 유전자의 발 현이 25°C 처리구에서는 점진적으로 증가하였으며, 30℃ 와 35°C 처리구에서는 노출된 시간이 경과할수록 발현 이 감소하는 경향을 보였다.
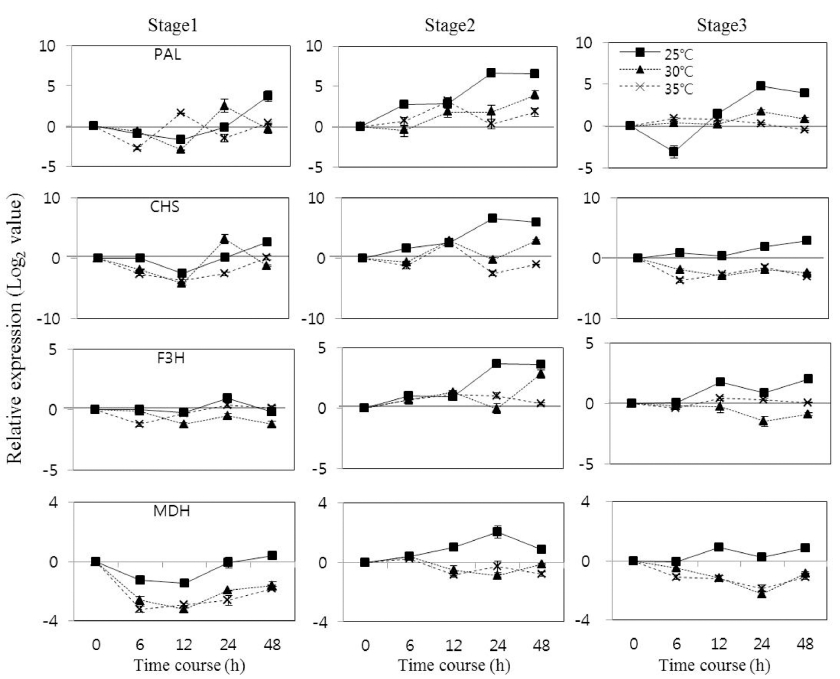
Fig. 2
Expression of phenylalanine ammonia lyase (PAL), chalcone synthase (CHS), flavone 3-hydrogenase (F3H), and malate dehydrogenase (MDH) genes by different temperatures in the fruits of apple. The error bars represent the standard error of the means of three replicates. Stage 1, initial ripening stage; Stage 2, middle ripening stage; Stage 3, late ripening stage.
변색기 마지막 단계의 성숙한 과실에서는 모든 유전자 가 25°C에서는 모든 유전자의 발현이 증가하는 경향을 나타내었지만, 30°C와 35°C의 발현수준은 미미하였다. 30°C와 35°C에서의 발현양은 큰 차이가 없었으며 25°C에 비해 발현이 현저하게 감소하였다. 변색기 이후의 ‘홍로’ 사과 과실에서 안토시아닌 합성 관련 유전자의 발현 수 준은 25-30°C보다 35°C에서 낮았으며, 이러한 유전자의 발현 억제는 고온에 의한 사과 과피의 착색불량과 관련 이 있는 것으로 여겨진다.
‘후지’ 사과의 가용성 고형물 함량은 생육기 온도가 30°C일때보다 저온조건인 20°C 및 25°C일수록 증가하는 경향을 보이는 것으로 보고되어 있다(Yoon et al., 2010). 과실비대기(6-8월)의 기온이 30°C이상일 때 신초 와 과실의 생장속도 및 광합성속도가 감소하고, 35°C이 상일 때는 호흡에 의한 에너지 소비가 많아져 광합성속 도가 급감한다(Lakso, 1994). 자당, 과당, 포도당 등의 당류 중에서 자당은 사과의 유과기 세포 생장에 가장 큰 영향을 끼치며, 솔비톨은 과당 축적의 주요 기질이며 당 축적 대사에서 중요한 역할을 한다(Beruter, 1985). 이와 같이 생육기에 고온을 받게 되면 당함량의 감소뿐 아니라 광합성이 감소하여 생장억제 등 악영향을 끼칠 수 있다.
PG는 큰 유전자군으로 식물조직이나 발달단계에 넓은 범위로 발현되며 사과 과실의 성숙과 연관되어 있으며 (Atkinson 등, 2002), 특이온도 의존적으로 에틸렌반응 유전자를 조절하며 세포벽효소의 작용에 의해 조절된다 (Costa 등, 2002). 본 연구에서는 당 합성관련 유전자인 BMY와 PG 유전자의 발현이 변색이 시작되는 1단계보 다 변색이 완료된 3단계에서 월등히 높았는데, 이는 과 실의 성숙이 진행됨에 따라 고온에 의해 당대사와 관련 한 유전자의 발현도 증가한 것으로 여겨진다.
사과 품종의 과실 발육 단계별 당과 전분농도 및 조성 에 대한 분석결과에 따르면, 중생종인 ‘홍로’ 과실에서는 생육기간 동안 당 농도는 꾸준히 증가하며 성숙기 이후 에 급속한 증가 양상을 나타낸 반면에 전분 농도는 급 격히 증가하였다가 급격히 감소하는 양상을 보였다 (Song 등, 2003). 성숙기의 총 전분 농도가 낮은 것은 대부분이 가용성 당으로 변환되었기 때문이다. 다양한 사과 품종에서 안토시아닌 합성을 위한 최적의 온도는 20-25°C이며, 이보다 낮거나 높으면 합성이 억제된다 (Curry, 1997). 사과의 착색에 직접적으로 관여하는 안토 시아닌 합성이 고온에 의해 억제되는 것으로 알려져 있 으며(Reay, 1999), 배와 사과에서 착색이 불량한 것은 고온에 의한 안토시아닌의 억제로 인한 것으로 보고되었 다(Steyn et al., 2004).
사과 과실에서 안토시아닌 생합성 유전자의 발현은 과 실의 붉은색의 착색 정도에 관련된 안토시아닌 축적에 비 례적이며, 유전자의 발현 수준은 안토시아닌 농도에 상응 한다(Honda 등, 2002). MdCHS, MdF3H, dihydroflavonol 4-reductase(pDFR), anthocyanin synthase(MdANS), UDP galactose:flavonoid glucose transferase(pUFGluT) 5개 유전 자를 대상으로 발현 수준을 분석하여 고온보다는 저온에 서 특히 MdCHS, MdANS, pUFGluT 유전자의 발현이 높 았다고 보고하였다(Ubi 등, 2006). 안토시아닌 함량과 PAL활성 측정 결과에 따라 15-20°C의 온도에서 착색에 효과적이라고 보고되었다(Noro 등, 1991;Lee, 1999). Lister 등(1996)에 의하면, ‘Splendour’ 사과 과실에서는 PAL, chalcone isomerase(CHI), UDP galactose:flavonoid 3-O-galactosyltransferase(UFGalT) 유전자의 활성이 과실 성숙 중에 안토시아닌 축적과 관련이 있다고 밝혀졌다. 그러나, ‘Delicious’와 ‘Ralls’ 사과 과실의 생육 기간 동 안 빛에 노출된다면 CHS 활성은 안토시아닌 생합성의 조절에 크게 영향을 끼치지 않는다는 것을 증명하였으며 (Ju 등, 1995a, 1995b), PAL 활성은 ‘Delicious’ 과피에 서 안토시아닌 축적과 관련이 없으며 플라보노이느 농도 는 과실 발달 단계 전체에서 높게 유지되었다. 본 연구 에서는 과피 착색과 관련있는 PAL, CHS, F3H, MDH유 전자의 발현을 확인하였으며, 서로 다른 온도처리구에서 변색 시작단계에서는 감소하다가 증가하는 경향을 보였 으며 변색 중간단계에서는 점차 증가하는 경향을 보였다. 변색단계별로 보았을 때 25°C 처리구가 다른 처리구보 다 발현 정도가 더 높은 것을 확인할 수 있었고, 30°C 이상의 고온에서는 발현이 억제되었으며, 변색기 초기단 계보다 성숙이 진행될수록 발현이 현저하게 억제되었다.
‘후지’ 사과의 생육기 온도가 20°C 정도일 때 광합성 률이 증가하여 착색을 증진시킬 뿐만 아니라 과중 및 당함량을 높여 과실품질을 향상시키는데 효과적이라고 한다(Yoon 등, 2010). 그러나 과실의 착색에는 온도뿐만 아니라 광의 영향도 크게 작용하며, 수관위치에 따른 광 환경에 따라 수관상단-외부 과실의 착색이 30% 정도 진 행이 되었을 때 수관하단-내부 과실의 경우 착색이 전혀 진행되지 않음을 알 수 있다(Song 등, 2014). 이와 같이 양호한 광조건에서 착색이 촉진되었으며, ‘Delicious’ 사 과에서도 광투과율이 감소한 경우에는 과실 크기 및 품 질, 생산성이 현저히 저하되었다(Barritt 등, 1991). 본 연구에서는 기후 변화에 따른 온도상승에 따른 유전자의 발현에 관한 연구를 수행하였으나, 기후 변화에 따른 고 온과 더불어 변화할 수 있는 광조건을 달리하여 처리한 다면 과실의 변색단계별 기후 변화에 따른 반응 기작을 더 깊이 이해할 수 있을 것으로 여겨진다.
국내에서도 지구 온난화 및 도시화에 의해 과실 생육 기 동안 기온이 높아져 ‘후지’ 사과 재배에서는 착색불 량이 가장 큰 문제점으로 대두되고 있다(Park 등, 2009;Sagong 등, 2013). 과피의 착색과 당 축적 기작에 관여하 는 여러 환경요소 중에서 온도에 따른 과실의 성숙차이 에 대한 연구가 성숙단계의 과실에서 주로 연구되고 있 다(Azuma 등, 2012;Bergqvist 등, 2001). 사과 과실의 성숙에는 많은 요소들이 관여하고 있으므로, 전사체 분석 을 통한 다양한 반응을 체계적으로 분석하면 고온에 의 한 생화학적 변화에 관한 유용한 정보를 얻을 수 있을 것이다. 또한 장기간 온도처리에 따른 당 대사 및 착색관 련유전자의 발현변화와 온도처리 전후의 당도 및 색차계 값의 추이를 분석해본다면 더 정확한 기초자료도 이용될 수 있을 것이다. 본 연구에서는 분자 수준에서 사과 과 실의 성숙단계에 따라 고온스트레스에 의해 변화하는 유 전자를 비교 분석하여 고온에 대한 사과과실의 반응 기 작을 이해하는데 필요한 유용한 정보를 얻을 수 있었다. 또한 이 연구를 통하여 향후 고온에 대응하는 과실의 변화를 전사체 분석과 같은 분자생물학 수준에서의 연구 를 수행하는 데에 있어서 사과 과실의 가장 적합한 성 숙단계를 선정할 수 있는 중요한 정보를 제공하게 될 것이다.
사 사
본 연구는 농촌진흥청 공동연구사업(과제번호: PJ010174) 의 지원에 의해 수행되었음.
References
KOSAT. 2014. http://kosat.go.kr/potal/korea/kor-nw/2/7/1/index.board.
Atkinson, R.G., R. Schroder, I.C. Hallett, D. Cohen, and E.A. MacRae. 2002. Overexpression of polygalacturonase in transgenic apple trees leads to a range of novel phenotypes involving changes in cell adhesion. Plant Physiol. 129:122-133.
Azuma, A., H. Yakushiji, Y. Koshita, and S. Kobayashi. 2012. Flavonoid biosynthesis-related genes in grape skin are differentially regulated by temperature and light conditions. Planta 236:1067-1080.
Ban, Y., S. Kondo, B.E. Ubi, C. Honda, H. Bessho, and T. Moriguchi. 2009. UDP-sugar biosynthetic pathway: contribution to cyaniding 3-galactoside biosynthesis in apple skin. Planta. 230: 871-881.
Barritt, B.H., C.R. Rom, K.R. Guelich, S.R. Drake, and M.A. Dilley. 1991. Light level influences spur quality and canopy development and light interception influence fruit production in apple. Hort Science 26:993-999.
Bergqvist, J., N. Dokoozlian, and N. Ebisuda. 2001. Sunlight exposure and temperature effects on berry growth and composition of Cabernet Sauvignon and Grenache in the central San Joaquin valley of California. Am. J. Enol. Vitic. 52:1-7.
Beruter, J. 1985. Sugar accumulation and changes in the activities of related enzymes during development of the apple fruit. J. Plant Physiol. 121:331-341.
Chang, S., J. Puryear, and J. Cairney. 1993. A simple and efficient method for isolating RNA from pine trees. Plant Mol.Biol. 11:113-116.
Costa, F., C.P. Peace, S. Stella, S. Serra, S. Musacchi, M. Bazzani, S. Sansavini, and W.E. Van de Weg. 2002. QTL dynamics for fruit firmness and softening around an ethylene-dependent polygalacturonase gene in apple (Malus x domestica Borkh.). J. Exp. Bot. 1-11.
Curry, E.A. 1997. Temperatures for optimal anthocyanin accumulation in apple tissue. J. Hort. Sci. 72:723-729.
Honda, C., N. Kotoda, M. Wada, S. Kondo, S. Kobayashi, J. Soejima, Z. Zhang, T. Tsuda, and T. Moriguchi. 2002. Anthocyanin biosynthetic genes are coordinately expressed during red coloration in apple skin. Plant Physiol. Biochem. 40: 955-962.
Hulme, M., Z.C. Zaho, and T. Jiang. 1994. Recent and future climate change in East Asia. Intl. J. Climatol. 14:637-658.
Ju, Z., C. Liu, and Y. Yuan. 1995a. Activities of chalcone synthase and UDPGal:flavonoid 3-O-glycosyltransferase in relation to anthocyanin synthesis in apple. Sci. Hortic. 63:175-185.
Ju, Z., C. Liu, Y. Yuan, C. Liu, and S. Xin. 1995b. Relationships among phenylalanine ammonia-lyase activity, simple phenol concentrations and anthocyanin accumulation in apple. Sci. Hortic. 61:215-226.
Kim, S.Y., I.H. Heo, and S.H. Lee. 2010. Impacts of temperature rising on changing of cultivation area of apple in Korea. J. Kor. Assoc. Reg. Geograph.. 16:201-215. (in Korean)
Kondo, S., K. Hiraoka, S. Kobayashi, C. Honda, and N. Terahara. 2002. Changes in the expression of anthocyanin biosynthetic genes during apple development, J. Am. Soc. Hort. Sci. 127:971-976.
Lakso, A.N. 1994. Apple. Handbook of Environmental Physiology of Fruit Crops. 1:3-42.
Lancaster, J.E. 1992. Regulation of skin color in apples. Crit. Rev. Plant Sci. 10:487-502.
Lee, H.C. 1999. Physiologycal and ecological factors affecting fruit coloration and color enhancement in Malus domestica Borkh. cv. 'Fuji'. Ph. D. Thesis. Seoul National University, Korea. (in Korean)
Lee, J.C., T. Tomana, U. Naoki, and K. Ikuo. 1979. Physiological study on the anthocyanin development in grape - I. Effect of fruit temperature on the anthocyanin development in "Kyoho" grape. Kor. J. Hort. Sci. Technol. 20:55-65. (in Korean)
Lister, C.E., J.E. Walker, and J.R.L. Lancaster. 1996. Developmental changes in enzymes of flavonoid biosynthesis in the skins of red and green apple cultivars. J. Sci. Food Agric. 71:313-320.
Noro, S., H. Ichinohe, and N. Obra. 1991. Effects of controlled air temperature on development of anthocyanin, sugar and citramalic acid during maturation of the apple cultivar Starking Delicious. Bulletin of the Aomori Apple Experiment Station. 27:111-123.
Park, M.Y., Y.Y. Song, H.H. Han, and D.H. Sagong. 2009. Influence of air temperature during the growing period on water core occurrence in 'Hongro' apple cultivar and the mitigation technique. Korean J. Agr. Forest Meteorol. 11:100-110. (in Korean)
Reay, P.F. 1999. The role of low temperatures in the development of the red blush on apple fruit ('Granny Smith'). Sci. Hortic. 79:113-119.
Sagong, D.H., H.J. Kweon, M.Y. Park, Y.Y. Song, S.H. Ryu, M.J. Kim, K.H. Choi, and T.M. Yoon. 2013. Impacts of urban high temperature events on physiology of apple trees: a case study of 'Fuji'/M.9 apple trees in daegu, korea. Korean J. Agr. Forest Meteorol. 15:130-144. (in Korean)
Saure, M.C. 1990. External control of anthocyanin formation in apple. Sci. Hortic. 42:181-218.
Seo, H.H. and H.S. Park. 2003. Fruit quality of 'Tsugaru' apples influenced by meteorological elements. Korean J. Agr. Forest Meteorol. 54:218-225.
Song, J.H., I.K. Kang, and D.G. Choi. 2014. Light conditions and characteristics of leaves and fruit at different canopy positions in slender-spindle 'Hongro' apple trees. Kor. J. Hort. Sci. Technol. 32:440-447.
Song, K.J., J.H. Hwang, and H.K. Yun. 2003. Changes of soluble sugar and starch concentrations in fruits of apple cultivars differing in maturity. Hort. Environ. Biotechnol. 44:207-210.
Steyn, W.J., D.M. Horlcroft, S.J.E. Wand, and G. Jacobs. 2004. Anthocyanin degradation in detached pome fruit with reference to preharvest red color loss and pigmentation patterns of blushed and fully red pears. J. Amer. Soc. Hort. Sci. 129:13-19.
Steyn, W.J., S.J.E. Wand, D.M. Holcroft, and G. Jacobs. 2005. Red colour development and loss in pears. Acta Hortic. 671:79-85.
Tomana, T. and H. Yamada. 1988a. Change in sugar composition during maturation stage of apple fruit grown at different locations. J. Jpn. Soc. Hortic. Sci. 57:178-183.
Tomana, T. and H. Yamada. 1988b. Relationship between temperature and fruit quality of apple cultivars grown at different locations. J. Jpn. Soc. Hortic. Sci. 56:391-397.
Ubi, B.E., C. Honda, H. Bessho, S. Kondo, M. Wada, S. Kobayashi, and T. Moriguchi. 2006. Expression analysis of anthocyanin biosynthetic genes in apple skin: Effect of UVB and temperature. Plant Sci. 170:571-578.
Warrington, I.J., T.A. Fulton, E.A. Halligan, and H.N. de Silva. 1999. Apple fruit growth and maturity are affected by early season temperatures. J. Am. Soc. Hortic. Sci. 124(5):468-477.
Yamada, H., H. Ohmura, C. Arai, and M. Terui. 1994. Effect of preharvest fruit temperature on ripening, sugar, and watercore occurrence in apples. J. Am. Soc. Hortic. Sci. 119(6):1208-1214.
Yamada, H., K. Hamamoto, A. Sugiura, and T. Tomana. 1988. Effect of controlled fruit temperature on maturation of apple fruits. J. Jpn. Soc. Hortic. Sci. 57(2):173-177.
Yoon, C.G., I.C. Son, and D.I. Kim. 2010. Effects of temperature during growth stage on tree growth and fruit quality in 'Fuji'/M.9 apples. J. Kor. Soc. Int. Agric. 22:143-147.