서 언
파프리카(Capsicum annuum L.)는 시설채소 중 단위 면적당 소득이 높고 수출유망품목으로 주목을 받으면서 국내산 파프리카가 일본 전체 수입량의 69.3%를 점유하 고 있으며, 2015년 현재 국내에서는 29.4천 톤의 파프리 카가 생산되었고, 수출액은 8.5천만 달러로 대표적인 농 가 소득 작물 중 하나이다(KATI, 2015).
국내 파프리카의 재배 작형은 크게 여름작형과 겨울작 형으로 구분되며, 여름작형은 높은 온도 환경으로 인해 중남부 고랭지에서 주로 재배되고 생산기로는 6월에서 12월이다. 반면, 겨울작형은 여름작형보다 재배기간이 길 고 평지에서 재배되며 11월에서 익년 7월까지 생산된다 (KATI, 2014). 여름작형은 겨울작형의 수확시기와 중복 되지 않아 단경기 가격이 비교적 높게 형성되지만, 여름 철 장마기 고온 다습 환경에서 병충해 발생이 높고 생 리장해가 빈발해 안정 착과율이 저하하여 수확량은 겨울 작형 수량의 60% 수준에 머물러 치밀한 병해충방제 및 재배환경 관리가 요구된다(Won 등, 2009). 우리나라의 단위면적당 파프리카 생산량은 네덜란드 생산량에 비해 단위면적당 수량이 58% 정도의 낮은 수준으로(Jeong 등, 2008), 국내 기상여건, 수경재배, 양액관리기술, 시설환경 조절 기술, 환경조절시스템 운영 등 여러가지 측면에서 개선의 필요성이 제기되고 있다. 특히 장기재배시 계절 변화에 따른 큰 폭의 온실 내 환경변화는 작물에 있어 서 불안정한 착화 및 착과로 생산량 감소의 원인이 되 므로, 변화하는 환경조건에 대응하는 신속한 영양상태의 진단 및 처방이 중요하다(Heuvelink 등, 2004).
영양상태의 진단을 위하여 일반적으로 식물체 건조시 료를 전처리후 ICP, AA, Spectrophotometer등의 기기를 활용하여 무기성분 함량을 정량하는데, 이들 방법은 식 물체를 건조 후 분해하고, 정량분석 결과를 얻기까지 시 간과 노력이 소요되어 현장에서 신속하게 식물체의 영양 상태를 판단하기에 적합하지 않다. 이러한 필요성 하에 신속한 영양상태 진단을 위해 간이엽록소계와 엽병 즙액 을 이용하여 분석하는 연구가 기존 국내·외에서 진행된 바 있다. 간이엽록소계(SPAD)는 오래 전부터 작물의 영 양상태를 신속하게 파악하는 간이영양진단기기로 활용되 어 왔으며, 간이 엽록소계를 이용하여 옥수수에서 질소 함량을 파악하였다(Waskom 등, 1996). 또한, 감자와 밀 의 질소시비 결정을 신속하게 내릴 수 있는 엽록소 함 량의 표준 범위가 제시된 바 있고(Islam 등, 2009; Isalm 등, 2014; Zheng 등, 2015) 특히, 신속한 시비요 구량 파악이 어려운 목본석 식물에서 엽록소계를 이용하 여 신속하게 질소 영양상태를 파악하고 시비량 산출을 시도하였다(Husni 등, 2014). 엽병 즙액을 이용하여 작 물의 무기성분을 신속하게 측정하는 test strip 방법 역시 기존에 많은 연구가 진행되었다. 목화(Gossypium spp.) 에서 일반 무기성분 분석법과 엽병 즙액을 활용한 신속 분석 방법 간에 NO3-N 농도의 상관성이 도출되었으며 (Smith 등, 1998), K원소에서도 토마토 엽병을 이용해 ICP와 test strip의 상관성을 분석한 결과 r2=0.88로 높은 상관관계를 보였다(Taber 과 Lawson, 2007). 또한 Test strip (RQ-flex®10, Merck, Germany)을 이용해 브로콜리, 오이, 멜론, 고추, 감자 등 원예 작물에 대해서 질소함량 을 신속하게 분석하고 생육단계별 영양상태의 농도 범위 를 제시하였다(Hochmuth, 1994). 국내에서도 test strip을 사용해 토마토와 오이의 엽병을 생육단계별, 수확시기별 로 채취 후 N, P, K 원소함량을 분석해 영양상태를 파 악하였고(Kim 등, 2003; Kim과 Kim, 2003), 딸기에서 는 엽병 즙액 내 P와 K의 신속 성분분석이 가능한 것으 로 확인되었다(Lim, 등 2012). 이와 같이 다양한 작물에 대해서 작물의 정상적인 영양상태의 무기성분 범위에 대 해서 산발적으로 연구가 진행되었으나, 파프리카의 경우 다양한 간이영양진단기기를 활용한 N, P, K, Fe 등의 영양원소의 모니터링 가능성만 검토되었고(Kim, 2011), 생육단계별, 품종별로 영양 상태의 신속진단 및 장·단기 영양상태의 모니터링에 대한 연구결과는 없는 상태이다. 장기 환경 및 재배관리가 중요한 파프리카 작물에서 변 동 환경 조건별, 생육단계별, 신속 영양상태의 분석 및 표준범위의 설정이 가능하다면 생리장해에 대한 신속한 대처 및 안정생산에 도움을 줄 수 있을 것으로 판단된 다. 따라서 본 연구에서는 엽병 또는 엽신 즙액의 신속 분석 결과의 효율성 및 장·단기 모니터링의 적용성을 생 육단계별 및 품종별로 검토하여 향후 파프리카 영양관리 의 기초자료로 활용하기 위하여 수행되었다.
재료 및 방법
1. 파프리카 수경재배 환경
본 연구는 경남농업기술원(Latitude 35°12’ N, longitude 128°12’E)내 벤로형 유리온실(2,000m2)에서 주간거리 30cm로 재배된 겨울작형 파프리카 식물체를 이용하였다. 실험재료는 대과종 ‘Nicole’(Kooij Korea seed, Korea), ‘TP2001’(Kooij Korea seed, Korea)과 소과종 ‘Raon Red’(Gnares, Korea), ‘Raon yellow’(Gnares, Korea)의 총 4 품종을 이용하였으며, 평균 온도 23.6°C 조건으로 재배되었다. 2015년 8월31일에 파종한 파프리카는 코코피 트(Dutch plantin, Netherlands, 100cm × 15cm × 10cm) 배지에 2015년 11월12일에 정식하였으며, 양액 공급은 그로단표준액(NO3-N 17.50, NH4-N 0.80, PO4-P 4.20, K 7.10, Ca 10.40, SO4-S 3.80 me·L−1)을 일사량 비례 방식으로 공급되었으며, EC 2.0~3.0 dS·m−1, pH 5.5 조 건에서 2015년 9월부터 2016년 7월까지 재배되었다.
2. 일반 식물체 분석법과 신속진단 방법간 상관성 분석
경남농업기술원 ATEC온실에서 2015년 9월 10일에 정 식된 파프리카 2품종인 Raon red, Raon yellow 이용하 여 분석시료를 채취하였다. 2016년 1월7일부터 6월20일 까지 생육단계를 2그룹부터 5그룹 과실 비대기까지 4단 계로 구분하여, 목표 수확 과실의 비대 시점에 각 착과 그룹 과실 하단 잎을 1주당 4장씩, 12주에서 총 48장의 잎을 관행 또는 신속분석 시료로서 품종별로 나누어 각 각의 봉투에 채취해 보관하였다. 2그룹비대기(정식 후 119일) 9~11번째 마디, 3그룹비대기(정식 후 168일) 17~19번째 마디, 4그룹비대기(정식 후 222일) 24~26번 째 마디, 5그룹비대기(정식 후 284일) 32~34번째 과실 아래 잎을 채취하였다. 엽 채취 후 3시간 이내에 엽병과 엽신을 분리하고 3일동안 열풍건조기(FO-600M, JEIO TECH)를 이용해 70°C에서 건조한 후 마쇄하여 건물시 료를 조제하였으며 Cataldo 등 (1975) 법에 따라, NO3- 표준용액을 이용하여 검량선을 작성하고 정량하였다. 시 료당 분말시료 0.1g씩 총3개의 샘플을 만들어 100mL의 3차 증류수를 가하고 45°C 1시간동안 항온수조에서 추출 해 균질화 한 후, 5% Salicylic acid 200uL를 가해 실온에 20분간 방치하고 2N NaOH 5mL를 첨가해 교반하고 20분 후 분광광도계(Multiskan Go, Thermo Scientific, USA)를 이용해 410nm에서 흡광도를 측정하였다(Cataldo 등, 1975). 동일 채취시점과 부위의 엽병과 엽신을 분리하여 각각 착즙기로 즙액을 짠 후, 2.0mL 튜브에 담아 15분 간 13,453g로 원심분리하고 상등액을 냉동 보관하여 저 장하였다. 확보된 엽병과 엽신의 즙액은 NO3- 농도를 측 정하기 위해 각각의 샘플 당 3반복씩 증류수로 100배 희석해 RQ-flex®10(Merck, Germany)을 이용하여 정량 하였다. NO3- test strip(측정범위 5-225 mg·L−1)을 희석 액에 2초간 침지하고 60초 반응시간이 지난 후에 기기 에 삽입하여 즙액 내 농도를 측정하였다.
3. 품종 및 착과그룹별 질산태질소함량 모니터링
경남농업기술원 ATEC 온실에서 겨울작형으로 재배된 ‘Nicole’(Kooij Korea Seed, Korea), ‘TP2001’ (Kooij Korea Seed, Korea)의 2 품종의 NO3- 함량을 관행 방법 및 test strip을 이용한 신속분석방법을 각각 이용하여 생 육단계별로 모니터링 하였다. 2015년 11월12일부터 6월 20일 까지 생육단계를 1그룹 부터 5그룹 비대기까지 5 단계로 구분하여, 목표 수확 과실의 비대 시점에 각 착 과그룹 과실 하단 잎을 1주당 4장씩, 12주에서 총 48장 의 잎을 관행 또는 신속분석 시료로서 채취하였다. 1그 룹비대기(정식일: 56일, 채취일: 15년 11월5일) 2~3 번 째 마디, 2그룹비대기(정식일: 119일, 채취일: 16년1월7 일) 9~11번째 마디, 3그룹비대기(정식일: 168일, 채취일: 16년2월25일) 17~19번째 마디, 4그룹비대기(정식일: 222 일, 채취일: 16년 4월19일) 24~26번째 마디, 5그룹비대 기(정식일: 284일, 채취일: 16년6월20일) 32~34번째 과 실 하단 잎을 채취하였다. 즙액시료의 확보는 상관분석 실험과 동일하게 진행되었다.
4. 파프리카 수관 전체의 마디별 엽 내 질산태질소 함량
경남농업기술원 ATEC 온실에서 2015년 11월12일 정 식 후 310일 된 적색품종 ‘Speero’ (Kooij korea seed, Korea)와 2016년 정식 후 301일 된 ‘Nicole’ (Kooij korea seed, Korea) 품종을 두 차례에 걸쳐 겨울작형 파 프리카의 수관 전체의 마디별 잎을 채취하였다. 마디는 방아다리 이후 14번째 마디 과실 하단부 잎부터 36번째 잎까지 짝수번째 마디를 채취하였고, 1주당 2장씩 10주 에서 총 20장의 잎을 채취하였다. 채취한 잎은 3시간 이 내에 착즙기를 사용하여 엽병 즙액을 확보한 뒤 2.0mL 튜브에 담아 15분간 13,453g원심분리하고 상등액은 냉 동 보관하여 저장하였다. 즙액 샘플은 간이영양진단기기 인 RQ-flex®10(Merck, Germany)을 이용해 샘플 1개당 3반복씩 NO3- 농도를 측정하였다.
5. 파프리카 엽병즙액 내 질산태질소 함량 일변화 분석
파프리카 식물체 내 NO3- 함량의 일변화 모니터링을 위하여 전북대학교 실험포장 플라스틱하우스(54m2)에서 코코피트 슬라브(JLife, Korea, 100cm × 15cm × 10cm) 당 3 주씩, 30cm × 25cm 간격으로 2줄씩, 총 108주의 적색 품종인 Nagano(Rijk Zwaan, The Nederland)를 정 식하여 2016년 5월 6일부터 7월 29까지 하우스 평균 온 도 28.7°C에서 재배되었다. 양액조성은 PBG표준액(NO3- N 12.50, NH4-N 0.50, P 3.00, K 5.75, Ca 7.00, Mg 2.25, SO4-S 2.00 me·L−1)을 이용하였으며, EC 3.0~3.2 dS·m-1 pH 5.7조건에서 재배하였다. 채취 시간은 오전 9 시부터 자정 12시까지 1시간 마다 총 16회 채취하였고, 1주당 총 4장씩 1그룹 과실 하단부 잎을 이용하였다. 채 취한 후 착즙기로 즙액을 짠 후 원심분리하여 냉동 보 관하였다. 보관한 즙액 샘플은 위 실험과 같은 방법으로 NO3- 농도를 측정하였다.
결과 및 고찰
1. 기존 식물체 질산태 질소 분석법과 신속진단 방법 간 상관성 분석
소과종 ‘Raon red’, ‘Raon yellow’의 2그룹부터 5그룹 까지 4단계로 구분하여 채취한 엽병과 엽신을 각각 간 이영양진단기기와 분광광도계를 이용하여 정량분석하고 NO3- 함량과의 상관분석을 실시하였다. 엽병 즙액의 test strip 측정 농도와 엽신의 함량 간에는 R2=0.6734로 유 의적인 상관관계를 보였다(Fig. 1A). Studstill 등(2006) 은 엽병즙액의 분석만으로 특정 작물의 영양상태를 신속 하게 파악할 수 있으며, Kim(2011) 역시 일반 파괴적 분석법과 test strip에 의한 신속 분석법 간에 높은 상관 성(R2=0.76)을 확인하였고 파프리카 엽병 즙액을 활용한 신속한 영양진단의 가능성을 제시한 바 있다. 본 실험에 서도 test strip으로 엽병 즙액 내 질산태질소의 농도가 높아지면 엽신 내 함량도 증가함이 확인되어 엽병 즙액 의 분석은 식물체의 질소 영양상태를 신속하게 진단 할 수 있는 간접적인 유용한 지표가 될 수 있을 것으로 판 단하였다. 또한, test strip으로 측정한 엽신 부위의 즙액 내 질산태질소 농도와 엽신 내의 함량 간에는 엽병 즙 액에서보다 더욱 높은 상관관계를 보여(R2=0.8628) 엽신 부위의 즙액을 이용한 신속분석 방법으로도 질산태질소 의 수준 파악이 가능한 것으로 확인되었다(Fig. 1B). Kim 과 Kim(2003)은 엽병 즙액 내 NO3- 함량은 재배 환경 조건에 따라 민감하게 변하기 때문에 식물체의 질 소 이동 및 대사 연구에 엽병 즙액 분석이 효과적이라 고 하였으며, 실용적으로 엽신보다는 엽병 즙액이 양적 인 확보 측면에서 용이하기 때문에 신속한 분석 차원에 서 더욱 유리할 것으로 판단된다.
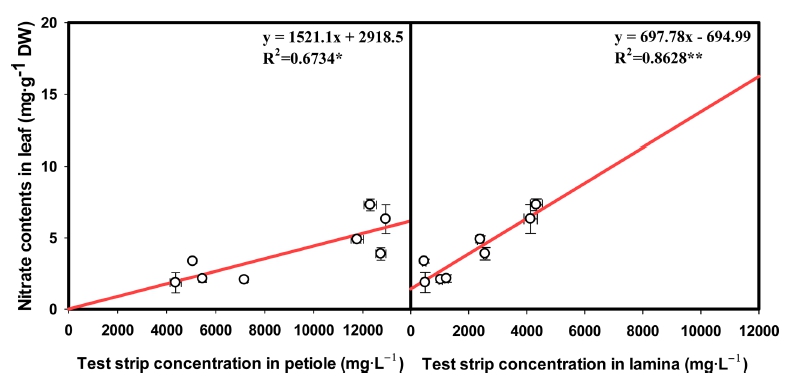
Fig. 1.
Correlation between rapid (X-axis) and spectroscopic (Y-axis) methods for nitrate contents in leaf petiole sap and leaf blade sap. A: correlation between nitrate concentration in leaf petiole sap using rapid detection kit and the leaf contents analysed by spectroscopy method; B, correlation between nitrate concentration in leaf blade sap using rapid detection kit and the leaf contents analysed by spectroscopy method. Vertical bars represent standard deviation of the means (n=3).
2. 생육단계별 엽병 즙액 내 질산태질소 농도 및 엽 내 함량 분석
대과종 ‘Nicole’, ‘TP2001’과 2품종을 1그룹부터 5그 룹까지 단계별로 나누어 채취한 엽병과 엽신을 각각 test strip 과 분광광도계를 이용하여 분석하였다(Fig. 2).
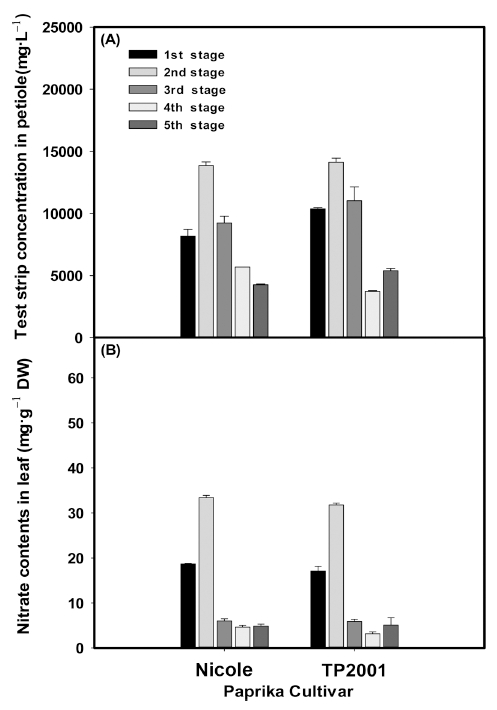
Fig. 2.
Nitrate concentration in leaf petiole sap analysed by test strip-based rapid detection kit (A) and spectroscopy method (B) at different fruit enlargement stages of winter cropping paprika cultivars (‘Nicole’ and ‘TP2001’). The vertical black boxes represent an average value of five growth stages. Each vertical bars represent mean ± standard deviation of the three replications.
착과 그룹별로 총 5단계로 대과종 2품종(Nicole, TP2001)의 엽병 즙액 내 질산태질소 농도와 엽 내 함량 을 비교 분석한 결과 ‘Nicole’과 ‘TP2001’ 두 품종 모두 2그룹 비대기 단계에서 높은 농도 및 함량을 보였으며, 생육단계가 진전됨에 따라 낮아지는 경향을 보였다(Fig. 2A, 2B). 고추에서도 생육이 진행될수록 엽병 즙액 농도 와 엽 함량이 유사하게 낮아지는 경향을 보이고 있다 (Hochmuth, 1994). Test strip과 분광광도계 분석 방법 간에 상응하는 생육단계별 경향은 완전히 일치하지 않지 만, 전반적인 감소 경향을 확인할 수 있었다. 두 품종간 에는 NO3- 함량 값이 비슷하지만, 생육단계별로는 함량 의 차이를 보이고 있다. Kim 과 Kim(2003) 또한, 오이 에서도 생육단계별로 함량 값이 차이가 있기 때문에 정 확한 영양상태 파악을 위해서는 생육단계별로 적정 함량 을 달리 정해야 한다고 보고하였다. ‘Nicole’ 엽병 즙액 의 질산태질소 평균 농도는 8,246 mg·L−1, ‘TP2001’는 8,923 mg·L−1 으로 동일 대과종인 두 품종간에 비슷한 평균 값을 보이고 있다(Fig. 2A). 잎의 평균 함량 또한 ‘Nicole’은 13mg·g-1 DW, ‘TP2001’은 12 mg·g-1 DW로 유사한 함량을 보이고 있다(Fig. 2B).
생육단계별로 test strip과 분광광도계를 이용해 분석한 결과, 경향은 유사하지만 각각의 단계를 세분화해서 비 교하면 상이한 결과를 보이고 있으며, 파프리카 식물체 는 특정 부위의 초장이 매우 크기 때문에 적절한 반복 수를 확립하지 않으면 양분 이동 파악의 편차가 크기 때문으로 추정된다. 또한, 일반적으로 파프리카는 적산일 사량에 대응하여 양액을 공급하기 때문에 양액 공급 시 점에 따라 즙액 내 농도의 편차가 큰 가능성이 있기 때 문에 시료채취를 할 때 양액 공급 개시 및 중단시점을 고려하여 특정 시점에 채취 후 신속 분석하며, 한 배지 에 있는 식물체들을 한 반복으로 채취하거나 반복수를 늘려야 할 것으로 판단된다.
종합적으로, 엽병 즙액 내 NO3- 함량이 서로 부합하였 고 생육이 진전됨에 따라 엽병즙액과 엽신 내 NO3- 함 량이 낮아지는 경향을 확인하였다.
3. 파프리카 수관 전체의 마디별 엽병 즙액 내 질소 농도 분포
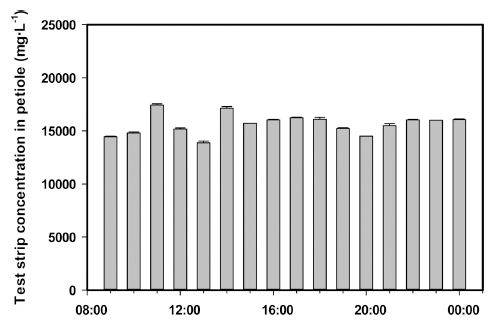
상관분석의 결과로부터 엽병 즙액의 분석으로 엽 내 NO3- 함량의 간접적 파악이 가능한 것으로 추정되어, 파 프리카 전체 마디별 NO3- 분포를 test strip에 의한 신속 분석법에 의하여 분석하였다. 정식 310일 후의 파프리카 식물체 엽병 내 질산태 질소를 14번째에서 36번째 마디 별로 test strip을 이용해 신속 분석한 결과, 정단부의 마 디일수록 질산태질소 함량은 낮아지는 것을 확인하였다 (Fig. 3A, B). Kim 과 Kim(2003)에 따르면, 오이 역시 상단 신초에서 NO3- 농도가 높아짐을 확인하였고, 본 연 구에서도 파프리카 역시 엽병 즙액으로 측정한 상위엽과 하위엽의 질산태 질소 농도 차이는 2배 이상 큰 차이를 보였기 때문에 질산태 질소의 경우 엽병 즙액 농도로 전 체 식물체의 영양을 진단할 때 부위의 선택에 따라 큰 변이가 있을 수 있음이 확인되었다. 동일 재배 온실에서 연차간에도 엽병 즙액의 농도 범위는 차이를 보였는데, 2016년에 재배한 ‘Nicole’ 품종의 평균은 12,838mg·L−1을 나타내었으며(Fig. 3A), 2015년에 ‘Speero’의 모든 부위 평균 농도 값은 16,019 mg·L−1이였다(Fig. 3B). 본 연구 결과를 토대로 평균 농도에 해당하는 마디는 24-26마디 라고 추정할 수 있으며, 연차간 차이 발생 이유는 샘플 채취 당시 식물체의 양액조건 및 기상환경조건이 다르기 때문으로 판단되며 질산태 질소의 경우, 하단과 상단의 농도 구배가 크기 때문에 장기 재배시 재배 후반부 상 단 또는 결실 부위 질소영양의 유지 관리가 중요할 것 으로 판단된다. NO3- 함량의 일변화에서는 시간대 별로 큰 차이 없이 비슷한 경향을 보였는데, 11시와 3시에 NO3- 함량이 다소 높은 것을 볼 수 있었으나(Fig. 4), 대 체적으로 질산태질소 함량은 하루동안 큰 변화 없이 평 균 농도(15,639 mg·L−1) 근방으로 유지되었다.
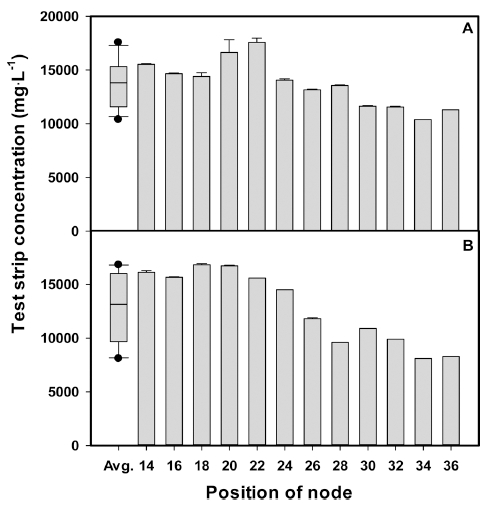
Fig. 3.
Yearly variation of nitrate concentration in the petiole sap of different nodes of ‘Nicole’ using rapid detection kit. A, petiole sap samples from 2016; B, petiole sap samples from 2015. The left variation boxes represent an average value of 12 nodes. Each horizontal bar represent mean ± standard deviation of the three replications.
파프리카 등 장기 배지경 수경재배 채소의 정확한 영 양상태의 파악은 생리장해 경감 및 생산성 증대에 있어 서 중요한 지표가 되며(Del Amor, 2006), 생육단계, 품 종, 환경에 따라서도 적절한 무기원소의 필요 범위가 다 르기 때문에, 각 시기에 맞는 적절한 동적 양액관리가 필요하다(Bennett, 1993).
본 연구에서는 간이영양진단기기로 파프리카의 엽병 즙액 분석을 통해 간접적으로 엽 내 질소 함량을 모니 터링한 결과 생육단계별 신속한 분석이 가능함을 확인하 였으며, 품종 및 부위별 차이도 있음을 파악할 수 있었 다. 또한, 농가에서 간이영양진단기기를 이용하여 질소의 영양상태 파악을 통한 합리적인 시비의 가능성이 검토되 었으며 신속분석 기기를 활용한 영양진단 접근법은 장기 재배 과채류의 변동 환경조건에서의 신속한 시비관리 및 대처를 위하여 유용한 기술이 될 것으로 예상된다.
본 연구는 시간과 노력이 많이 소요되는 관행 파괴적 무기성분 분석방법을 대체하여 이용할 수 있는 현장 적 용 가능 신속 모니터링 기술의 개발을 주된 목표로 하 였으며, 일차적으로 신속분석기기를 이용한 즙액 내 질 산태질소의 수준이 관행의 분석방법을 반영할 수 있는지 확인하고, 이차적으로 다양한 환경조건에서 재배된 파프 리카 식물체의 생육단계 및 수관전체의 질산태질소 농도 분포의 신속한 파악이 가능함을 검증하였다. 향후 동일 품종에 대하여 좀 더 다양한 부위 및 생육단계에서 반 복수를 늘려 분석함으로써 정상 또는 불량 환경에서 재 배되고 있는 파프리카의 신속 영양진단을 위한 표준 무 기성분 범위의 제시 및 농가 현장에서의 신속분석기술 확립이 가능할 것으로 판단된다.