서 론
재료 및 방법
1. 실험재료
2. 생리활성물질 분석
3. 통계분석
결 과
1. 성숙단계에 따른 칼리스테핀 함량 변화
2. 성숙단계에 따른 시아니딘-3-글루코사이드 함량 변화
3. 성숙단계에 따른 (+)-카테킨 함량 변화
4. 성숙단계에 따른 에피카테킨 함량 변화
5. 성숙단계에 따른 퀘르세틴-3-글루코사이드 함량 변화
6. 성숙단계에 따른 퀘르세틴 함량 변화
7. 성숙단계에 따른 클로로겐산 함량 변화
8. 성숙단계에 따른 엘라그산 변화
9. 성숙단계에 따른 신코닌 함량 변화
고 찰
서 론
딸기(Fragaria × ananassa Duch.)는 장미과의 초본성 다년생 식물로 우리나라의 시설 과채류 중에서 생육적온이 가장 낮은 저온성 작물로 난방비 부담이 적어 겨울철 시설재배에 유리한 작물이다. 특히 우리나라 환경에 적합한 재배작형이 잘 확립되어 고품질의 신선 딸기를 생산하고 있으며 다른 시설작물에 비해 가격도 안정화되어 시설재배 농가의 주요 소득작물로 자리 잡고 있다. 국내 딸기 재배면적과 생산량(2022)은 각각 5,745ha와 158,807톤이고 생산액은 14,717억원으로 전체 채소류 생산액의 11.6%를 점유하고 있다(MAFRA, 2022).
최근 건강 기능성 성분으로 채소작물에 함유된 안토시아닌, 플라보노이드 및 폴리페놀 화합물과 같은 생리활성물질에 대한 관심이 높아지고 있다(Naczk와 Shahidi, 2003; Nile과 Park, 2014). 생리활성물질이란 식물에서 만들어지는 모든 유기화학 물질을 통틀어 일컫는 개념으로 식물 자체에서는 자신과 경쟁하는 식물의 생장을 방해하거나 불량한 환경, 각종 미생물 또는 해충 등으로부터 보호하기 위해 만들어지는 물질로 지금까지 2만 5천 종류가 발견되었다(Alan 등, 2011; Molyneux 등, 2007; Palermo 등, 2014; Smith-Warner 등, 2003). 채소작물에는 여러 가지 영양성분과 다양한 생리활성물질이 함유되어 있는데, 이러한 각종 유용한 성분들은 품종의 유전적 특성, 재배환경과 지역, 과실의 성숙단계 및 수확 후의 가공 등에 의해서 차이가 있다(Bae 등, 2019; Bobinaite 등, 2012; Jeong 등, 2024; Saridas 등, 2022; Yong 등, 2019; Zhang과 Hamauzu, 2003). 특히 딸기에는 항산화물질인 유기산과 비타민 C 뿐만 아니라 엘라그산이나 클로로겐산과 같은 다양한 폴리페놀화합물이 많이 함유되어 있다(Bae 등, 2019; Kim 등, 2010b; Koyama 등, 2022; Lee 등, 2015; Panico 등, 2009).
과실이나 채소작물 등에 많이 함유되어 있는 폴리페놀 화합물은 다양한 구조와 분자량을 가진 2차 대사산물로 액포 또는 세포막에 존재한다(Branen, 1975). 식물에서 폴리페놀 화합물은 벤조산과 계피산의 유도체인 페놀산, 플라보노이드 및 탄닌의 형태로 분류되는데, 폴리페놀 화합물의 항산화력은 페놀 화합물의 구조에 따라 차이가 있다(Moure 등, 2001). 또한 폴리페놀 화합물은 수산기를 갖고 있기 때문에 단백질 및 기타 거대 분자들과 쉽게 결합하며 항산화와 항암 등의 다양한 생리활성을 가진다고 알려져 있다(Isemura 등, 2000; Lee 등, 2005; Naczk와 Shahidi, 2003; Rice-Evans 등, 1996; Rice-Evans 등, 1997; Yoo 등, 2005). 채소작물이나 과실에는 캠페놀, 퀘르세틴, 퀘르세트린, 갈릭산, 카테킨, 크로로제닉산, 카페익산 및 코마릭산 등과 같은 페놀 화합물이 존재하는데(Bandyopadhyay 등, 1990; Liu 등, 2012), 각종 비생물학적인 환경스트레스에 대한 저항성을 증가시키기도 하고 병원체나 다양한 불량환경으로부터 보호 역할을 하는 것으로 알려져 있다(Hernandez 등, 2009; Mann, 2014; Samec 등, 2021; Treutter, 2010). 또한 폴리페놀 화합물이 산화적 스트레스를 줄이고, 만성적인 질병을 예방하는데 효과적이라는 것이 알려져 다양한 식물을 대상으로 폴리페놀 화합물의 항산화 능력에 관한 연구가 활발히 진행되었는데(Alvarez-Fernandez 등, 2014; Bandyopadhyay 등, 1990; Chisari 등, 2010; Jafarinia 등, 2020; Kang과 Salveit, 2002; Mann, 2014; Wahyuni 등, 2013), 폴리페놀 화합물의 함량이 높을수록 라디컬 소거능이나 환원력간에는 상관관계가 있다(Cantin 등, 2009). 폴리페놀 화합물의 함량이 높은 고추와 같은 가지과 작물의 과실은 위암, 폐암 및 전립선암을 예방하고 식욕증진, 혈압강하, 혈액순환 증진 및 피로회복 등의 생리활성 작용을 하는 중요한 작물이다(Davies와 Hobson, 1981; Davis 등, 1970; Kim 등, 2006; Lee 등, 1995; Materska 등, 2003; Song 등, 2010; Zhang과 Hamauzu, 2003). 또한 폴리페놀 화합물은 각종 환경 스트레스에 의해서 유기되는 산화적 스트레스에 대한 식물의 저항성을 증가시키는데, 식품으로 섭취하면 항산화제로서 스트레스 감소와 더불어 만성질환 예방에 효과적이라는 보고도 있다(Andersen 등, 2004; Chisari 등, 2010; Hernandez 등, 2009; Zheng 등, 2007). 식물에서 폴리페놀 화합물의 합성은 식물의 종, 발육과정 또는 성숙과정에 따라 조절되는데(Macheix 등, 1990), 딸기나 참다래 과실의 폴리페놀 화합물 함량과 항산화력은 성숙과보다는 미숙과에서 높은데(Oh 등, 2011; Shin 등, 2008) 비해 복분자나 유자의 경우에는 성숙될수록 페놀 화합물의 증가와 더불어 활성이 높다고 하였다(Cha 등, 2007; Yoo 등, 2005). 또한 같은 종이지만 품종에 따라 성숙과정별로 페놀 화합물의 함량이나 항산화력 차이가 반대의 경향을 보이는 연구 결과도 있다(Thanyaporn 등, 2004). 이러한 연구결과는 작물의 종류, 품종, 과실의 부위 및 과실의 성숙단계에 따라 폴리페놀 화합물의 함량과 더불어 항산화력에도 차이가 있다.
딸기의 과실 색은 수정 후 과실이 비대하여 성숙하면서 적색으로 변하는데, 품종에 따라 과실의 색은 다양하여 과실의 품질을 결정하는 주된 요인 중의 하나이기도 하다. 과실의 과색은 안토시아닌 함량에 의해서 결정되며 성숙단계가 진전될수록 안토시아닌 함량이 급격히 증가하여 빨간 딸기가 된다. 그러나 최근에는 성숙과정 중에 안토시아닌 색소의 합성이 줄어들거나 합성되지 않아 과색이 연한 분홍색이거나 흰색을 나타내는 딸기가 개발되어 재배자와 소비자의 관심을 받고 있다. 과실색이 빨간 딸기의 영양학적 또는 생리활성물질에 대한 연구는 많이 진행되었지만, 최근 소비자의 관심이 높은 과실색이 흰색이거나 분홍색인 딸기의 성숙단계에 따른 생리활성물질의 축적 양상에 대한 정보는 아직 미흡한 실정이다. 따라서 본 연구는 추출용매에 따른 딸기과실의 생리활성물질 추출효율을 검정하여 산업화를 위한 기초자료를 제공하고자 하였다. 또한 완숙기의 과실색이 빨간색과 분홍색인 딸기 품종의 성숙단계에 따른 폴리페놀 화합물의 축적 양상을 비교 분석하여 고품질 기능성 딸기 생산과 소비자에게 유용한 정보를 제공하고자 수행하였다.
재료 및 방법
1. 실험재료
실험에 사용한 딸기(Fragaria × ananassa Duch.) 품종은 성숙한 과실의 색이 적색인 설향과 분홍색인 만년설을 사용하였다. 과실의 성숙단계는 수분 후 13일경인 녹숙기(green), 26일경인 변색기(turning), 및 39일 경인 완숙기(mature)로 구분하여 수행하였다(Fig. 1). 실험용 딸기는 경남 산청군 단성면에 위치한 양액재배농가에서 2화방 과실을 착과 후 2월 10일에서 3월 20일 사이에 채취하였다. 분석용 딸기 과실은 전체 하우스에서 완전임의배치 3반복으로 반복당 3지점(9지점)을 선정한 후 각 지점에서 9개의 과실을 성숙단계별로 채취하여 동결건조한 후 분쇄하여 생리활성물질 분석용으로 사용하였다.
2. 생리활성물질 분석
2.1 시료의 처리
분석용 딸기 과실 시료는 채취하여 -70℃ 초저온 냉동고에서 급냉시킨 후 동결건조기(Hypercool HC 3110, Hanil Scientific Inc., Seoul, Korea)에서 동결건조 시켰다. 균일하게 마쇄된 시료 0.5g을 15mL conical tube에 넣고 에탄올 70과 50% 및 물을 각각 10mL을 가하여 초음파 추출기에서 1시간 추출한 다음 3,000rpm에서 10분간 원심분리(Allegra 64R, Beckman, CA, USA)하여 상징액을 회수하였다. 회수하고 남은 침전물에 각각의 용액 10mL을 가하여 동일한 방법으로 3회 추출하여 상징액을 모은 다음 최종 부피를 30mL로 조정하여 HPLC 분석용 시료로 사용하였다.
2.2 시약 및 기기
HPLC 분석 및 시료의 추출에 사용한 유기용매는 Fisher Scientific(Fisher Scientific Korea, Seoul, Korea)의 HPLC급 용매를 사용하였다. HPLC 분석기기는 Agilent 1100 Series LC system(Agilent Technologies, Santa Clara, CA, USA)의 System controller, Photodiode array detector(PDA), auto sample injector, degasser를 사용하였으며 HPLC column은 Phenomenex사의 Luna C18 column(150 × 4.6mm, 5μm, Phenomenx, USA)을 사용하였다.
2.3 표준물질
생리활성물질 분석을 위한 표준물질은 Sigma-Aldrich (Sigma-Aldrich Chemical Co., MO, USA)사의 Callistephin, Cyanidin-3-glucoside, (+)-catechin, epi-catechin, quercitrin-3- glucoside, quercetin, chlorogenic acid, ellagic acid 및 cinchonine을 사용하였다.
2.4 HPLC 분석방법
표준물질의 정량분석은 용매별 추출물을 0.45μm syringe filter(Millipore, Billerica, MA, USA)로 여과하였다. HPLC는 Agilent 1100 series(Agilent Technologies Inc., CA, USA)이고 칼럼은 역상 칼럼인 Luna C18(5μm, 4.6 × 150mm), 검출기는 UV detector(254nm)를 사용하였다. 이동상은 0.025% formic acid(A 용액)과 acetonitrile(B 용액)을 사용하였고 펌프 프로그램을 통하여 gradient를 설정하였으며 유속은 0.8mL/min으로 하였다. 준비된 각각의 용액을 autosampler로 10μL씩 주입하여 분석하였다. HPLC로 얻은 chromtogram의 면적을 회귀직선방정식에 대입하여 각각 표준물질의 함량을 구했으며 각각의 시료에 대해 3반복하여 지표성분의 함량을 계산하였다. HPLC를 이용한 분석법의 신뢰도와 재현성을 검증하기 위하여 ICH 가이드라인에 의한 분석을 수행하였다. 직선성(linearity)은 5개의 농도(6.25, 12.5, 25, 50, 100μg/mL)별로 피크 면적을 구하여 표준물질 농도(X축)와 피크 면적비(Y축)에 대한 검량선을 작성하였으며 검량선으로 부터 직선성의 상관계수를 구하여 확인하였다.
3. 통계분석
성숙단계별로 채취된 모든 시료의 분석은 3반복으로 실시하였으며, 분석 결과는 SigmaPlot 12.0(SYSTAT, Chicago, IL, USA) 프로그램을 이용하여 평균과 표준 오차를 계산하였고, SAS 통계 프로그램(SAS, 9.4, nstitute Inc., USA)을 이용하여 Duncan’s multiple range test로 95% 유의수준에서 분석하였다.
결 과
1. 성숙단계에 따른 칼리스테핀 함량 변화
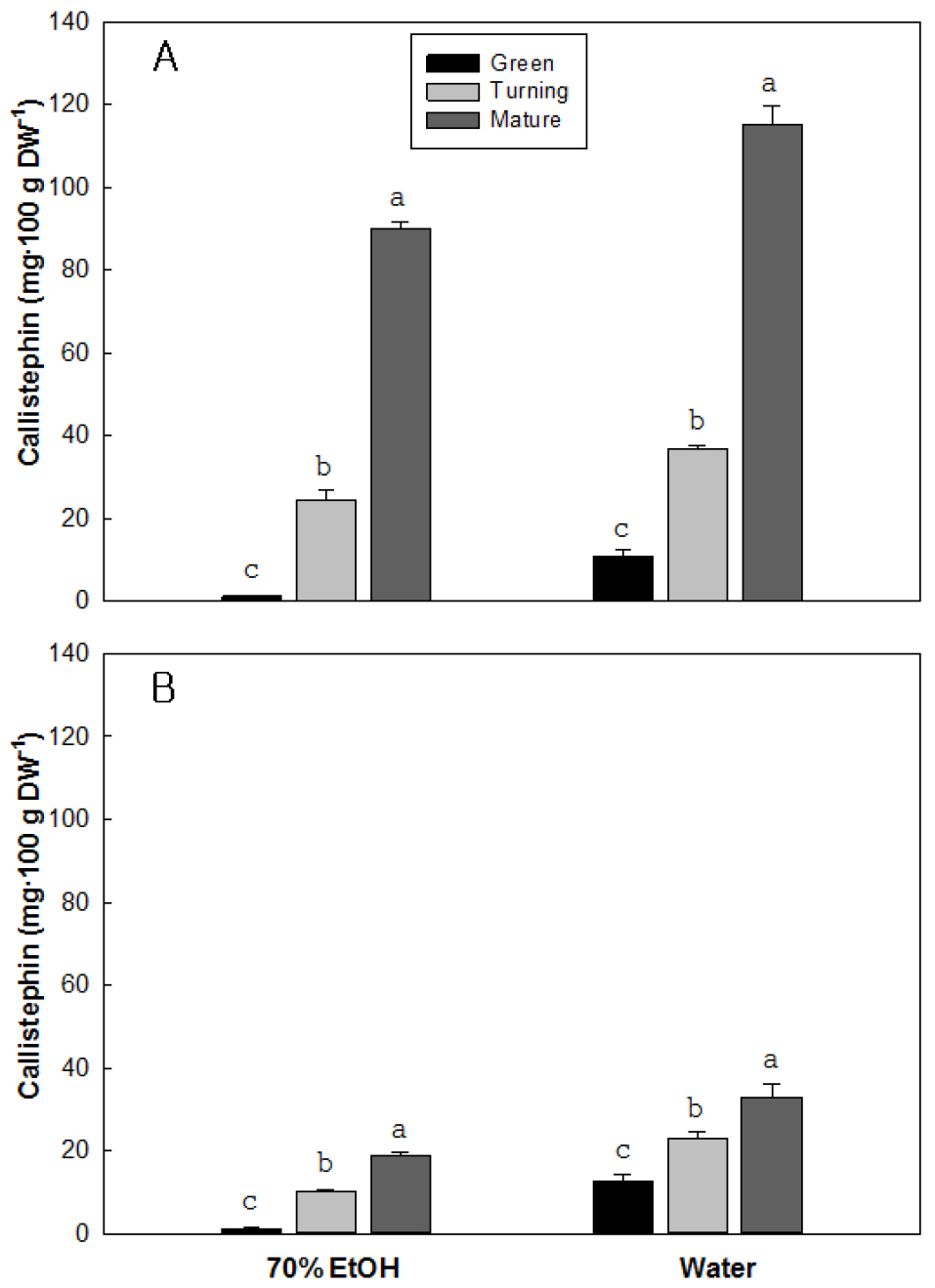
추출용매와 성숙단계에 따른 딸기 과실의 칼리스테핀 함량을 분석한 결과, 추출용매에 따른 추출효율은 에탄올보다는 물에서 다소 높았고 성숙단계가 진전될수록 증가하는 경향을 보였으며 과실색이 다른 두 품종 간의 함량 차이는 뚜렷하였다(Fig. 2). 과실색이 적색인 설향의 녹숙기 칼리스테핀 함량은 에탄올 70%와 물을 사용하여 추출할 경우 건물 100g 당 각각 1.1과 10.7mg인데 비해 변색기에는 각각 24.4와 36.8mg으로 증가하였고 완숙기에는 각각 90.5와 115.3mg으로 급격하게 증가하였다. 과실색이 분홍색인 ‘만년설’의 녹숙기 함량은 에탄올 70%와 물을 사용하여 추출할 경우 각각 0.9와 12.7mg인데 비해 변색기에는 각각 10.2와 22.9mg으로 증가하였고 완숙기에는 각각 18.8과 32.9mg으로 증가하였다. 그러나 전반적으로 ‘만년설’의 칼리스테핀 함량은 설향에 비해 낮은 경향을 보였다.
2. 성숙단계에 따른 시아니딘-3-글루코사이드 함량 변화
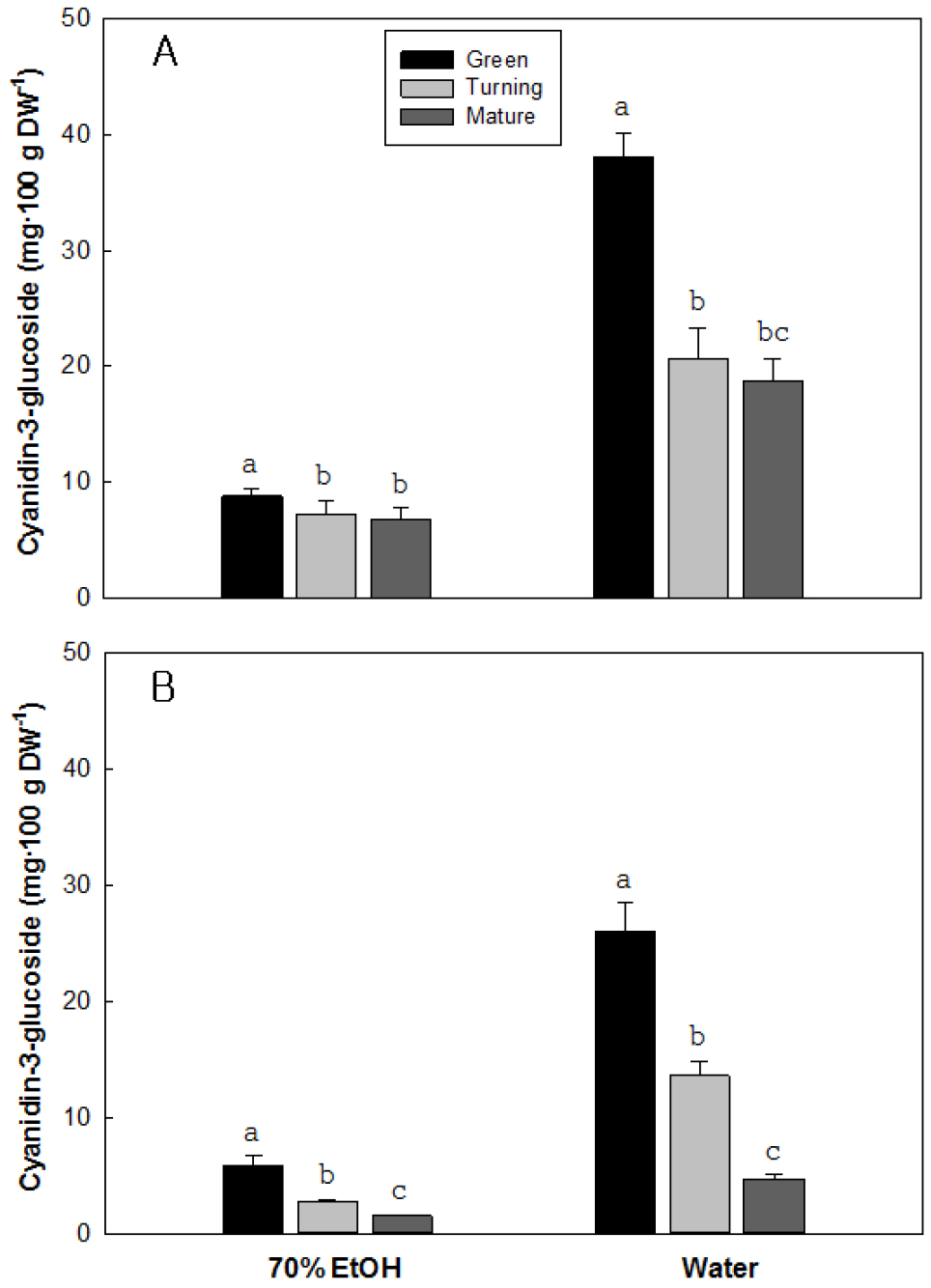
추출용매와 성숙단계에 따른 딸기 과실의 시아니딘-3-글루코사이드의 함량 변화를 분석한 결과, 추출효율은 에탄올에 비해 물이 월등하게 높았고 성숙과정에 따른 함량 차이도 있었다(Fig. 3). 설향의 시아니딘-3-글루코사이드 함량은 70% 에탄올을 사용하여 추출하면 건물 100g 당 녹숙기의 8.7mg에서 완숙기의 6.8mg으로 추출효율은 낮았고 성숙단계에 따른 차이도 크지 않았다. 그러나 물을 사용하여 추출하면 녹숙기의 시아니딘-3-글루코사이드 함량은 38.0mg으로 높았고 변색기와 완숙기에는 각각 20.7과 18.7mg으로 녹숙기 대비 각각 44.7과 50.8% 수준으로 감소하였다. ‘만년설’에서도 70% 에탄올을 사용하여 추출하면 시아니딘-3-글루코사이드의 함량은 녹숙기의 5.8mg에서 완숙기의 1.5mg으로 아주 낮았다. 그러나 물을 사용하여 추출하면 녹숙기에서 26.0mg으로 가장 높았고 변색기와 완숙기에는 각각 13.6과 4.7mg으로 급격하게 감소하는 경향을 보였다.
3. 성숙단계에 따른 (+)-카테킨 함량 변화
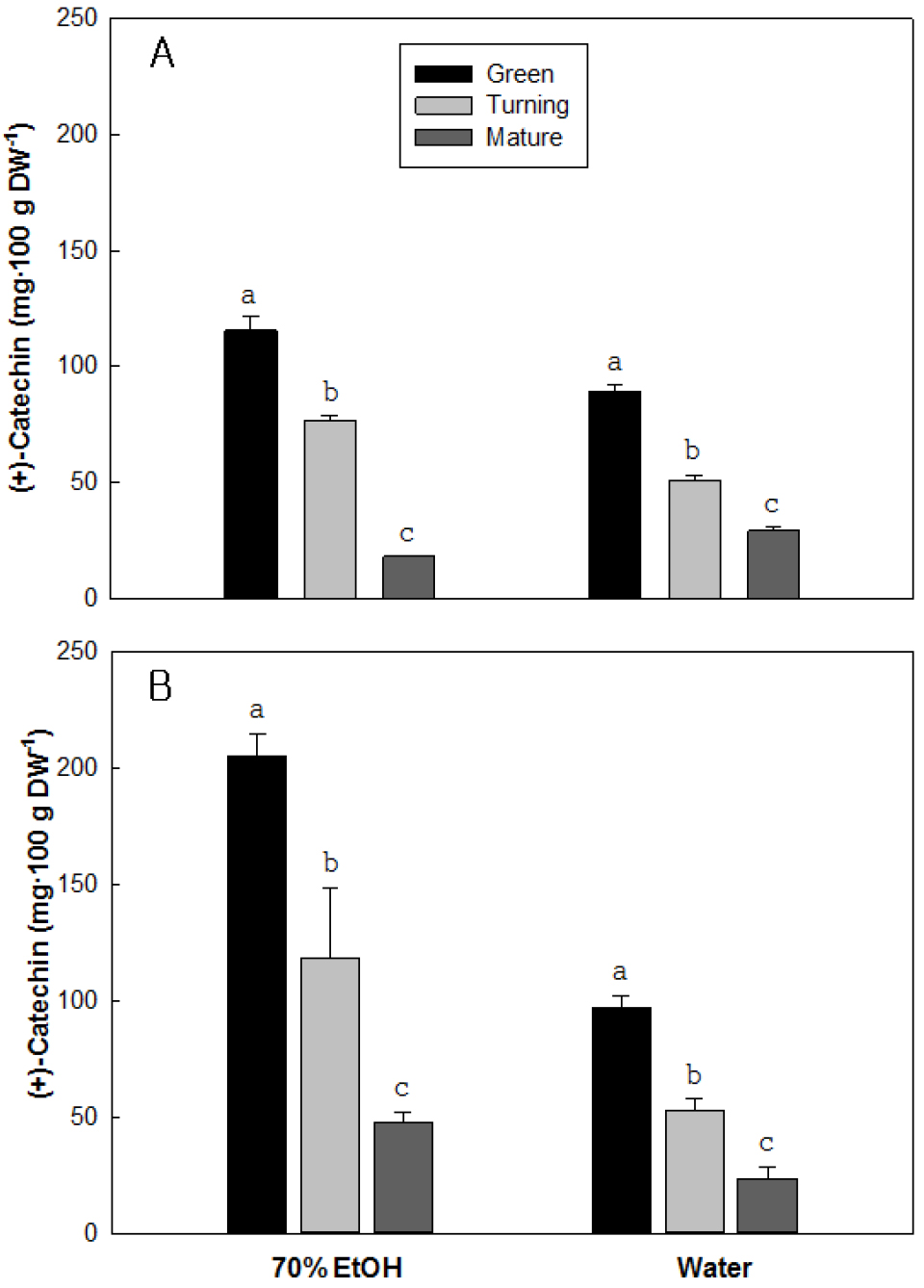
추출용매와 성숙단계에 따른 딸기 과실의 카테킨 함량 변화를 분석한 결과, 물보다는 에탄올을 사용할 경우에 추출 효율이 높았으며 성숙과정이 진행될수록 감소하는 경향을 보였다(Fig. 4). 설향의 녹숙기 카테킨 함량은 70% 에탄올과 물을 추출 용매로 사용할 경우에 건물 100g 당 각각 115.6과 89.2mg으로 70% 에탄올 추출 용매에서 높았다. 변색기에는 추출용매에 따라 각각 76.8과 51.1mg 수준을 보였고 완숙기에는 각각 18.2와 29.3mg 수준으로 급격하게 감소하였다. 만년설의 녹숙기의 카테킨 함량은 70% 에탄올과 물을 사용하여 추출할 경우에 각각 205.3과 97.2mg으로 추출용매에 따른 추출효율에는 큰 차이가 있었다. 이러한 카테킨의 함량은 성숙과정이 진행될수록 급격하게 감소하였는데, 변색기에는 70% 에탄올과 물을 추출용매로 사용할 경우에 각각 118.4와 52.8mg으로 감소하였고 완숙기에는 각각 47.5와 23.6mg으로 녹숙기 대비 각각 76.9와 75.77% 감소하였다.
4. 성숙단계에 따른 에피카테킨 함량 변화
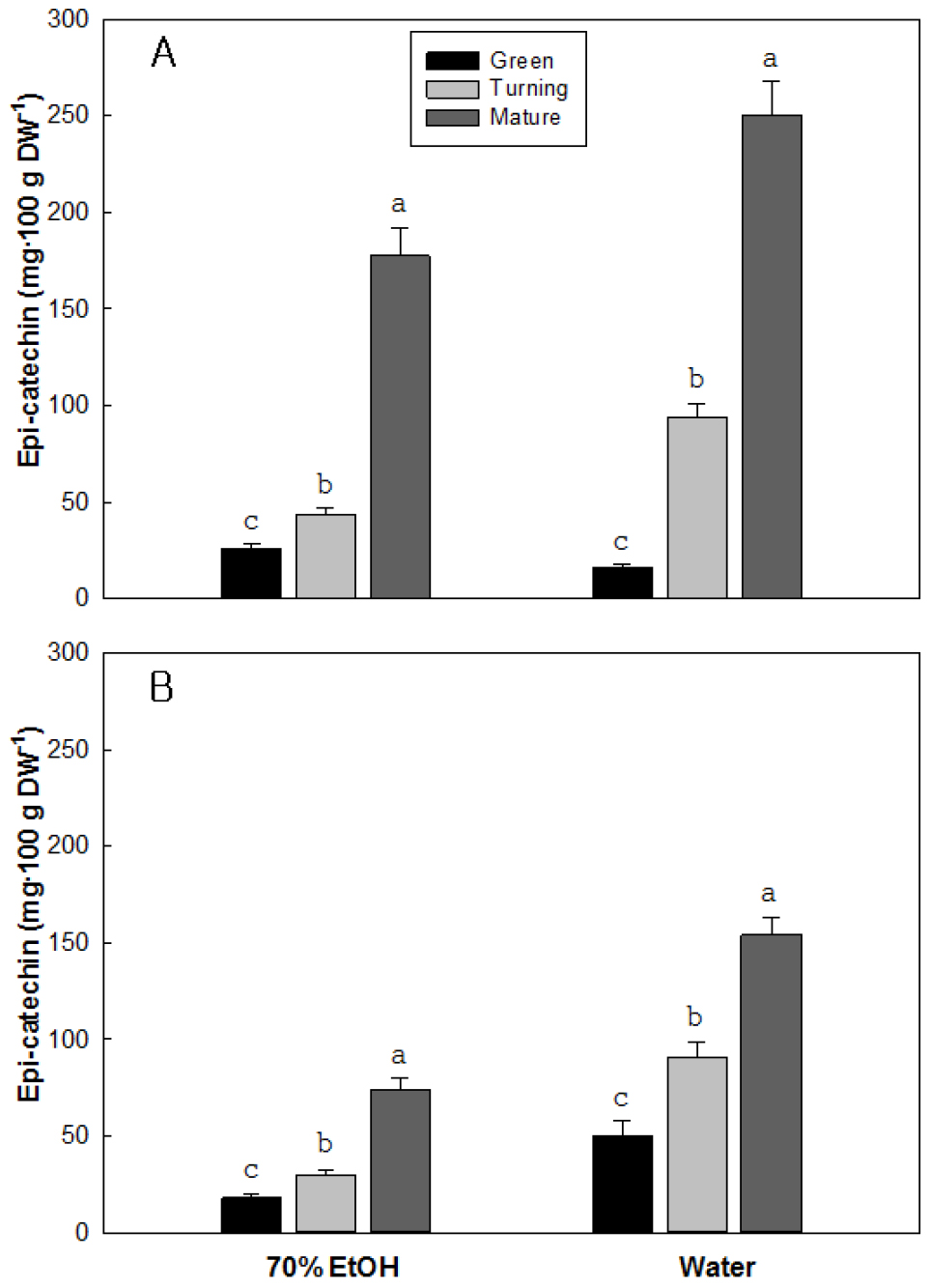
추출용매와 성숙단계에 따른 딸기 과실의 에피카테킨 함량 변화를 분석한 결과, 추출용매에 따른 추출효율은 에탄올보다는 물이 높았고 함량은 성숙 과정이 진행될수록 증가하는 경향을 보였다(Fig. 5). 과실 색이 적색인 설향의 녹숙기 에피카테킨 함량은 건물 100g 당 추출용애인 에탄올과 물에서 각각 15.7과 25.5mg 수준을 보였는데, 변색기와 완숙기에서 함량이 가장 높았던 추출용매는 물로서 각각 93.9과 250.3mg 수준으로 녹숙기 대비 각각 5.9배와 16.0배 수준으로 증가하는 경향을 보였다. 과실 색이 분홍색인 ‘만년설’의 에피카테킨 함량은 설향에 비해 낮은 경향을 보였는데, 가장 함량이 높았던 추출 용매는 물로서 녹숙기의 50.1mg에 비해 변색기와 완숙기에는 각각 91.1와 153.9mg으로 녹색기 대비 각각 1.8과 3.11배 수준으로 증가하는 경향을 보였다.
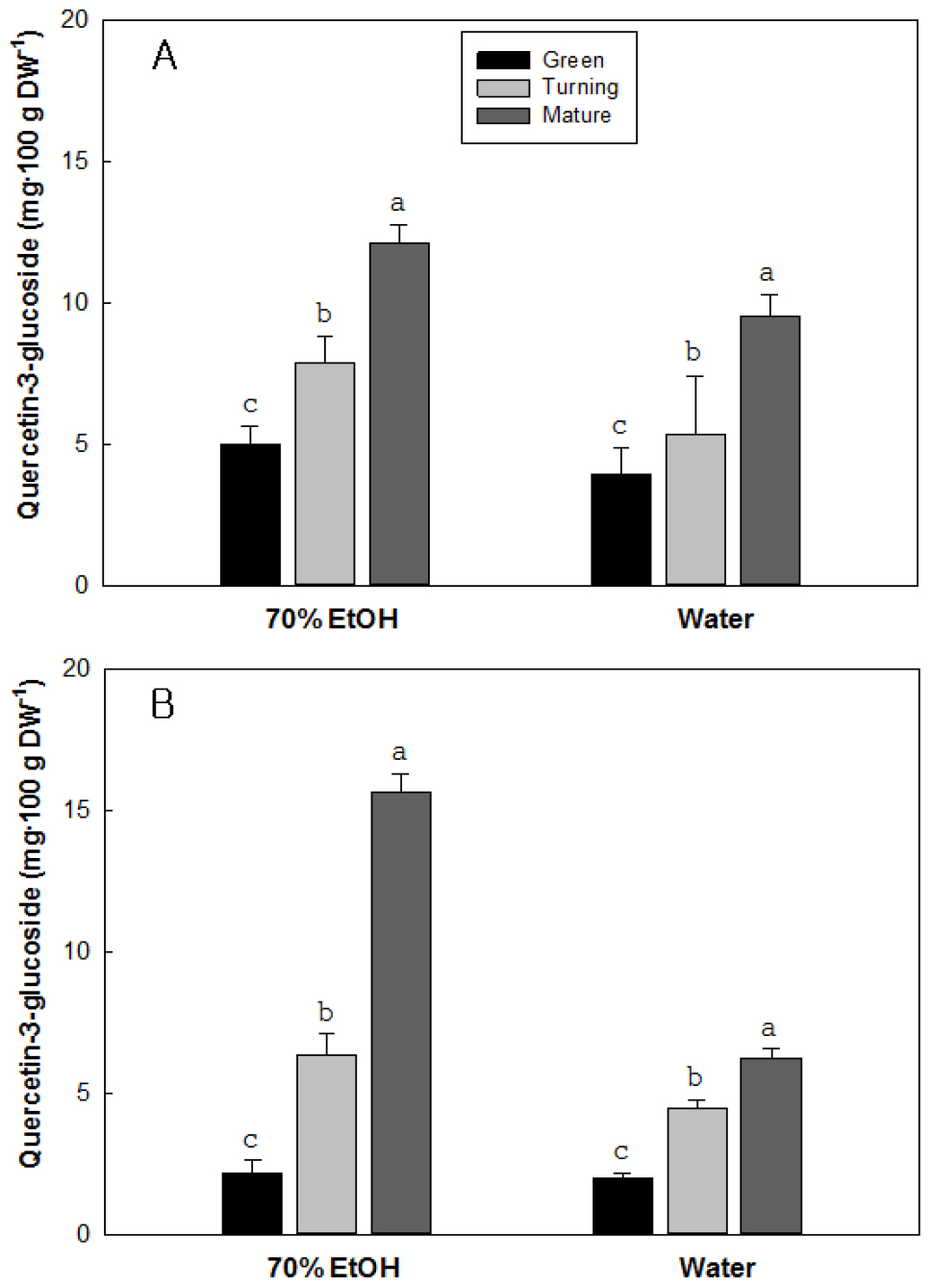
5. 성숙단계에 따른 퀘르세틴-3-글루코사이드 함량 변화
추출용매와 성숙단계에 따른 딸기 과실의 퀘르세틴-3-글루코사이드 함량 변화를 분석한 결과, 추출 효율은 물보다는 에탄올에서 효율이 높았으며 성숙이 진전될수록 급격하게 증가하는 경향을 보였다(Fig. 6). 설향의 퀘르세틴-3-글루코사이드의 함량은 성숙 과정이 진행될수록 증가하는 경향을 보였는데, 녹숙기의 함량은 건물 100g 당 5.0과 3.9mg 수준으로 추출용매에 따른 큰 차이는 없었다. 변색기의 함량은 추출용매인 70% 에탄올과 물에서 각각 7.8과 5.3mg 수준으로 녹숙기에 비해 다소 높았고, 완숙기에는 추출 용매에 따라 12.2에서 9.5mg 수준으로 녹숙기에 비해 2배 이상 증가하는 경향을 보였다. 만년설의 퀘르세틴-3-글루코사이드 함량은 성숙 과정이 진행될수록 증가하는 경향을 보였는데, 완숙기의 함량은 에탄올로 추출할 경우에는 건물 100g 당 15.7mg 수준으로 높았지만, 물을 사용할 경우에는 6.2mg 수준으로 낮았다.
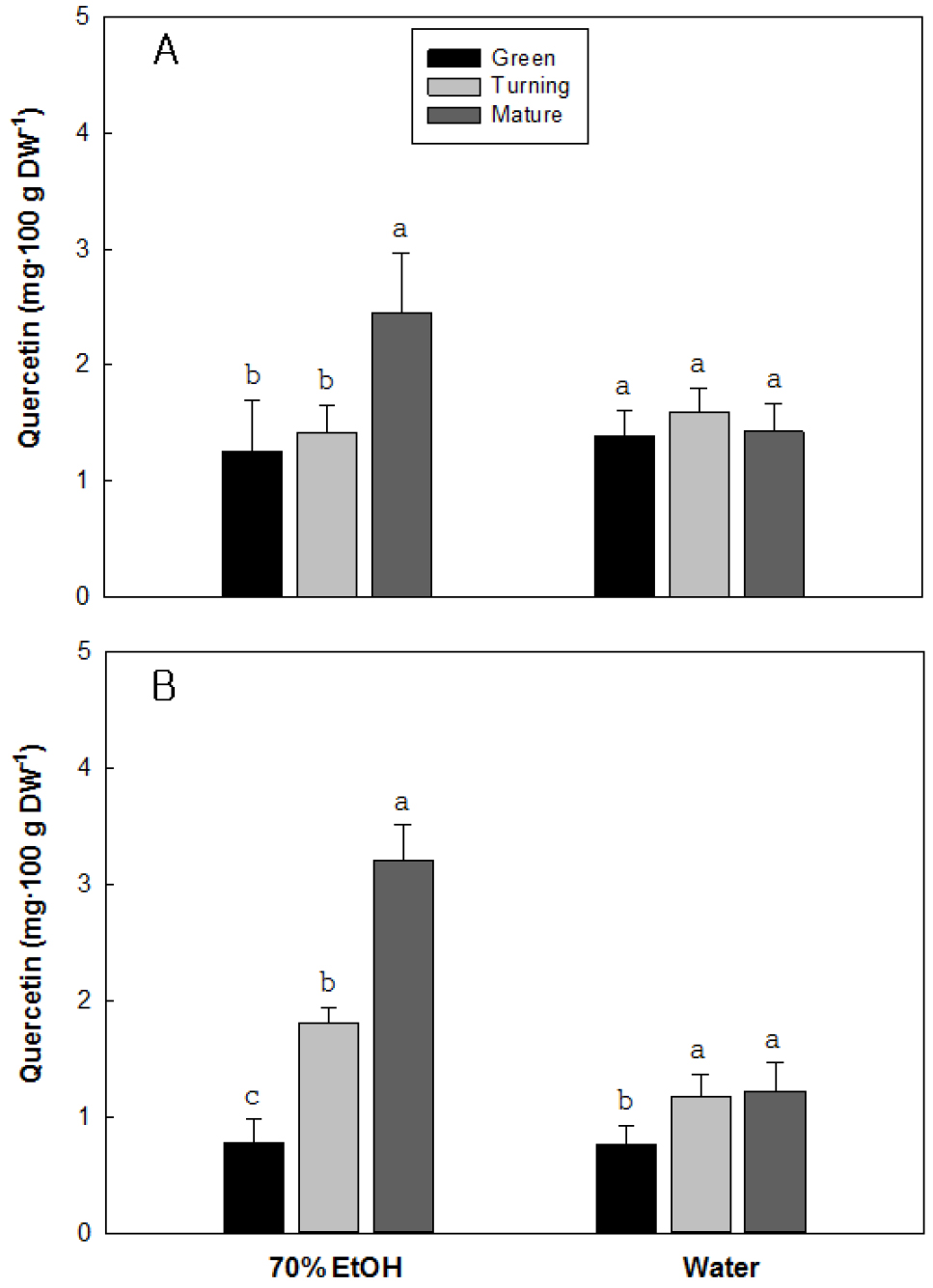
6. 성숙단계에 따른 퀘르세틴 함량 변화
추출용매와 성숙단계에 따른 딸기 과실의 퀘르세틴 함량 변화를 분석한 결과, 추출용매로 에탄올을 사용하면 설향과 만년설 두 품종 모두 성숙이 진전될수록 낮은 함량을 보였지만, 물을 사용하면 두 품종 모두 완숙기에 상대적으로 높은 함량을 보였다(Fig. 7). 설향의 퀘르세틴 함량은 녹숙기에는 70% 에탄올과 물로 추출할 경우에 각각 1.3과 1.4mg이었고, 변색기에는 큰 차이가 없이 1.4와 1.6mg 수준이었다. 그러나 완숙기에는 70% 에탄올을 추출용매로 사용하면 2.5mg으로 급증하였고, 물을 사용하면 변색기와 큰 차이 없이 1.4mg 수준이었다. 만년설의 녹숙기 함량은 70% 에탄올이나 물로 추출하면 0.8에서 0.7mg 수준으로 큰 차이가 없었지만, 변색기와 완숙기에는 물보다는 에탄올로 추출할 경우가 높았다. 물을 추출용매로 사용할 경우, 변색기와 완숙기의 함량이 1.2mg 수준으로 녹숙기에 비해 증가하는 경향을 보였다. 그러나 70% 에탄올로 추출하면 변색기에는 1.8mg으로 녹숙기에 비해 2.3배 증가하였고, 완숙기에는 3.2mg으로 녹숙기 대비 4배 증가하는 경향을 보였다.
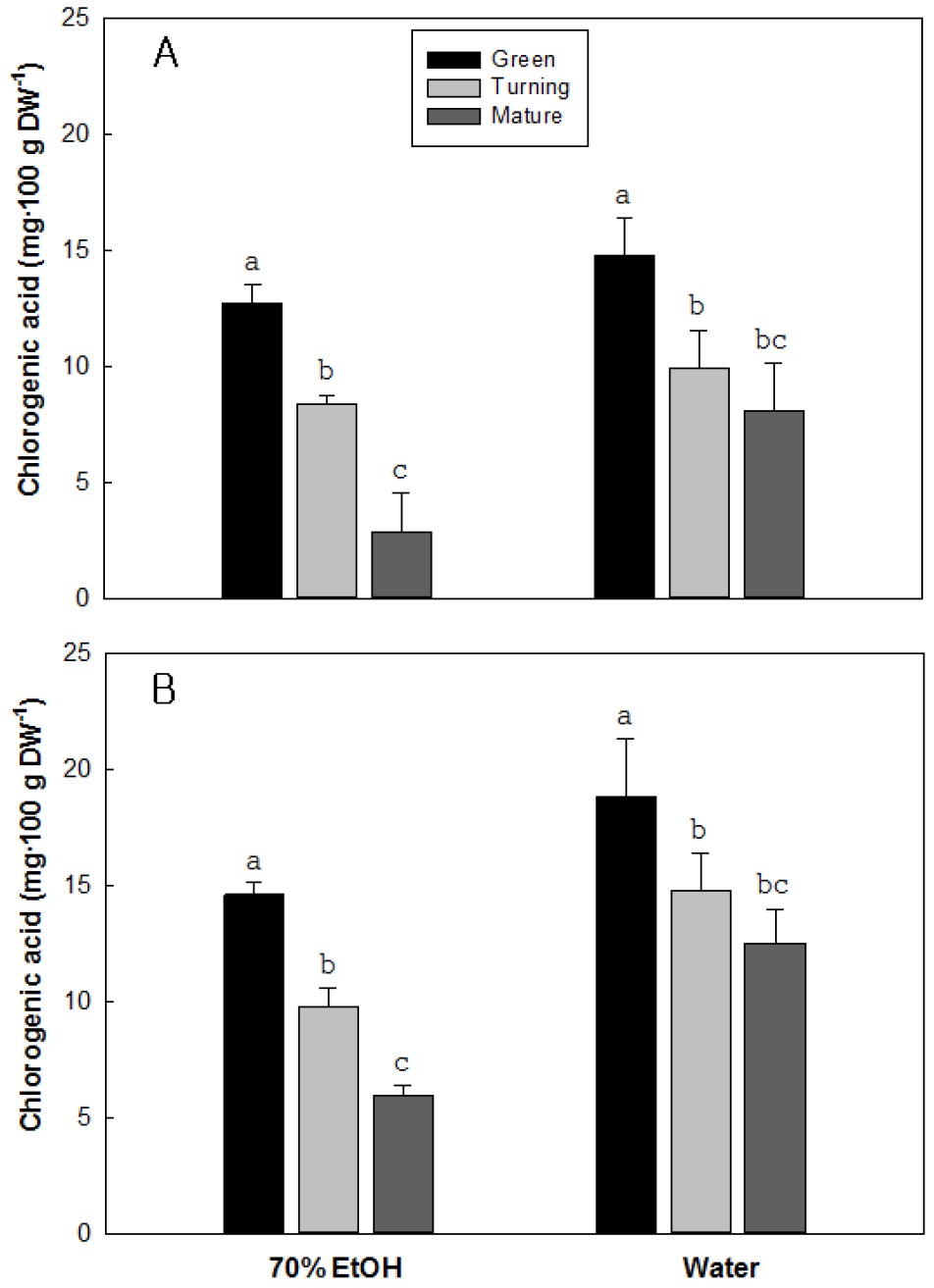
7. 성숙단계에 따른 클로로겐산 함량 변화
딸기 품종별 성숙단계 및 추출 용매에 따른 chlorogenic acid의 함량 변화를 분석한 결과, 모든 품종에서 성숙과정이 진행될수록 감소하였고 70% 에탄올보다는 물이 추출 효과가 높은 경향을 보였다(Fig. 8). 설향의 녹숙기 chlorogenic acid 함량은 70% 에탄올로 추출할 경우에 건물 100g 당 12.7mg으로 녹숙기가 가장 높았으며 성숙이 진행되면서 감소하여 변색기와 완숙기의 함량이 각각 8.4와 2.9mg으로 각각 33.9와 77.2% 수준으로 감소하는 경향을 보였다. 물로 추출할 경우에는 다소 높아 녹숙기에는 14.8mg에서 변색기와 완숙기에는 각각 9.9와 8.1mg 수준으로 다소 감소하는 경향을 보였다. 만년설의 chlorogenic acid 함량도 다른 품종과 유사한 변화 양상을 보였는데, 물로 추출할 경우에 가장 높은 함량을 보인 녹숙기에는 18.9mg인데 비해 변색기와 완숙기의 함량은 각각 14.7과 12.5mg으로 각각 21.6과 33.5% 수준으로 감소하였다.
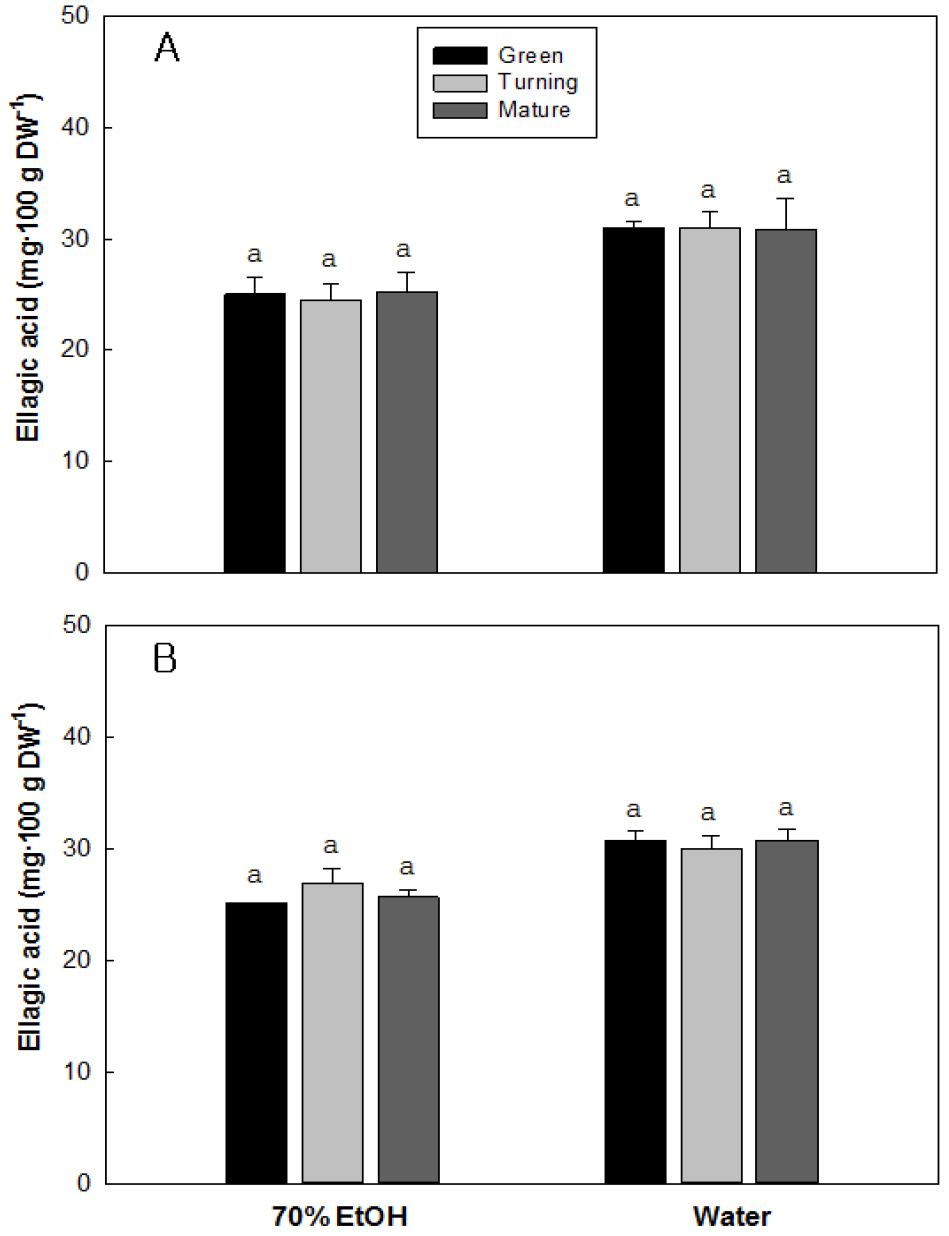
8. 성숙단계에 따른 엘라그산 변화
Fig. 9는 딸기 품종별 성숙단계 및 추출 용매에 따른 엘라그산 함량 변화를 분석한 결과인데, 전반적으로 품종이나 성숙과정에 따른 함량 차이는 크지 않았고 에탄올 추출보다는 추출용매로 물을 사용한 경우에 다소 높은 함량을 보였다. 설향의 엘라그산 함량은 성숙과정에 따른 차이는 없었는데, 에탄올 추출 시에는 건물 100g 당 녹숙기의 25.0mg에서 완숙기의 25.6mg 수준으로 성숙과정에 따른 차이는 없었고 물로 추출할 경우에는 녹숙기의 31.0mg 수준에서 완숙기의 30.8mg 수준으로 70% 에탄올 추출보다는 다소 높은 경향을 보였다. 만년설에서도 성숙과정에 따른 차이는 없었으며 에탄올 추출 시에는 녹숙기의 25.1mg에서 완숙기의 25.6mg 수준이었고, 물로 추출할 경우에는 녹숙기의 30.6mg 에서 완숙기의 30.7mg 수준을 보였다.
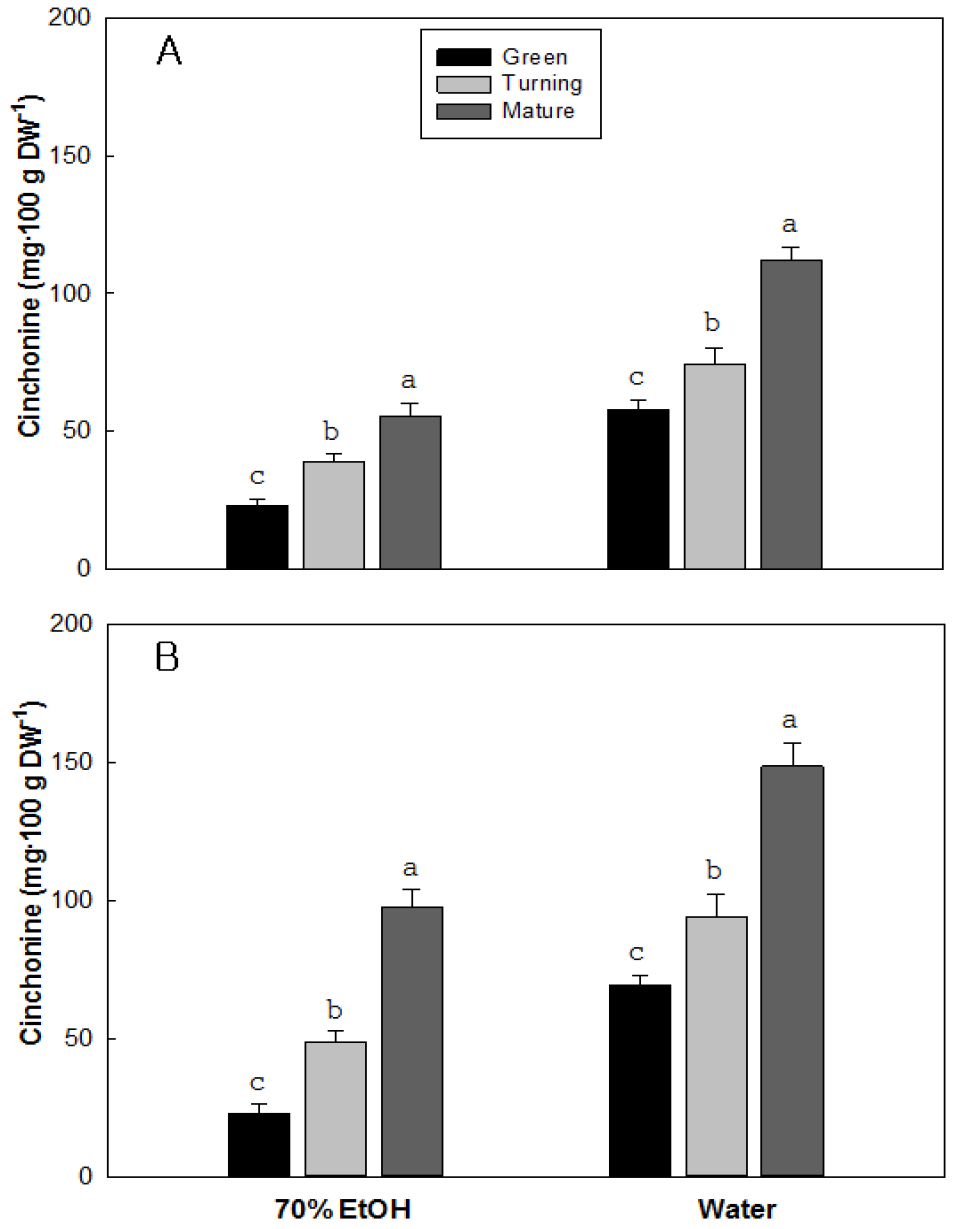
9. 성숙단계에 따른 신코닌 함량 변화
딸기 품종별 성숙단계 및 추출 용매에 따른 신코닌의 함량 변화를 분석한 결과인데, 모든 품종에서 과실이 성숙될수록 증가하는 경향을 보였으며 에탄올보다는 물에 추출할 경우에 높은 함량을 보였다(Fig. 10). 설향의 신코닌 함량 변화는 성숙과 더불어 증가하는 경향을 보였는데, 물을 추출용매로 사용할 경우가 가장 높은 값을 보여 녹숙기의 신코닌 함량이 건물 100g 당 57.9mg에 비해 변색기와 완숙기의 함량은 각각 74.4과 112.1mg으로 각각 1.3과 1.9배 수준으로 증가하였다. 만년설에서도 물을 추출용매로 사용할 경우가 가장 높은 값을 보였는데. 녹숙기의 69.1mg에 비해 변색기와 완숙기에는 각각 94.0과 148.6mg으로 각각 1.4와 2.2배 수준으로 증가하는 경향이었다.
고 찰
붉은색 색소의 안토시아닌 화합물인 칼리스테핀은 pelargonidin 3-O-glucoside chloride라고도 부르는데, CGN(Cerebellar Granule Neurons) apoptosis 모델에서 기능성 산화방지와 염증 경감 효과가 있는 것으로 알려져 있다(Kelsey와 Natalie, 2010; Zhao 등, 2019). 또한 칼리스테핀에 의한 항산화 효과는 미토콘드리아 글루타치온 결핍과 지질의 과산화를 방지하며, OPA-1의 분열을 보호하여 미토콘드리아 구조를 유지함으로서 효과를 나타내는 것으로 알려져 있다(Kelsey와 Natalie, 2010). 칼리스테핀을 포함한 안토시아닌은 각 색소에 따라 77-99%의 높은 유전력을 보이기도 하지만, 파종기나 연차 등 환경요인에 따라 유전력 차이를 보인다고 하였는데(Chu 등, 2003), 완숙기의 과실색이 적색인 설향과 분홍색인 ‘만년설’의 칼리스테핀 함량은 뚜렷한 차이를 보였다(Fig. 2).
딸기 과실의 주된 색소인 안토시아닌은 펠라르고니딘과 시아니딘으로 알려져 있으며 완숙기에 도달하기까지는 계속 안토시아닌 합성은 이루어지는 것으로 알려져 있다(Kalt와 McDonald, 1996; Lopes da Silva 등, 2002). 딸기와 블루베리 등의 베리류 과실은 성숙과정이 진전될수록 안토시아닌 함량이 크게 증가하며(Wang과 Lin, 2000), 완숙된 딸기 과실의 안토시아닌 함량은 재배지역과 품종에 따라 차이가 난다고 하였다(Kim과 Shin, 2015), 시아니딘-3-글루코사이드는 비타민 E보다 노화억제 효과가 뛰어나며 활성산소종을 제거하여 뇌와 신체의 노화를 예방하고 망막 장애 치료를 통하여 시력 개선에도 효과가 있고 종양세포의 성장을 지연하고 폐암 세포의 체내 전이를 줄인다는 보고도 있다(Baek 등, 2023; Edderkaoui 등, 2008). 또한 시아니딘-3-글루코사이드는 불포화지방산인 리놀렌산을 증가시켜 혈중 콜레스테롤과 중성지질의 축적을 억제시킨다고 하였다(Edderkaoui 등, 2008; Kim 등, 2010a). 본 실험의 결과에서는 완숙기의 과실색이 분홍색인 ‘만년설’에 비해 적색인 설향에서 시아니딘-3-글루코사이드의 함량이 높은 경향을 보여 품종에 따른 차이가 난다는 Kim과 Shin (2015)의 결과와 일치하였다(Fig. 3). 따라서 신선딸기의 섭취로 인한 시아니딘-3-글루코사이드의 다양한 건강 기능성 증진효과는 최근 개발되어 소비자에게 관심을 받고 있는 분홍색이나 흰색 딸기에 비해 적색 딸기에서 그 효과가 높을 것으로 판단되었다.
카테킨은 플라보노이드 계열의 물질로 flavan-3-ol 구조를 가지고 있으며 카카오 열매 등에 다량 함유되어 있는데, 카테킨은 3차원 구조의 차이에 따라 (+)-카테킨, (-)-카테킨, (+)-에피카테킨, (-)-에피카테킨으로 구분하기도 한다(Alan 등, 2011). 카테킨의 생리적 활성 중의 하나가 병원균에 대한 저항성인데, 뿌리를 침입하는 병원균에 대한 저항성에 카테킨이 관여하고 있다는 결과는 인삼 등에서 보고되었다(Mahfuzur와 Zamir, 2005). 카테킨은 인삼 뿌리에 빨간 색소의 생성을 유도하는 균에 대한 항균활성을 나타내기도 하고, 잎이 상처를 입으면 에피 카테킨이 증가하여 상처 부위를 통해서 들어오는 병원균에 대한 저항성을 증가시키는 것으로 추정하고 있다(Constabel 등, 2000). 카테킨의 건강 기능성 효과는 발암 억제, 동맥경화 예방, 혈압상승 억제, 혈전 예방, 항바이러스, 항비만, 항당뇨, 해독작용, 소염작용, 충치 예방 등 다양하다(Constabel 등, 2000; Mahfuzur와 Zamir, 2005). 특히 카테킨의 항산화 작용과 자유라디컬 제거능은 비타민 C나 E보다 효과적인 것으로 보고되었다(Grzesik 등, 2018; Sheng 등, 2023). 한편으로 카테킨의 산화에 의한 조직의 갈변현상은 상품성을 저하시키는 요인으로 작용하기도 하는데, 딸기나 포도에서 나타나는 갈변 현상은 (+)-카테킨의 산화에 의한 것이다(Lucille 등, 2007). 본 연구의 결과, 딸기 과실의 카테킨 함량은 전반적으로 완숙기에 비해 녹숙기에 높은 경향을 보였고 완숙기의 과실색이 적색인 설향보다는 분홍색인 만년설에서 높았다(Fig. 4). 딸기 과실의 카테킨 함량은 녹숙기에 비해 성숙과 더불어 급격하게 감소하였지만, 완숙기의 함량은 설향의 18.2mg에 비해 만년설은 47.5mg으로 높은 경향을 보여 카테킨에 의한 항산화력 등 다양한 건강 기능성 효과는 분홍색 딸기가 더 높은 것으로 판단되었다.
카테킨의 입체 이성질체인 에피카테킨은 서로 다른 위치에 있는 6개의 수산기로 구성된 3개의 탄화수소 고리를 가진 폴리페놀 화합물로 식물체에 널리 존재한다(Xu 등, 2004). 에피카테킨은 녹차와 홍차(Arts 등, 2000; Ding 등, 1999), 카카오와 미숙한 콩의 꼬투리(Arts 등, 2000; de Pascual Teresa 등, 2000) 및 딸기와 같은 베리류와 여러 가지 과실에도 많이 함유되어 있다(Prakash 등, 2019). 에피카테킨은 항산화 활성과 세포 신호 전달 및 막 단백질과 상호 작용하는 능력으로 인해 세포의 신호 전달 메커니즘을 조절한다는 결과(Fraga와 Oteiza, 2011)와 더불어 생물학적 이용 가능성에 대한 많은 연구가 이루어졌다(Bigelow와 Cardelli, 2006; Manach와 Donovan, 2004; Monika 등, 2019; Ravindranath 등, 2006). 에피카테킨의 생물학적 활성에 대한 연구결과는 항산화력(Manach와 Donovan, 2004; Monika 등, 2017), 항균작용(Gupta 등, 2011), 심장계 질환 예방(Bailey와 Mukhta, 2013), 당뇨병 예방(Calabriso 등, 2016) 및 항염증(Orlikova 등, 2014) 등 다양한 분야에서 그 기능성이 보고되었다. 딸기의 경우 딸기 생체 100g 당 에피카테킨 함량은 7.5mg으로 대표적인 에피카테킨 함유 식품으로 보고하였는데(Arts 등, 2000), 본 실험의 결과에서는 품종, 성숙시기 및 추출용매에 따른 차이는 있었지만, 전반적으로 에피카테킨의 함량은 딸기에서 높은 것을 알 수 있었다. 딸기의 성숙단계에 따른 에피카테킨의 함량은 완숙기에서 높은 경향을 보였으며 분홍색 딸기인 ‘만년설’에 비해 적색인 설향에서 높은 경향을 보였다(Fig. 5).
생리활성물질은 화학적 구조를 바탕으로 플라보노이드, 페놀 화합물 및 리그난 등으로 분류하는데(Karrie와 Sheri, 2008), 많은 식물에 함유된 다양한 플라보노이드 화합물은 전체 화합물의 50-80%가 배당체의 형태로 존재한다(Jeong, 2005; Lee 등, 2007; Woo 등, 2006). 이러한 페놀 화합물은 항산화 작용, 순환계 질환의 예방, 항염증, 항균 및 항바이러스 효과, 지질의 산화억제 및 면역증강 작용 등 보고된 바 있다(Kawaguchi 등, 1997; Materska 등, 2003; Nile 등, 2021). 퀘르세틴의 배당체인 퀘르세틴-3-글루코사이드에 대한 연구는 양파(Kiviranta 등, 1988), 보리수(Lee, 2012) 및 사과(Nile 등, 2021) 등에서 보고되었는데, 그 기능성은 항산화 효과, 콜라겐 생합성에 의한 노화억제 효과, 항염증 및 면역강화 효과가 검정되었다. 퀘르세틴과 그 배당체를 포함한 플라보노이드 관련 연구는 생합성 기작(Bovy 등, 2007; Graham, 1998), 작물에 따른 함량이나 특성 및 기능성(Iorizzi 등, 2001; Lee 등, 1995; Marin 등, 2004; Materska 등, 2003)뿐만 아니라 배당체 중에서 비당 성분인 아글리콘 탐색(Lee 등, 1995)에 많이 보고되었다. 고추의 경우, 품종뿐만 아니라 성숙단계에 따라 그 함량은 차이가 있는 것으로 보고되었는데(Howard 등, 2000; Sun 등, 2007; Wahyuni 등, 2011), 성숙기의 과피색이 다른 품종간의 차이와 더불어 성숙단계에 따른 퀘르세틴-3-글루코사이드의 함량 차이가 뚜렷하여 고추 등의 결과 유사한 경향을 보였다(Fig. 6). 퀘르세틴은 플라보노이드 화합물의 일종으로서 양파, 베리류의 열매, 어성초, 두충나무 잎, 참당귀 나무의 잎 등에 아글리콘이나 배당체의 형태로 존재한다(Hakkine 등, 1999; Lee 등, 2002; Moon 등, 2002; William 등, 1999).
퀘르세틴은 과산화지질 형성의 억제작용(Cavallin 등, 1978), 항바이러스(Veckenstedt 등, 1978; Veckenstedt와 Pusztai, 1981), 항균효과(Han과 Lee, 1989; Kimura와 Hiromi, 1984) 및 항돌연변이 작용(Edenhader와 Tang,1996)에 영향을 미치는 기능성 물질로 보고되었다. 특히 퀘르세틴은 발암물질의 활성억제, 암세포의 효소작용 저해, 암세포의 성숙 저해 및 항암물질의 활성증대 등 광범위한 항암 관련 기능성을 가진다고 보고되고 있다(Leighton 등, 1992). 또한 퀘르세틴은 천식(Jafarinia 등, 2020), 비염(Sagit 등, 2017) 및 아토피 피부염(Karuppagounder 등, 2015)과 같은 알레르기성 병을 예방하는 효과도 보고되기도 하였다. 설향과 ‘만년설’의 완숙기 과실에서 퀘르세틴의 함량이 많았는데(Fig. 7), 이는 퀘르세틴의 배당체인 퀘르세틴-3-글루코사이드의 함량이 상대적으로 적었던 결과(Fig. 6)를 감안하면 딸기의 완숙기에는 배당체로 저장되기보다는 퀘르세틴으로 존재하는 것으로 판단되었다. 또한 딸기의 과피색이 다른 두 품종에서 생과용으로 이용되는 완숙기의 퀘르세틴 함량은 적색인 설향보다는 분홍색인 만년설 품종에서 높은 경향을 보였는데, 이러한 결과는 퀘르세틴 섭취에 따른 여러 가지 건강 기능성에 대한 효과에 대한 품종간 차이를 설명할 수 있을 것으로 판단되었다.
클로로겐산은 카페산과 퀸산이 에스테르 결합으로 생성된 폴리페놀 화합물질로 식물이 스트레스를 받으면 발생하는 다양한 활성산소종과 반응하여 스트레스에 대한 식물의 저항성을 높여주며 곤충에 대한 방어작용을 하기도 한다(Wang 등, 2022). 또한 클로로겐산은 자외선을 흡수하여 완충시킴으로써 식물의 잎이 받게 되는 각종 스트레스를 감소시키는 것으로 알려져 있다(Cle 등, 2008). 병원균에 감염되었을 경우에 체내 클로로겐산의 함량이 높을수록 병원균에 대한 저항성이 높아지기도 한다는 보고도 있다(Niggeweg 등, 2004). 클로로겐산은 생체 내에서 과산화지질의 생성 억제효과, 콜레스테롤 생합성 억제효과, 항산화 및 항암작용 효과가 있는 것으로 보고되기도 하였다(Wang 등, 2022). 본 실험의 결과 딸기 과실의 클로로겐산 함량은 전반적으로 완숙기에 비해 녹숙기에 높은 경향을 보였는데 품종에 따른 함량 차이를 보였다. 녹숙기의 클로로겐산 함량은 설향보다는 ‘만년설’에서 높은 경향을 보였지만, 완숙기에는 품종간에 큰 차이가 없었다(Fig. 8).
엘라그산은 채소, 과실 및 견과류 등에 많이 함유되어 있는 폴리페놀 화합물로 대표적인 효능은 항산화 및 항암작용으로 잘 알려져 있다(Daniel 등, 1989; Mukhtar 등, 1988; Osawa 등, 1987; Thresiamma와 Kuttan, 1996). 딸기 과실에서는 성숙단계나 과색에 따른 품종간의 엘라그산 함량에는 차이가 없었다(Fig. 9). 엘라그산의 항암 작용은 주로 암세포 증식 억제, 세포사멸 유발 및 세포주기를 조절하는 것으로 보고되었다(Edderkaoui 등, 2008; Larrosa 등, 2006; Pacheco-Palencia 등, 2008; Stoner와 Gupta, 2001). 특히 엘라그산은 암세포의 세포분열주기에서 G1기를 저지해서 세포분열을 중단시키며(Gonzalez-Sarrias 등, 2009; Li 등, 2005), 암세포가 종양을 억제시키는 유전자를 파괴하는 것을 방지한다는 보고도 있다(Mertens-Talcott 등, 2005). 또한 엘라그산은 노화된 피부에서 피부의 엘라스틴화를 유발하는 단백질 분해를 억제함으로써 항섬유화 및 주름개선에 효과적이라는 연구 결과도 있다(Jimenez 등, 2006).
알칼로이드 화합물에 속하는 신코닌은 말라리아 치료제로 사용되고 있는 퀴닌, 퀴니딘, 신코니딘과 같은 퀴닌 관련 화합물에 비해 낮은 독성을 가지며(Genne 등, 1995), 항말라리아 치료 효과(Tracy와 Webster, 1996)뿐만 아니라, 혈소판에서 Ca2+의 유입과 PKC 경로를 억제함으로서 항혈전 작용(Gilani와 Shaheen, 1997; Shah 등, 1997) 및 항비만에 효과가 있는 물질로 알려져 있다(Jung 등, 2012). 다양한 기능성을 가진 신코닌은 딸기 과실의 성숙과 더불어 증가하는 경향을 보였으며 적색보다는 분홍색 딸기 과실에서 다소 높은 경향을 보였다(Fig. 10).