서 론
재료 및 방법
1. 재배환경 및 실험처리
2. 생육조사
3. MDA 및 H2O2 분석
4. 통계분석
결과 및 고찰
1. 생육 특성
2. 근권부 형태 특성
3. MDA 및 H2O2 반응
서 론
식물은 외부 환경의 자극에 적응하며 생장하게 된다. 특히 물리적인 접촉에 대한 자극인 기계적 자극(Mechanical stimulation)은 식물의 형태와 호르몬 변화 같은 반응을 유도하게 된다(Jaffe, 1973). 특히 반복적인 쓸어주기(brushing, 브러싱)처리를 통한 생장점 주변의 자극은 오이와 토마토 묘의 신장을 억제할 수 있는 것으로 보고되었다(Kim 등, 2018). 이러한 반응을 접촉형태형성(Thigmomorphogenesis)으로 정의되어 연구가 진행된 바 있다(Börnke와 Rocksch, 2018; Mitchell, 1996).
한편, 염 스트레스는 수분 포텐셜 저하, 산화적 손상 등을 유발하는 스트레스 요인이다(Bernstein, 1975). 고농도의 염분에 노출된 식물은 삼투 스트레스와 이온 독성, 그리고 활성산소종(ROS) 축적에 따른 산화 스트레스로 인해 생장 지연, 엽록소 함량 감소, 광합성 저해 등 복합적인 생리적 이상으로 이어진다(Athar 등, 2022; Zhao 등, 2021). 식물은 염 스트레스 하에 적응하기 위해 이온항상성 유지, 삼투 조절 물질 합성, 항산화 효소 활성화 등 다양한 메커니즘을 이용한다(Zhu 등, 2007).
기계적 자극에 노출된 식물의 반응은 형태의 변화뿐만 아니라 환경 스트레스에 대한 내성증진을 유도하는 priming 효과를 가져올 수 있다(Ghosh 등, 2021). Chehab 등(2012)은 기계적 자극을 받은 애기장대 식물에서 해충에 대한 저항성이 증가하였음을 보고한 바 있으며, 바람 자극을 받은 콩에서 진딧물에 대한 내성이 증가하였다는 연구도 진행된 바 있다(Cipollini, 1997). 또한 소리로 인한 진동 처리에 노출된 애기장대가 가뭄 스트레스에 대한 생존률이 유의미하게 증가하였다(López-Ribera와 Vicient, 2017). 이처럼 기계적 자극을 통한 식물의 저항성 증진과 내성 변화에 대한 생리적 반응에 대한 관심은 증가되고 있다.
하지만 기계적 자극의 종류와 환경 스트레스의 종류에 따라 식물의 반응은 다양하게 나타난다. 또한 기계적 자극의 특성 상 종류와 강도가 매우 다양하고 복잡하여, 이를 정량적으로 측정하거나 표준화하는 방법이 아직 확립되지 않았다. 이로 인해 적절한 자극 강도와 빈도를 결정하는 것이 어렵고, 과도한 자극 시 오히려 스트레스 반응이 과도하게 유발되어 생육 저해가 발생할 위험도 있다. 따라서 환경 스트레스 내성 증진을 위한 효과적인 기계적 자극 처리 방법을 개발하기 위해서는, 자극 강도에 따른 식물의 생리적 반응과 내성 메커니즘을 체계적으로 규명하고 이를 정량화하는 연구가 반드시 필요하다.
따라서 본 연구는 오이묘를 브러싱(brushing) 처리 후 다양한 농도의 NaCl을 처리하여 기계적 자극 이후의 식물체가 염 스트레스에 노출되었을 때의 영향을 평가하고자 수행되었다. 이를 통해 브러싱 처리가 염 스트레스 내성 증진에 미치는 영향을 규명하고, 향후 기계적 자극을 활용한 내성 증진 연구의 기초 자료를 제공하는 것을 목적으로 한다.
재료 및 방법
1. 재배환경 및 실험처리
2021년 10월 4일 오이(Cucumis sativus L. ‘Joeunbakdadagi’, Farmhannong Co. Ltd., Korea) 종자를 상업적 공정육묘용 상토(Tosilee, Shinan Grow Co. Ltd., Jinju, Korea)가 충진된 40구 트레이(54×27.5×5cm, Bumnong Co., Ltd., Jeongeup, Korea)에 1구당 1립씩 파종하였다. 파종 후 20일 뒤 본엽이 전개된 오이묘를 개별포트로 이식하여 재배하였다. 기계적 자극 처리(이하 브러싱처리)는 2021년 11월 1일부터 연질 아크릴(acrylic, 두께 1mm, 단위면적당 중량 1.13kg·m-2)이 부착된 자동 이송장치(240×120×80cm)를 이용하여 브러싱 처리를 진행하였으며, 브러싱 처리의 강도는 이전의 연구에서 오이 및 토마토의 생육 억제효과가 보고된 결과를 기준으로 수행되었으며(Jeong 등, 2020; Kim 등, 2018), 식물체 상단부를 스치는 수준의 자극을 초당 0.2m의 속도로 2시간 간격(1일 12회)으로 2021년 11월 8일까지 7일간 처리를 하였다. 기계적 자극 처리 후 환경 스트레스에 대한 내성 증진 효과를 확인하기 위해 브러싱 처리 7일 후 인 2021년 11월 8일에 NaCl을 50, 100, 150, 200mM 농도로 제조하여 식물체당 100mL씩 1회 관주하였다. 이후 2021년 11월 16일 생육조사를 진행하였다. 실험은 경상국립대학교 부속농장 벤로형 유리온실에서 자연광 조건에서 진행되었다. 실험기간 동안 양수분 공급은 온실 다용도 액비를 조제하여 pH 6.5와 EC 1.5dS·m-1로 조정한 양액을 2일 간격으로 1회 저면관수하였다(Table 1).
Table 1.
Composition of the nutrient solution used in the experiment.
2. 생육조사
각 처리별 12개체를 무작위로 선발하여 초장, 경경, 엽장, 엽폭, 엽수, SPAD 값, 엽면적, 지상부와 지하부의 생체중 및 건물중을 측정하였다. 초장은 식물체의 지제부에서 생장점까지의 길이를 측정하였고, 경경은 버니어캘리퍼스(CD-20CPX, Mitutoyo Co. Ltd., Kawasaki, Japan)를 이용하여 지제부 상단 1cm를 측정하였다. 엽장과 엽폭은 생장점 기준 두 번째 잎을 측정하였다. SPAD는 엽록소 측정기(SPAD 502, Konica Minolta Inc., Tokyo, Japan)를 이용하여 측정하였고, 엽면적은 줄기를 제외한 잎의 면적을 엽면적 측정기(LI-3000, LI- COR Inc., Lincoln, NE, USA)를 이용하여 측정하였다. 지상부와 지하부의 생체중 및 건물중은 전자저울(EW220-3NM, Kern&Sohn GmbH., Balingen, Germany)을 이용하여 측정하였다. 건물중은 시료를 70°C 항온 건조기(Venticell-222, MMM Medcenter Einrichtungen GmbH., Planegg, Germany)에서 72시간 이상 건조한 후 측정하였다. 각 처리에 따른 오이묘의 지하부 발달 정도를 확인하기 위해, 묘의 지하부를 채취하여 스캐너(Expression 12000XL professional scanner, Epson America Inc., Los Alamitos, CA, USA)로 취득한 이미지데이터를 WinRhizo Pro 2020 뿌리 형태 분석 시스템(Regent Instruments Inc., Sainte-Foy, QC, Canada)을 이용하여 처리별 총 근장, 뿌리 표면적, 평균 근경, 뿌리 부피 그리고 근단 수를 측정하였다.
3. MDA 및 H2O2 분석
Malondiadehyde(MDA)의 측정을 위해 잎 생체중 1.5g을 0.1%의 trichloroacetic acid(TCA) 용매에 균질화한 후, 4℃에서 15분간 12,000×g에서 원심분리(5810R, Eppendorf, Hamburg, Germany)하였다. 상층액 1mL에 0.6% thiobarbituric acid(TBA) 용매를 1mL 첨가한 뒤 30분 동안 95℃ 항온수조에 가열하였다. 추출 용매를 다시 4℃에서 10분간 12,000×g에서 원심분리 한 후 분광광도계로 450, 532, 600nm의 파장에서 흡광도를 측정하여 다음과 같이 계산하였다(Lee 등, 2011).
MDA (nmol·L-1) = 6.45 × (A532 - A600) - 0.56 × A450
H2O2 의 측정을 위해 잎의 생체중 0.1g을 TCA 용매에 균질화 한 후 4℃에서 30분간 12,000×g에서 원심분리하였다. 상층액 0.5mL에 10mM photassium phosphate buffer (pH 7.0) 0.5mL과 1.0mM potassium iodide 0.5mL을 첨가한 뒤 390nm 파장에서 흡광도를 측정하였다. 측정 이후 표준곡선을 이용하여 정량화하였다.
4. 통계분석
통계분석은 SAS 프로그램(SAS 9.4, SAS Institute Inc, Cary, NC, USA)을 이용하여 분산분석(ANOVA)을 실시하였고, 평균 간 비교는 던컨의 다중검정(Duncan’s multiple range test)을 이용하여 5% 유의수준에서 각 처리 간 유의성을 검증하였다. 그래프는 SigmaPlot 프로그램(SigmaPlot 14.5, Systat Software, San Jose, CA, USA)을 이용하여 나타내었다.
결과 및 고찰
1. 생육 특성
브러싱처리와 염 스트레스 처리는 오이 묘의 생육에 뚜렷한 영향을 미쳤으며, 특히 초장과 엽면적은 두 처리를 함께하였을 때 더욱 효과적이었다(Table 2와 Fig. 1). NaCl을 처리하지 않은 무처리구(Non-treatment + 0mM)에서는 초장과 엽면적이 각 21.0cm와 208.04cm2으로 나타났으며, 이는 NaCl 무처리와 브러싱 처리구(Brushing + 0mM)의 초장(20.4cm) 및 엽면적(201.02cm2)과 유의적인 차이를 보이지 않았다. 하지만 NaCl 처리와 브러싱 처리가 함께 진행되었을 때 초장과 엽면적이 유의적으로 크게 감소하는 것을 확인할 수 있었다. 특히 브러싱 처리와 함께 NaCl의 농도가 가장 높았을 때(Brushing + 200mM) 초장과 엽면적이 각 15.3cm와 127.49cm2로 크게 감소하는 것을 확인할 수 있었다. 한편 SPAD 값은 엽면적과 반대의 경향을 보였으며 엽면적이 가장 컸던 무처리(Non- treatment + 0mM)에서 30.8로 가장 작았으며, 반대로 엽면적이 작았던 브러싱 처리와 고농도 NaCl 처리에서 상대적으로 높게 나타났다.
Table 2.
Growth characteristics of cucumber seedlings exposed brushing and NaCl stress (n = 12).
|
Mechanical stimulation (A) |
NaCl concentration (mM) (B) |
Plant height (cm) | Leaf length (cm) |
Leaf width (cm) | SPAD | Leaf area (cm2/plant) | Fresh weight (g/plant) | Dry weight (g/plant) | |||
| Shoot | Root | Shoot | Leaf | Root | |||||||
| Non- treatment | 0 | 21.0 az | 8.8 a | 10.6 a | 30.8 c | 208.04 a | 8.70 bc | 1.92 ab | 0.27 b | 0.51 ab | 0.065 bc |
| 50 | 19.2 a-c | 7.8 cd | 9.7 bc | 31.1 c | 178.24 bc | 8.26 cd | 1.54 e | 0.27 b | 0.51 ab | 0.052 de | |
| 100 | 18.6 bc | 8.0 bc | 9.6 bc | 32.2 bc | 165.10 cd | 8.16 cd | 1.60 de | 0.27 b | 0.47 bc | 0.057 c-e | |
| 150 | 19.6 ab | 8.6 a | 10.2 ab | 32.5 bc | 192.42 ab | 9.34 ab | 1.79 b-d | 0.29 ab | 0.46 cd | 0.061 b-d | |
| 200 | 17.3 cd | 7.9 b-d | 9.5 b-d | 35.4 a | 139.74 ef | 7.10 e | 1.27 f | 0.26 b | 0.38 e | 0.048 e | |
| Brushing | 0 | 20.4 ab | 8.4 ab | 10.1 ab | 33.1 b | 201.02 a | 9.46 a | 2.07 a | 0.32 a | 0.55 a | 0.096 a |
| 50 | 18.2 bc | 7.9 b-d | 9.1 cd | 33.3 b | 161.51 cd | 8.06 cd | 1.84 bc | 0.27 b | 0.42 de | 0.070 b | |
| 100 | 15.5 d | 7.6 cd | 8.9 d | 35.9 a | 156.34 de | 7.82 d | 1.76 b-e | 0.27 b | 0.43 c-e | 0.067 bc | |
| 150 | 16.0 d | 7.4 d | 9.1 cd | 36.8 a | 136.88 f | 7.54 de | 1.68 c-e | 0.27 b | 0.42 de | 0.066 bc | |
| 200 | 15.3 d | 7.7 cd | 9.1 cd | 35.5 a | 127.49 f | 7.05 e | 1.65 c-e | 0.29 ab | 0.39 e | 0.062 bc | |
| F-test | A | *** | *** | *** | *** | *** | * | *** | ns | * | *** |
| B | *** | *** | *** | *** | *** | *** | *** | ns | *** | *** | |
| A × B | ns | ** | ns | * | *** | *** | * | ns | ** | * | |
기계적 자극에 의한 식물의 지상부 생육 억제는 접촉형태형성(Thigmomorphogenesis)반응으로 알려져 있으며, 다양한 식물에서 기계적 자극에 의해서 반응이 나타나는 것으로 알려져 있다(Jaffe, 1973). 기계적 자극에 의한 식물의 반응은 줄기 신장의 감소, 경경의 증가 등 생장을 조절하는 방법으로 사용될 수 있으며(Börnke와 Rocksch, 2018), 최근 기계적 자극이 에틸렌, 자스몬산의 발현 등 다양한 생리적 경로를 통해 장기적 자극으로 생장 억제를 유도함이 밝혀지고 있다(Brenya 등, 2022). 엽장과 엽폭은 브러싱 처리에 상관없이 NaCl 처리에 의해 생육이 감소하는 경향을 보였다. SPAD값의 변화는 엽면적이 작을수록 증가하였으며, 단위면적당 엽록소 밀도가 높아지면서 SPAD 값이 상대적으로 증가한 것으로 보인다. 이는 식물이 엽면적 감소 상황에서도 광합성 기능을 유지하려는 보상기작으로 볼 수 있다. 지상부의 생체중과 건물중은 브러싱 처리의 여부에 상관 없이 NaCl의 농도가 증가함에 따라 감소하였지만, 지하부의 생체중과 건물중은 브러싱 처리에서 상대적으로 증가하는 경향을 보였다. 이는 기계적 자극을 받은 식물체의 지하부 생육이 증가하였다는 이전의 연구와 유사 하며(Eshel 등, 2005; Goodman과 Ennos, 1996; Nam 등, 2020; Sarmast 등, 2014), 브러싱 처리로 인해 지상부 생장이 적재 되면서 생육에 필요한 자원의 분배가 지하부로 우선 되었을 것으로 보여진다.
2. 근권부 형태 특성
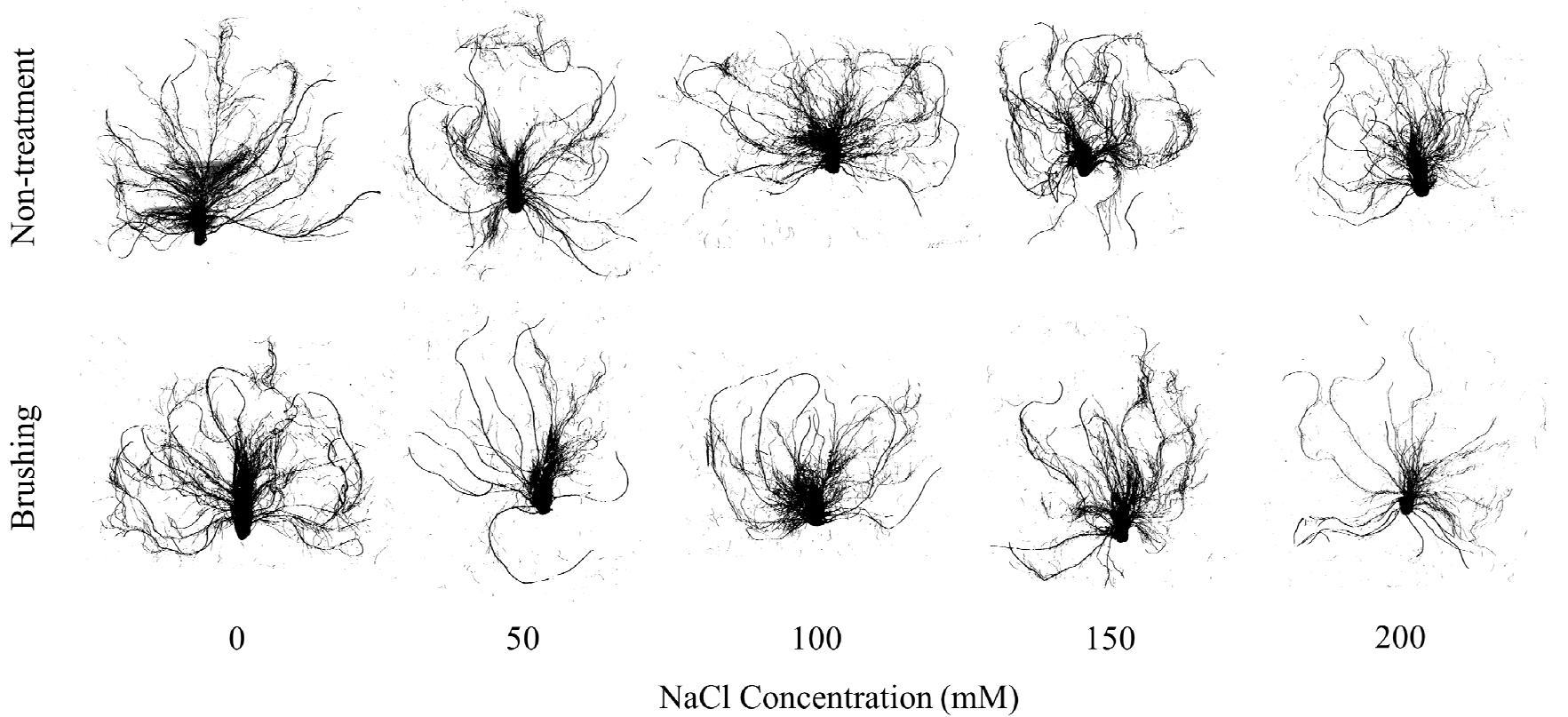
염 스트레스는 오이묘의 뿌리 발달에도 직접적인 영향을 미쳤다(Table 3과 Fig. 2). 브러싱 처리를 하지 않았을 때, NaCl 농도가 증가함에 따라 총 근장, 뿌리 표면적, 뿌리 부피는 전반적으로 감소하였으며, 고농도 NaCl 조건(200mM)에서는 특히 뚜렷한 억제 현상이 나타났다. 평균 근경은 NaCl 처리를 하지 않은 브러싱 처리구(Brushing + 0mM)에서 가장 높았으며, 근단 수 는 브러싱 처리구에서 감소한 것으로 나타났다. 지하부의 특성 중 특히 총 근장의 감소 폭이 컸으며 무처리(Non-treatment + 0mM) 시 901.4cm에서 NaCl 200mM 처리 시 519.5cm로 약 42% 감소하였다.
Table 3.
Root morphological characteristics of cucumber seedlings exposed brushing and NaCl stress (n = 12).
|
Mechanical stimulation (A) |
NaCl Concentration (mM) (B) |
Total root length (cm) |
Root surface (cm2) |
Root average diamter (mm) |
Root volume (cm3) | Root tips |
| Non-treatment | 0 | 901.4 abz | 149.2 ab | 0.513 c | 1.92 bc | 3199.7 a |
| 50 | 745.6 bc | 135.8 bc | 0.519 bc | 1.56 cd | 2838.2 ab | |
| 100 | 733.1 bc | 129.2 bc | 0.559 a-c | 1.91 bc | 2708.5 ab | |
| 150 | 630.9 cd | 111.7 cd | 0.566 a-c | 1.55 c | 2521.7 b | |
| 200 | 519.5 d | 87.8 d | 0.548 a-c | 1.21 d | 1715.5 c | |
| Brushing | 0 | 932.8 a | 174.0 a | 0.618 a | 2.10 a | 2307.3 b |
| 50 | 744.8 bc | 120.2 c | 0.584 a-c | 1.98 bc | 2276.7 b | |
| 100 | 748.9 bc | 133.8 bc | 0.573 a-c | 1.82 bc | 2429.3 b | |
| 150 | 796.1 a-c | 150.0 ab | 0.603 ab | 2.30 ab | 1620.5 c | |
| 200 | 762.6 bc | 128.5 bc | 0.544 a-c | 1.74 cd | 2536.5 b | |
| F-test | A | ns | ns | ns | ns | ** |
| B | *** | *** | ns | *** | ** | |
| A × B | ** | *** | * | *** | *** |
고농도 NaCl처리에서 지하부의 생육지표가 감소한 것은 고염도 환경에서의 수분 스트레스와 이온 독성이 뿌리 생장 세포의 확장을 제한하고, 물질 흡수 기능을 저해하기 때문으로 해석된다(Du 등, 2010; Karimi 등, 2022). 그러나 브러싱 처리된 모종에서는 염 스트레스가 증가하는 조건에서도 총 근장, 뿌리 표면적, 뿌리 부피 등의 지하부 생장 지표가 상대적으로 안정적으로 유지되었으며, 이는 물리적 자극이 염류에 의한 생장 저해를 완화한 것으로 보여 진다. 특히 브러싱 처리구는 고농도 NaCl 처리에서도 총 근장의 발달이 저해되지 않고 100mM 농도의 NaCl 처리와 유사한 수준의 생육을 보였다. 이는 기계 자극이 뿌리 생장 관련 호르몬 조절 또는 세포 분열 활성을 간접적으로 자극했을 가능성을 보여준다. Ghosh 등(2021)은 기계적 자극이 식물의 기초 방어 시스템뿐만 아니라 근권 내 환경 감지 및 조절 메커니즘까지 활성화한다고 보고한 바 있다. 이전의 연구에서 Jeong 등(2023)은 브러싱 처리를 한 토마토 묘가 무처리구와 비교하여 총 근장과 뿌리 표면적이 각 9%, 8% 증가하였다고 보고한 바 있다. 따라서 본 연구에서는 브러싱 처리가 염 스트레스로 인한 지하부 생육 감소를 막을 수 있는 가능성을 가지며 추가적인 연구가 필요할 것으로 보인다.
3. MDA 및 H2O2 반응
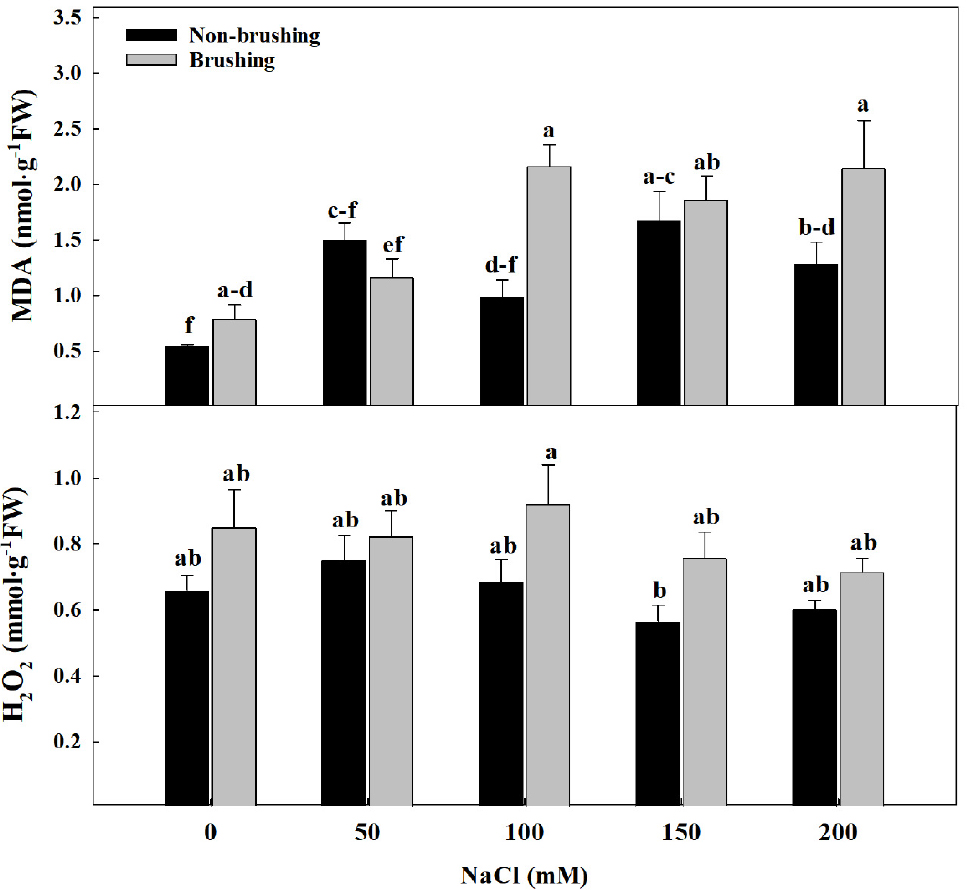
MDA와 H2O2는 염 스트레스와 브러싱 처리에 따라 유의적으로 증가하였다(Fig. 3). MDA와 H2O2 모두 브러싱 처리에서 높게 나타나는 경향을 보였으며 MDA는 NaCl 농도가 증가할수록 높은 축적을 보였으며, H2O2는 NaCl 처리에 상관 없이 브러싱 처리에서 유의적으로 높게 나타났다. 기계적 자극은 식물체에 물리적 충격을 가하기 때문에 적절한 강도의 처리를 하는 것이 중요하다. 특히 과한 물리적 자극의 처리는 식물체에 지속적인 스트레스가 될 수 있다. 따라서 기계적 자극의 스트레스 강도에 따라 식물체는 다른 반응을 보일 수 있어서 환경 스트레스 내성을 가질 수 있는 강도의 스트레스를 확인하는 것이 중요할 것으로 보인다. Benikhlef 등(2013)은 기계적 자극이 산화적 스트레스와 항산화 효소 활성에 영향을 준다고 보고하였다. H2O2는 활성산소종(reactive oxygen species, ROS)인 동시에 신호전달 물질로 작용하며(Hung 등, 2005), 적당한 수준의 자극은 항산화 시스템 활성화와 이온항상성 조절에 영향을 줄 수 있다. 따라서 브러싱 처리에 의해 H2O2 함량이 증가하였고 이로 인해 방어체계가 유도되었을 것으로 보여진다. 브러싱 자극은 요이묘의 산화적 스트레스를 유발하였으며, 이는 H2O2및 MDA의 증가로 확인되었다. 그러나 동시에 염 스트레스 하에서 뿌리 생육을 유지시키는 효과가 나타났다. 이는 기계적 자극이 식물의 스트레스 방어 시스템을 사전 활성화하거나, 자원을 뿌리 쪽으로 재분배한 결과일 수 있다. 이처럼 기계 자극이 이중적인 생리 반응을 유도할 수 있음을 보여주며, 이는 향후 기계적 자극을 통한 저항성 유도 전략이 재배 기술로 적용될 수 있는 가능성을 제시한다.
본 연구는 오이묘에 브러싱 처리와 NaCl 처리를 통한 염 스트레스를 처리하여 복합적인 스트레스 반응을 확인하고자 수행되었다. 두 스트레스를 처리하였을 때 초장과 엽면적은 더욱 감소하는 것을 확인하였으며, 지하부의 생육은 브러싱 처리에서 염 스트레스에도 생육의 감소가 적게 나타나는 것을 확인하였다. 또한, 브러싱 자극은 오이 묘에 일정 수준의 산화 스트레스를 유도함과 동시에, 염 스트레스 환경에서도 뿌리 생장을 유지시키는 긍정적인 반응을 유도하였다. 이러한 결과는 기계적 자극이 스트레스 방어 체계를 사전 활성화하는 priming 효과 또는 생존을 위한 자원 재분배 전략을 유도했을 가능성을 시사한다. 이는 기계적 자극을 활용하여 식물의 스트레스 저항성을 효과적으로 유도할 수 있는 가능성을 보여주며, 향후 스트레스 저항성 증진을 위한 기계적 자극의 적용 방법(강도 또는 처리 기간) 대한 추가적인 연구가 필요할 것으로 판단된다.