서 론
재료 및 방법
1. 식물재료 및 재배관리
2. 플라즈마 발생 장치 및 플라즈마 활성수 분석
3. 생육조사 및 성분 분석
4. 통계 분석
결과 및 고찰
1. 플라즈마 활성수 분석
2. 생육분석
3. 바이오 활성 물질 분석
서 론
국화과(Asteraceae)에 속하는 1년생 초본 식물인 상추(Lactuca sativa L.)는 건강한 식재료로 인식되어 소비량이 많은 작물이다(Dupont 등, 2000). 상추의 지상부는 샐러드, 쌈 채소로 많이 소비되며 비타민 C와 폴리페놀(polyphenol) 같은 항산화 물질과 섬유소 함량이 높다(Nicolle 등, 2004; Serafini 등, 2002). 바이오 활성 물질 중 flavonoid 계열의 quercetin 성분은 상추에서 1.01~1.04mg·g-1의 함량을 보이며. 간의 지질 대사에 영향을 주어 혈청 내 지질 수치를 감소 시키고(Hoek-van den Hil 등, 2013), 고지방 식습관으로 인한 체중의 증가와 지방간 축적의 감소에도 영향을 준다고 보고 되었다(Hoek-van den Hil 등, 2014). 다른 바이오 활성 물질 중 하나인 chlorogenic acid는 상추에서 0.19~0.20mg·g-1의 함량을 보이며, 지방의 축적을 억제하는 효과를 가지고 있으며 혈압 조절에도 좋은 영향을 미친다고 알려져 있다(Blum 등, 2007; Shimoda 등, 2006). 또한, benzoic acid는 상추에 0.30~ 0.32mg·g-1 함유되어 있으며, 편두통, 피부질환, 호흡기질환, 발열 등 다양한 병 치료에 활용되고 있다(Nadkarni, 1989).
플라즈마는 고압, 대기 및 저압 조건에서 발생할 수 있는 이온화된 기체이다(Fröhling 등, 2012). 직류 초고주파 전자빔 등의 전기적 방법을 통해 생성되는 플라즈마는 저온 플라즈마(non-thermal plasma)를 이용한 환경 오염물의 정화, 자동차 배기가스 처리 등의 환경 분야부터(Moreau 등, 2008; Mok 등, 2004), 의료기기 살균 세척, 상처 치유, 치아미백 등의 의학 분야까지 다양하게 활용된다(Bekeschus 등, 2016; Hayashi 등, 2011; Kim 등, 2014). 유전체 장벽방전(DBD, dielectric barrier discharge), 코로나방전(corona discharge)등의 대기압 플라즈마 방식은 OH 라디칼, 오존(O3), 과산화수소(H2O2) 등의 활성산소종(reactive oxygen species)을 생성한다(Deng 등, 2006; Eliasson 등, 1994; You 등, 2020). 활성산소종 중 과산화수소는 다양한 생물적, 비생물적 스트레스를 포함한 환경 조건에서 식물 세포벽 강화(Ngo Thi 등, 2014), 파이토알렉신(phytoalexin) 생산(Dempsey 등, 1995), 광합성(Dat 등, 2000), 광호흡(Noctor와 Foyer, 1998) 그리고 생장(Foreman 등, 2003)에 이르기까지 식물에 중요한 역할을 한다. 과다하게 발생 된 과산화수소는 작물에 산화 스트레스 발생 요인이 되고(Baek 등, 2010), 스트레스는 식물체 방어 물질인 이차대사산물의 발생량을 증가시킨다(Dixon과 Paiva, 1995). 최근에는 과산화수소 침지 처리를 통해 항산화 능력을 증가시키고 내한성 유전자의 발현을 촉진함으로써 유채 씨앗의 저온에서 발아 능력을 향상하는 연구가 진행되었고(Zhang 등, 2017), 완두콩에 과산화수소를 처리할 경우 물리 해부학적 반응과 생산성 및 품질을 증진 시키는 연구에서도 식물 생장, 광합성 색소 등이 증가하는 결과를 보였다(Farouk 등, 2018). Lau와 Mattson(2021)이 수행한 수경재배에서 과산화수소의 농도가 상추 크기에 미치는 영향을 알아보기 위한 연구에서는 생체중, 엽장, 엽폭, 근장 등 모든 부분의 수치가 증가하였다.
본 연구에서는 플라즈마 활성수 처리 시 과산화수소 희석수와 비교해 상추의 생육 및 이차대사산물 함량에 미치는 영향에 대해 살펴보았다. 더 나아가 지금까지는 플라즈마 활성수 안에서 발생되는 과산화수소에 대한 연구가 진행되었고, 실제 과산화수소 수용액과의 비교 관련 연구가 없었기 때문에 플라즈마 활성수와 과산화수소 수용액을 이용한 침지 처리를 했을 때 변화하는 상추의 생육 및 이차대사산물을 비교하기 위해 수행되었다.
재료 및 방법
1. 식물재료 및 재배관리
실험에는 적축면 상추(Lactuca sativa L.) 종자(Seonpung Plus+, Kwonnong Co. Ltd., Cheongju, Korea)를 사용하였으며, 종자를 암면배지로 만들어진 240공(Kiemplug standard tray, Grodan, Denmark) 파종판에 22 ± 2℃에 48시간 동안 암 처리 후 광 강도 230 ± 10μmol·m-2·s-1, 습도 70-75%, 광주기 16h/8h(명기/암기)의 조건에서 3주간 육묘하였으며 저면관수 방법으로 격일 관수하였다. NO3-N 14me·L-1, NH4-N 1me·L-1, PO4-P 3me·L-1, K 6me·L-1, Ca 8me·L-1, Mg 4me·L-1, SO4-S 4me·L-1로 조제된 Hoagland 양액을 사용하여 본엽이 발생한 시점부터 급액하였다. 파종 후 3주째 본엽이 3-4매 전개되었고 이후 균일한 묘를 선정하여 semi-DFT(Gafatec Co. Ltd., Jincheon, Korea) 재배 장치 6개에 14주씩 총 84주를 정식하여 완전제어형 식물공장에 설치된 선반에 옮겨 온도 23 ± 1℃, 습도 70%, 광주기 16h/8h(명기/암기), 광 강도 250 ± 10μmol·m-2·s-1 조건으로 설정하여 재배하였다. 정식 후 양액의 농도는 EC 1.3 ± 0.2dS·m-1, pH 6.5 ± 0.3으로 유지하였다.
정식 2주 후 정식 거리로 인한 뿌리의 지상부 생육의 발달 정도 및 양분 경합 방지를 막기 위해 솎아주기 작업을 시행하였고, 양액의 pH 및 EC 변화를 고려하여 1주일 간격으로 교체해주었다. 총 3주간 semi-DFT 시스템에서 상추를 재배하였으며, 수확하기 24시간 전 각 처리구들을 각각 4L의 양액, 플라즈마 활성수, 그리고 플라즈마 발생 시간에 따른 수중 H2O2 농도를 고려하여 과산화수소 0, 3, 6%로 침지 처리를 진행하였다. 이후 수확하여 생육 조사 및 바이오 활성 물질 분석을 시행하였다.
2. 플라즈마 발생 장치 및 플라즈마 활성수 분석
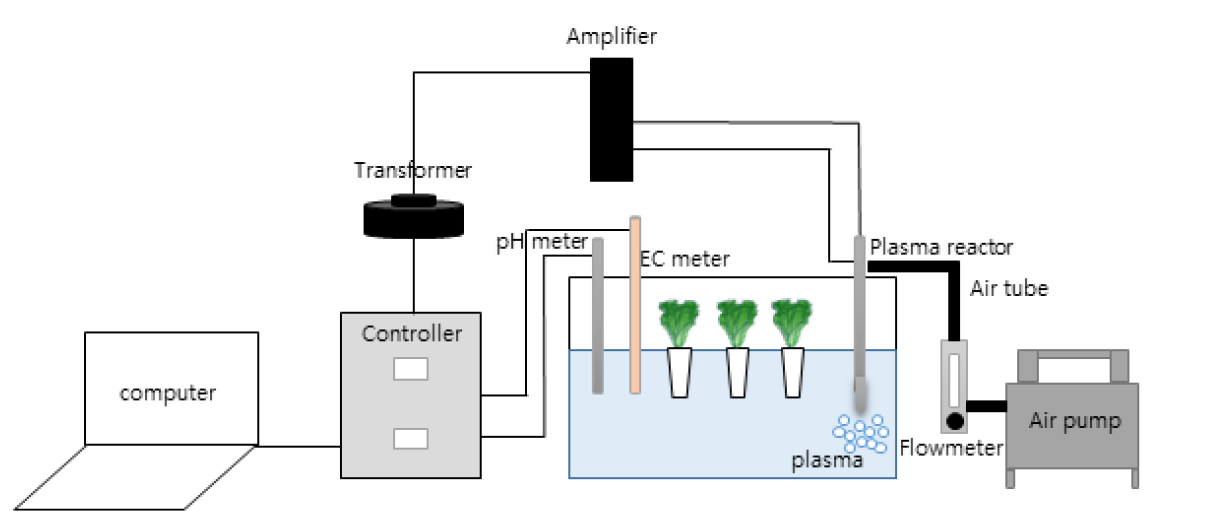
플라즈마는 코로나 방전을 이용해 수중에서 생성이 되었다. 전극 반경은 2mm이며, 전극을 둘러싸고 있는 석영관의 반경은 4mm로 구성되었다. 컴퓨터를 컨트롤러에 연결해 제어하는 방식이며 증폭기(amplifier)을 통해 전류를 증폭시켜 방전이 이루어졌으며 변압계가 결합된 전원장치를 통해 전압을 조절하였다. 플라즈마 발생용 변압기의 주파수는 25kHz 사인파(sine wave)로 최대전압은 4.2kV로 설정하였다. semi-DFT에서 플라즈마 장치가 작동 중 수중에 흐르는 최대전류는 30mA로 측정되었다. 산소 가스를 2L·min-1의 속도로 플라즈마 활성수 생성 시간 동안 주입하였다. 생성된 플라즈마는 유동과 함께 메쉬형 전극을 통해 양액 안에서 용존 되도록 플라즈마 발생 장치를 담액 수경재배 시스템과 결합을 하였다(Fig. 1).
플라즈마는 수확 전 24시간 동안 배양액 조건에서 작동시켰다. 수중에서 플라즈마가 발생하는 동안 pH, EC 및 과산화수소(H2O2)의 변화를 살펴보고자 수돗물(tap water)에서 플라즈마 발생 전과 발생 후 2가지의 경우로 나누어 측정 및 분석하였다.
3. 생육조사 및 성분 분석
생육 조사를 위하여 각 처리구 당 5주를 분석하였으며, 페놀 함량 분석을 위해서 각 처리구 당 3주의 상추를 파괴 분석하였다. 상추의 생육 조사는 수확 후 캘리퍼스(SD500-300PRO, Shin Con CO. Ltd., Korea)를 이용하여 상추의 가장 큰 엽을 기준으로 엽장, 엽폭, 근장을 측정하였으며, 처리구별 비파괴 엽록소 함량을 측정하기 위하여 단위면적당 엽록소 수치를 SPAD-502(Minolta Camera Co. Ltd., Japan)을 이용하여 측정하였다. 지상부의 생체중 및 근권부의 생체중은 전자저울(MW-2N, CAS Co. Ltd., Korea)을 이용하여 측정하였다. 건물중 측정을 위해 지상부와 근권부를 각각 시료 분석용 봉투에 넣어 70℃로 설정한 건조기(HB-501M, Hanbaek Scientific Technology Co. Ltd., Korea)에 7일간 건조 시킨 후 동일한 전자저울로 측정하였다.
상추의 바이오 활성 물질 및 폴리페놀 함량 분석은 Noh 등(2020)의 방법을 참고하였다. 상추를 동결건조기(TFD5503, Ilshin BioBase Co. Ltd., Korea)를 이용하여 건조히였다. 이후, 믹서기(SMX 800SP, Shinil Co. Ltd., Korea)에 넣어 분쇄한 후 유발과 유봉을 이용하여 분말화시켰다. 각 처리구와 대조구 상추 분말 50mg을 MeOH(2ml의 80%)에 넣은 후 1시간 동안 초음파처리(Sonication)한 후 10분간 원심분리를 하였다. 그리고 상청액을 추출하여 필터링 후 HPLC용 vial에 담았다. 폴리페놀 함량 분석은 HPLC 1260 Infinity II(Agilent Technologies Co. Ltd., The United States)를 이용해 진행하였으며, 컬럼(column)은 optimapak C18 column(250 × 4.6mm, 5μm)을 사용하였으며, 컬럼 온도 30℃, 유량 1.0ml·min-1, 검출 파장 280nm로 설정하였다. 이동상 용매로는 0.15% 아세트산을 포함한 solvent A 와 80% MeOH를 solvent B로 사용하여 분석을 진행하였다. 용매 구배는 solvent B를 기준으로 실시하였고 총 27분간 분석하였다. Solvent B는 처음 2분까지는 0%로 유지하였고 7분에 0에서 10%로 증가시키고, 16분에는 10에서 31%로 증가시켰다. 19분에는 31%를 유지 시키고 21분까지 31에서 0%로 감소, 27분에는 0%를 유지하였다.
4. 통계 분석
측정 데이터의 통계 분석은 SPSS 프로그램(SPSS 20, SPSS Inc., Chicago, IL, USA)을 사용하여 ANOVA 변량분석을 수행하였으며, 평균 간 유의차 검증을 위하여 Tukey의 다중검정법으로 유의수준 p ≤ 0.05 에서 분석하였다.
결과 및 고찰
1. 플라즈마 활성수 분석
플라즈마 활성수 발생 전과 후로 나눠 비교 분석한 결과 pH는 발생 전 7.62에서 발생 후 7.24로 낮아졌으며(Fig. 2A), EC는 발생 후 발생 전에 비해 높아졌으나 변화량이 0.03 정도로 큰 차이를 보이지는 않았다(Fig. 2B). 과산화수소 함량은 플라즈마 발생 전 0.006에서 발생 후 10배 증가한 0.06의 수치를 보였다(Fig. 2C).
수경재배에서 플라즈마를 발생시키면 수중 pH가 감소하게 되는데, 이는 공기 중의 산소와 질소가 반응하여 질산성 질소(NO3-)를 만들기 때문이라 알려져 있다(Kim과 Park, 2012). 근권부 양수분의 흡수는 양액의 pH와 EC에 따라 달라지는데 (Trejo-Tellez와 Gomez-Merino, 2012), Lee 등(1998)이 pH 5에서 8까지의 상추 생육을 본 결과 양액의 pH가 8 이상이 되면 Fe, Cu, Mn 등의 금속 원소의 흡수가 저해되고 상추의 뿌리가 갈변하지만(Inden, 1982), pH 5에서 7까지는 생육에 차이가 없었다고 보고했다. 또한, pH 5.5에서 8.5 범위 내에서는 인삼 생육에 영향을 미치지 않는다는 연구결과도 보고되었다(Islam 등, 1980). 본 실험에서 변화된 pH 및 EC의 정량적 폭이 적었으며, 처리된 24시간은 식물체에 영향을 미치기에 짧은 시간이었다고 생각되며, 침지 처리 간 플라즈마 활성수의 화학적 특성은 상추 생육에 적합한 수준이었다고 판단된다.
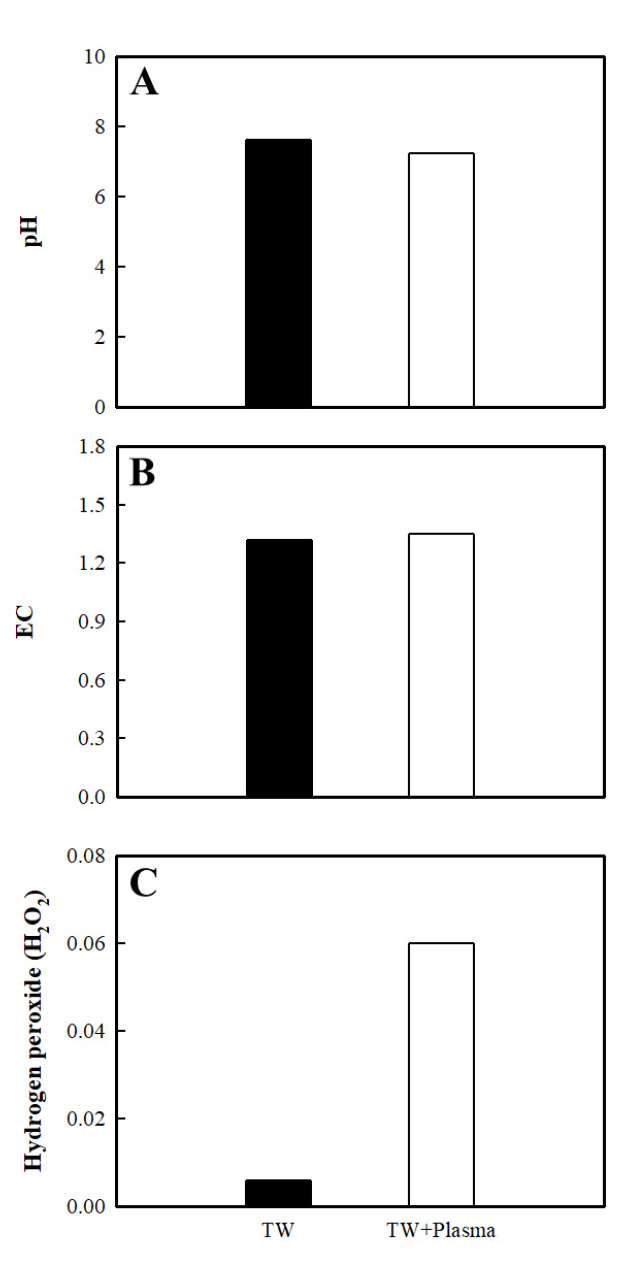
Fig. 2
pH values when in tap water (TW) and plasma generated in a tap water (TW+Plasma) (A), EC values when in tap water and plasma generated in a tap water (B), in the concentration of hydrogen peroxide(H2O2) when in a tap water and plasma generated in a tap water (C). A plasma generator is operated for 24 hour before harvest.
2. 생육분석
담액 수경재배에서 플라즈마 활성수와 과산화수소 희석수 침지에 따른 생육 분석결과 엽장은 대조구에서 평균 19.57cm로 가장 높은 수치를 나타냈고 과산화수소 6% 처리에서 가장 낮은 수치를 나타냈으며 통계적으로 유의적인 차이를 보였다(Fig. 3A). 엽폭의 경우엔 과산화수소 3% 처리에서 증가하다 6% 처리에서 감소하였으나, 유의적 차이는 발생하지 않았다. 단위 면적당 엽록소 함량을 비파괴적으로 나타내는 SPAD 값은 대조구에서 17.48로 가장 낮은 수치를 나타냈고, 과산화수소 0%, 3% 처리에서는 각각 18.18, 18.35로 큰 차이를 보이지 않았으나 과산화수소 6% 처리에서는 20.12로 가장 높은 수치를 나타내었다(Fig. 3B). 근장 역시 유의적인 차이는 보이지 않았으며 플라즈마 처리구에서 25.97cm로 가장 높은 수치를 나타내었다. 지상부 생체중은 과산화수소 0% 처리에서 42.97g으로 가장 높은 수치를 보였으며, 과산화수소 농도가 높아짐에 따라 수치가 낮아졌다(Fig. 3C). 지상부 건물중은 대조구에서 1.13g으로 가장 낮은 수치를 보였으며, 과산화수소 0% 처리구에서 1.80g으로 가장 높은 수치를 보였다. 근권부 생체중은 대조구에서 과산화수소 3%, 6% 처리구에 비해 각각 83.90%, 97.77%만큼 높은 수치를 보이며 유의미한 차이를 나타내었다(Fig. 3D). 근권부 건물중도 마찬가지로 유의적인 차이를 보이지 않았으며, 가장 수치가 낮은 플라즈마 처리구에 비해 과산화수소 6% 처리에서 0.11g 더 높은 수치를 나타냈다.
근권부에 과산화수소가 축적되면 농도가 높아질수록 뿌리 압력이 낮아지게 되고 지상부로의 수분 수송이 감소된다(Lee 등, 2004). 이는 과산화수소 농도가 증가할수록 평균값에서 지상부 생체중이 감소하는 경향(Fig. 3C)과 유사하였다. 과산화수소는 탈수를 일으킨다고 알려져 있는데(Bray, 1997), 이는 과산화수소 농도가 증가함에도 근권부 건물중은 차이를 나타내지 않으나 수분이 함유된 생체중에서는 뚜렷하게 차이를 나타낸 결과(Fig. 3D)와 일치했다. 저농도의 과산화수소는 근권부 발달에 긍정적인 영향을 미친다고 알려져 있다(Deng 등, 2012). Schützendübel 등(2002)의 연구에서 스코틀랜드 소나무(Populus × canescens)의 뿌리에 2mM의 과산화수소와 20mM의 과산화수소를 처리해 뿌리 생육을 비교하였는데, 저농도의 과산화수소 처리에서 고농도의 과산화수소 처리에 비해 103% 높은 결과를 나타냈다. 과산화수소는 뿌리털 신장에도 중요한 역할을 하지만, 고농도 처리 시 뿌리털 신장이 억제되는 결과를 보였다(Dunand 등, 2007). 이는 본 실험에서 과산화수소 고농도 처리 시 뿌리 생육이 억제된 결과와 유사하였다. 고농도의 과산화수소는 산화 스트레스를 유발한다(Chen 등, 2009). 그리고 높은 농도의 과산화수소는 직간접적으로 식물 발달에 중요한 역할을 하는 아스코르브 산(ascorbic acid), 글루타티온(glutathione)을 산화시키며, 세포발달에 필수적인 단백질, 지질, 핵산과 같은 생체분자들에 피해를 입혀 생육에 악영향을 미친다(Mittler, 2002). 또한, 높은 농도의 과산화수소는 세포가 죽는 아폽토시스(apoptosis)를 유도하는 것으로 알려져 있는데(Apel과 Hirt, 2004), 이는 24시간 플라즈마 활성수 및 H2O2 처리를 했을 때, 과산화수소에 침지한 상추의 뿌리가 6% 농도에서 갈변된다. Fig. 3의 결과는 이러한 식물 생육에 대한 고농도 과산화수소 영향에 대한 기존 연구 결과들로 설명 될 수 있었다.
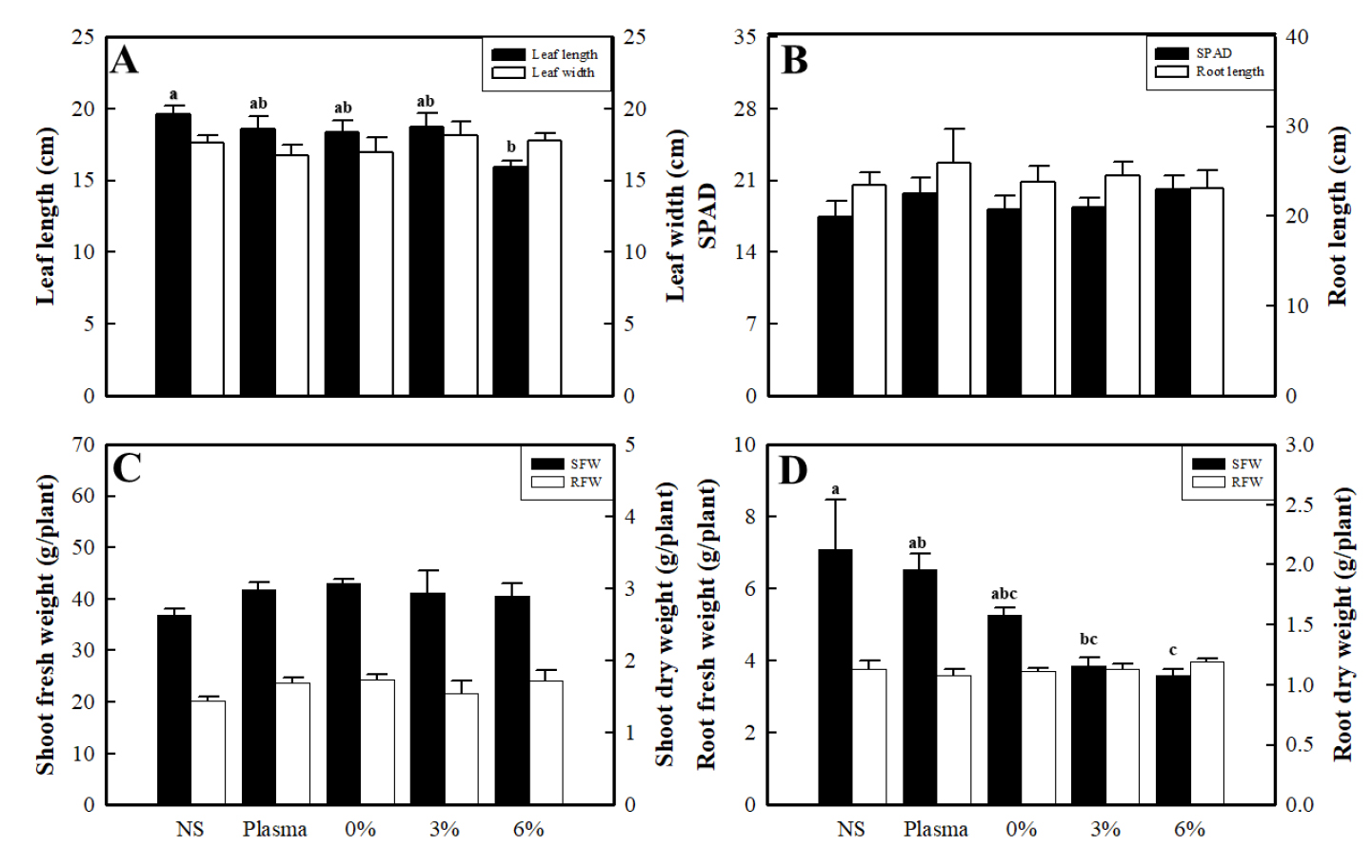
Fig. 3
Leaf length and leaf width (A), SPAD and root length (B), shoot fresh weight and shoot dry weight (C), root fresh weight and root dry weight (D) of the lettuce grown in the nutrient solution for 20 days and soaked in hydrogen peroxide and plasma activated water for 24 hours before harvest. The data represent the means and the vertical bars indicate standard errors (n=5) of Lactuca sativa (p ≤ 0.05).
3. 바이오 활성 물질 분석
담액 수경재배 시스템에 20일간 양액을 사용해 재배, 수확 24시간 전 플라즈마 및 과산화수소 처리를 한 후 바이오 활성 물질을 분석하였다. 상추의 단위 중량당 클로로겐산(chlorogenic acid)은 가장 높은 수치를 나타낸 과산화수소 6% 처리와 가장 낮은 수치를 나타낸 대조구에서 85%의 차이를 보였으며, 과산화수소 0%와 3% 처리를 제외하고 모든 처리구간에 유의적인 차이를 나타내었다(Fig. 4A). 4-hydroxy benzoic acid도 동일하게 과산화수소 6% 처리에서 0.61mg·g-1으로 가장 높은 수치를 나타냈으며, 과산화수소 0% 처리와 3% 처리 간에 유의적인 차이를 나타내지 않았다. 상추의 단위 중량당 4-hydroxy3-benzoic acid 농도는 과산화수소 6% 처리에서 1.58mg·g-1으로 가장 높은 수치를 나타냈으며, 모든 처리구간에 유의적인 차이를 나타내었다(Fig. 4B). 지상부 총 페놀 함량에서도 마찬가지로 과산화수소 6% 처리에서 가장 높은 수치를 나타냈으며, 대조구와 과산화수소 0% 처리간에 유의적인 차이를 나타내지 않았으나, 다른 처리구에서 모두 유의적인 차이를 나타내었다. 근권부 퀘르세틴(quercetin) 함량에서는 지상부와는 다르게 플라즈마 처리구에서 1.14mg·g-1으로 가장 높은 수치를 나타냈고, 과산화수소 농도가 높아질수록 감소하는 경향을 보였다(Fig. 4C). 근권부 총 페놀 함량도 플라즈마 처리구에서 가장 높았으며, 제일 낮은 수치를 보인 과산화수소 6% 처리와는 107.81% 차이를 보이며 유의적인 차이를 보였다.
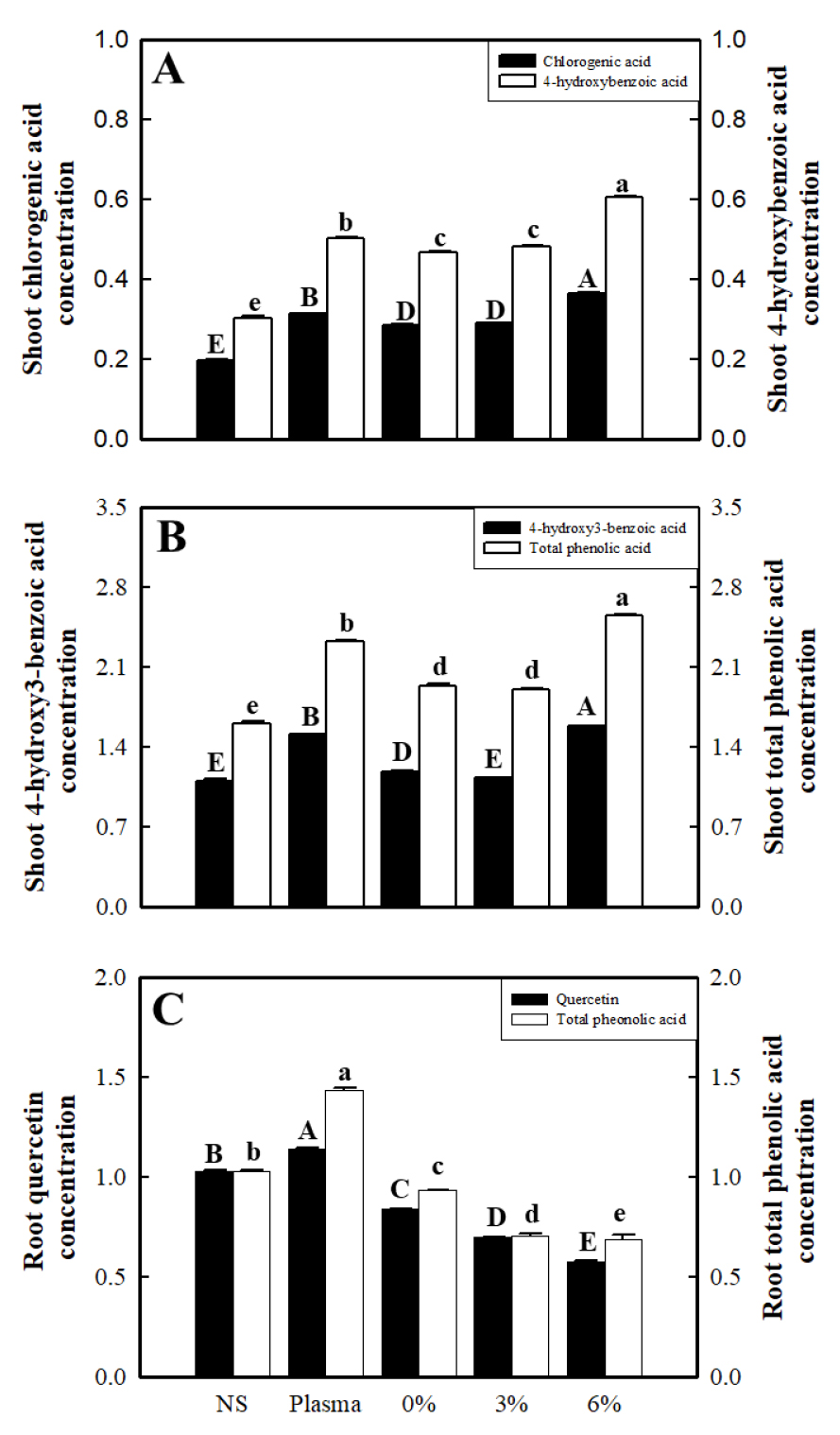
Fig. 4
Shoot chlorogenic acid contents and shoot 4-hydroxy benzoic acid contents (A), shoot 4-hydroxy3-benzoic acid contents and shoot total phenolic contents (B), root quercetin contents and root total phenolic contents (C) of lettuce grown in nutrient solution for 20 days and soaked in hydrogen peroxide and plasma activated water for 24 hours before harvest. The data represent the means and the vertical bars indicate standard errors (n=3). Different letters at the top of bars indicate significances of Lactuca sativa (p ≤ 0.05).
가뭄, 냉기 등의 자연 상황에서 야기되는 스트레스에 의해서 생성되는 활성산소종(ROS) 중 과산화수소는 낮은 농도에서는 유익하지만, 높은 농도에서는 세포에 부정적인 영향을 준다(Peng 등, 2005; Sharma 등, 2012). 저농도의 과산화수소는 폴리페놀과 같은 이차대사산물의 합성을 유도한다고 알려져 있는데(Moskova 등, 2009), 본 실험의 지상부 chlorogenic acid, 4-hydroxy benzoic acid, 4-hydroxy3-benzoic acid, 그리고 지상부 총 페놀 함량이 과산화수소 6% 처리에서 가장 높았던 결과는 기존 연구결과와 일치하였다. 근권부 quercetin 함량 및 근권부 총 페놀 함량은 높은 농도의 과산화수소 처리일수록 감소하는 결과를 나타내었는데, 이는 과산화수소에 직접 접촉하는 피해를 받았기 때문으로 판단된다.
담액 수경재배에서 플라즈마 활성수 및 과산화수소 침지에 따른 상추의 바이오 활성 물질 함량 변화를 분석해본 결과 플라즈마 활성수 처리에서 지상부 이차대사산물 함량은 과산화수소 6% 처리와 유사하였고, 특히 과산화수소 6% 처리와 다르게 근권부에서 생리 장해를 일으키지 않았다. 플라즈마 발생기를 이용하여 수확 1시간 전 플라즈마 활성수에 상추를 침지처리 하는 본 기술을 엽채류의 수경재배 시스템에 적용할 경우 지상부의 이차대사산물 함유량을 증대시키는 효과를 보였다. 또한, 과산화수소 침지 처리가 고농도에서 근권부를 괴사시킨 반면 플라즈마 활성수 처리는 생육 장해를 일으키지 않았으며, 바이오 활성 물질 함량은 더 높았다. 위와 같은 효과를 볼 때, 본 기술의 도입은 주로 섭취되는 지상부 그리고 근권부의 높은 바이오 활성 물질을 기대 할 수 있을 것으로 예상된다.