서 론
재료 및 방법
1. 식물 재료 및 재배 조건
2. 필름 처리 및 분광 특성
3. 생육 조사
4. 엽 광합성 속도
5. 통계분석
결과 및 고찰
1. 광 스펙트럼 및 필름의 투과 특성
2. 광-광합성 반응 및 엽록소 함량
3. 묘의 생육 및 형태형성
서 론
광은 식물의 생장에 필수적인 요소이며, 광질은 식물의 생육과 형태형성 반응을 결정한다(Dieleman 등, 2019). 적색광을 인지하는 광수용체인 phytochrome은 종자 발아, 줄기 신장, 잎의 확장, 개화 유도 등 다양한 식물의 생육 및 발달 반응을 매개하고(Smith, 2000), 청색광은 cryptochrome과 phototropin 등의 광수용체로부터 인지되어 광형태형성, 굴광성, 기공 개폐 등 다양한 기작에 관여한다고 알려져 있다(Schulze 등, 2019). 또한 청색과 적색 등 서로 다른 광질의 혼합 이용은 식물의 엽록소 함량 및 순광합성 속도에도 직접적인 영향을 미친다(Lee 등, 2007). 식물의 엽록소는 주로 적색(663nm와 642nm) 및 청색(430nm와 453nm) 영역의 빛을 흡수하며, 광합성에 대한 분광 양자수율은 적색광과 청색광에서 가장 높은 것으로 알려져 있다(McCree, 1971). 그러나 발광다이오드(light emitting diode, LED)와 같은 단색광을 이용한 이전 연구들은 자연광 같이 다양한 파장의 스펙트럼이 동시에 식물에게 미치는 영향을 설명하기에는 충분하지 않다.
태양광은 온실 피복재를 통과하여 작물에 도달하며, 온실 내 광환경은 피복재의 광학적 특성에 따라 결정된다. 광전환필름은 작물의 광합성 및 생육을 향상시키기 위하여 태양광 스펙트럼을 변형시키는 기능성 피복재이다(Lamnatou와 Chemisana, 2013). 광전환필름은 상대적으로 높은 에너지를 가지면서 광합성 효율이 낮은 파장(주로 280-400nm의 자외선 또는 500-600nm의 녹색)을 흡수하여 광합성 효율이 높은 긴 파장(주로 400-500nm의 청색 또는 600-700nm의 적색)으로 발광하는 광전환재를 포함하며, 일반적으로 자외선을 청색으로 또는 녹색을 적색으로 전환시킨다(Park 등, 2016). 기존 연구들에 따르면 광전환필름은 여러 작물에서 생육을 촉진하고 생산성을 향상시킨다고 알려져 있어왔다(Hidaka 등, 2008; Nishimura 등, 2009; Park 등, 2016). 최근에는 광전환 필름에서의 식물의 광합성 효율 증가와 그 메커니즘에 대한 연구가 보고되고 있지만(Li 등, 2017; Yoon 등, 2020a), 광전환필름으로 인한 태양광의 광질 변화에 따라 발생하는 형태형성적 영향에 대해서는 충분히 보고되지 않다.
광질에 의한 식물의 형태형성 반응은 발달 단계 전반에 걸쳐 다양하게 나타나며, 생육 초기의 반응은 그 자체로 묘소질을 결정한다. 채소류의 묘소질은 정식 후 생육과 수량에 큰 영향을 미칠 수 있으며, 도장을 억제하고 지하부 생육을 촉진하여 충실도 높을수록 품질이 높은 묘라고 할 수 있다. 최근에도 LED 조명에 따른 참외와 오이 등 과채류의 묘소질에 대한 연구들이 보고되고 있다(Jeong 등, 2020a; Lee 등, 2016). 오이는 광질에 민감한 주요 시설 원예작물 중 하나로, 많은 연구자들이 광질에 대한 식물의 광합성 및 형태형성 반응을 연구하는 데에 이용하고 있다(Hogewoning 등, 2012; Kang 등, 2020). 엽채류 중에서도 상추와 배추는 대표적인 쌈 채소로 국내에서 신선 상태로 소비되고 있으며 연중 생산을 위해 시설 재배의 비중이 늘어가는 추세다. 상추의 경우 광전환필름 및 LED 조합을 포함하여 다양한 광질에서의 광합성 및 생육에 대해 이전 연구들에서 보고된 바 있다(Nishimura 등, 2009; Son과 Oh, 2013). 본 연구는 광전환 필름에 의해 변형된 태양광 스펙트럼이 상추와 배추, 오이의 묘 생장과 형태특성, 광합성 효율에 미치는 영향을 구명하고자 수행되었다.
재료 및 방법
1. 식물 재료 및 재배 조건
본 실험은 경기도 수원시(37°16'N, 126°59'E)에 위치한 서울대학교 실험 온실에서 수행되었다. 온실 내 기온은 천창 환기 및 온수 난방을 통해 주간 25°C, 야간 15°C로 조절되었다. 실험 작물로는 로메인 상추(Lactuca sativa L.) ‘시저스그린’, 배추(Brassica rapa L. ssp. pekinensis) ‘CR노랑쌈’, 오이(Cucumis sativus L.) ‘조은백다다기’의 엽채류 및 과채류 3종을 이용하였다. 2020년 11월 6일에 각 종자를 원예용 혼합 상토(‘쑥쑥이’, Nongwoo Bio Co., Ltd., Korea)가 충진된 50구 플러그 트레이에 파종하였으며, 실험 필름을 각 트레이에 아치형으로 피복하였다. 파종 후 각 트레이는 점적관을 이용하여 1일 2회 10분씩 저면관수하였다.
2. 필름 처리 및 분광 특성
실험에 사용된 필름은 광전환 필름(spectrum conversion film, SCF)와 대조구로서 상업용 폴리에틸렌 필름(Tajopyo PE, Taekwangnewtec Co., Ltd., Korea)이 이용되었다. SCF는 자외선을 청색으로 전환하는 형광 염료와 녹색을 적색으로 전환하는 형광 염료, 근적외선을 차단하는 염료를 포함하는 필름이며, 실험에 사용된 필름의 전광선 투과율은 이전 연구에 따라 분광복사계(BLUE-Wave spectrometer, StellarNet, Inc., USA)와 적분구(IC-2, StellarNet, Inc.)를 이용하여 300-900nm 파장 범위에서 측정하였으며, 솔라시뮬레이터(XIL-01B50KPV1, SERIC, Ltd., Japan) 광원을 이용하였다(Yoon 등, 2020b). 필름이 피복된 온실 내 분광 분포는 2020년 12월 30일 오후 12시에 스펙트로라디오미터를 이용하여 측정하였다.
3. 생육 조사
상추와 배추는 12월 7일(피복 후 31일차)에 본엽이 5매가 되었을 때, 오이는 화방 및 덩굴손이 출현한 12월 17일(피복 후 41일차)에 6개체씩 무작위로 선별하여 지상부와 지하부 생체중, 초장을 측정하였다. 작물의 엽병, 절간(1-2번째 마디 사이) 길이, 엽면적, 엽장 및 엽폭은 작물 사진을 촬영한 후 이미지 소프트웨어(ImageJ 1.49, National Institutes of Health, USA)를 이용하여 획득하였고, SPAD 값은 엽록소 측정기(SPAD-502 Plus, Konica Minolta Inc., Tokyo, Japan)를 이용하여 완전히 전개된 잎을 측정하였다. 지상부 생체중을 측정한 후 건조 오븐에서 75°C로 1주일 건조한 뒤 중량을 측정하여 건물중으로 삼았다. 비엽면적(specific leaf area, SLA), 왜화율(dwarf rate), 묘의 충실도(compactness)는 기존 연구에 따라 아래의 계산식으로 산출하였다(Jeong 등, 2020b).
4. 엽 광합성 속도
광합성 속도는 작물의 완전히 전개한 잎을 대상으로 휴대용 광합성 측정기(LI-6400XT, Li-Cor Inc., USA)와 LED 챔버(6400-02B, Li-Cor Inc.)를 사용하여 오전 10시부터 오후 3시까지 생육 조사와 동일한 날에 처리구별 4개체씩 광 반응곡선을 측정하였다. 모든 측정 전 잎을 챔버 내에서 1000μmol·m-2·s-1 광합성 유효광량자속밀도(Photosynthetic photon flux density, PPFD)로 약 15분 동안 적응시켰으며, 챔버 내의 엽온은 22.1±1.5°C, 상대습도는 66.1±6.7%, CO2 농도는 400μmol·mol-1로 동일한 조건에서 측정하였다. 광합성속도는 0, 100, 200, 400, 600, 900, 1200, 1500μmol·m-2·s-1 PPFD 수준에서 획득했다. CO2 동화에 대한 광반응 곡선은 직각쌍곡선 모델을 이용하였으며, 다음의 식으로 표현된다.
Pn은 순 광합성속도(μmol CO2·m-2·s-1), Rd는 호흡속도(μmol CO2·m-2·s-1), Pmax는 최대 광합성속도(μmol CO2·m-2·s-1), I는 광합성 유효광양자속밀도(μmol·m-2·s-1), θ는 I가 0μmol·m-2·s-1일 때의 광자 수율을 의미한다. 광도에 따른 상추, 배추, 오이 묘의 엽 광합성 속도 측정 결과를 이용하여 비선형 회귀분석을 실시하였다.
5. 통계분석
생육조사 결과의 경우, 6개체 중 최대값과 최소값을 갖는 개체를 제외한 후 통계 분석을 진행하였다. 생육 조사 및 광합성 속도 결과는 Student’s t-test를 실시하였고, 처리 간 차이를 비교하였다. 광합성의 광반응 곡선의 회귀분석을 포함하여 모든 통계 분석과 그래프 작성은 R 소프트웨어(R 3.6.2, R Foundation, Austria)를 사용하였다.
결과 및 고찰
1. 광 스펙트럼 및 필름의 투과 특성
광전환 필름(SCF)과 대조구 필름으로 피복된 실험 온실로 투과된 태양광의 분광분포는 Fig. 1에 나타내었다. 대조구 필름 대비 SCF 피복 온실의 PPFD는 적색 파장대(600–700 nm)에서 10.1% 증가하였고, 청-녹색 파장대(400–600 nm)에서 13.6% 감소하였다. 적색 대 원적색(R/FR) 비는 SCF와 대조구 필름에서 각각 1.5, 1.4로 나타났고, PPFD는 대조구 필름 대비 SCF 하에서 4.8% 감소하였다. 대조구 필름 대비 SCF의 투과율은 적색 파장대에서 16.1% 높았으며, 청-녹색 파장대에서 10.8% 감소하였다(Fig. 1B, Table 1). 100%보다 높은 투과율은 입사된 광량보다 투과된 광량이 높음을 의미하며, 형광 특성을 갖는 SCF에서만 발견된다. 이전 연구에 따르면 SCF와 같은 형광 필름의 경우, 측정 광원의 스펙트럼에 따라 투과율이 다르게 나타난다(Yoon 등, 2020b). 따라서 본 실험에서는 태양광과 가장 유사한 인공 광원인 솔라시뮬레이터에서 측정하였다.
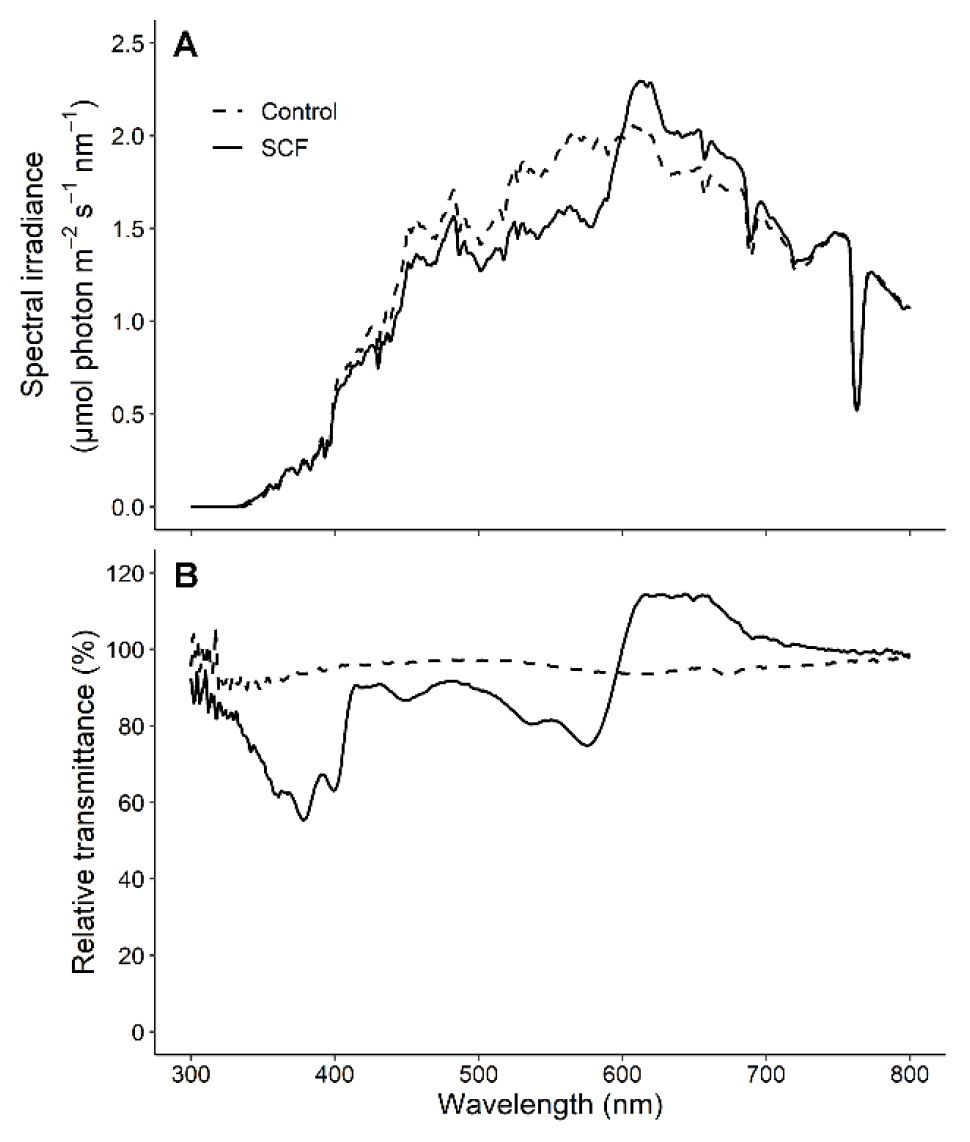
Fig. 1
Spectral distributions (A) of incident light under the spectrum conversion film (SCF) and poly-ethylene film (Control) measured in the experimental site at 12:00 h on 30 December 2020. Total transmittances (B) of the films measured using a spectroradiometer with an integrating sphere and relative percentages to incident light.
Table 1.
Spectral transmittance of the spectrum conversion film (SCF) and poly-ethylene film (Control) before covering.
|
Film
|
Transmittance (%)
|
|
Ultravioletz |
Blue
|
Green
|
Red
|
PAR
|
Far-red
|
|
Control
|
94.4
|
96.5
|
95.6
|
94.3
|
95.5
|
96.5
|
|
SCF
|
75.9
|
87.9
|
82.7
|
110.4
|
93.7
|
100.0
|
2. 광-광합성 반응 및 엽록소 함량
엽 광합성속도는 대조구 필름 대비 SCF 하에서 자란 배추와 오이 묘에서 유의적으로 증가하였으며, 상추 묘에서는 차이가 나타나지 않았다(Fig. 2). 회귀분석 결과 광반응 곡선의 매개 변수 값은 Table 2에 나타내었다. 최대 광합성속도(Pmax)는 대조구 필름 대비 SCF 하에서 자란 배추와 오이 묘에서 각각 23.1%, 19.0% 높았다. 반대로 호흡 속도(Rd)는 SCF 처리구의 배추와 오이 묘에서 각각 40.1%, 26.0% 감소하였다. 이러한 결과는 이전의 파프리카를 대상으로 녹색에서 적색으로 전환시키는 광전환 필름 처리와 동일하였다(Yoon 등, 2020a). 마찬가지로 광전환 필름에서 자란 Arabidopsis가 대조구에 비해 1200μmol·m-2·s-1 PPFD에서 순 광합성속도가 유의적으로 증가한 바 있다(Li 등, 2017). 본 연구에서 동일한 광원(적색 및 청색 LED)으로 측정한 결과를 통해 광전환필름에 의해 변형된 태양광이 작물의 잎 자체의 광합성 효율을 높이는 광합성 순응 반응을 유도한 것으로 추측할 수 있다. 또한 선행 연구에서는 이러한 순응 반응이 특히 광계1(photosystem I) 주위의 cyclic electron flow를 높여 CO2 동화를 촉진한 것으로 제안하고 있다(Li 등, 2017; Yoon 등, 2020a). 모든 회귀식의 결정 계수(R2)가 0.9 이상으로 매우 높았으며, 본 연구에서 사용된 광합성 모델식이 광-광합성속도를 잘 설명하고 있음을 나타낸다(Table 2). 직각 쌍곡선 모델의 경우 광-광합성 반응 곡선을 나타내는 간단한 모델로 이전 연구에서도 이용되고 있다(Lobo 등, 2013).
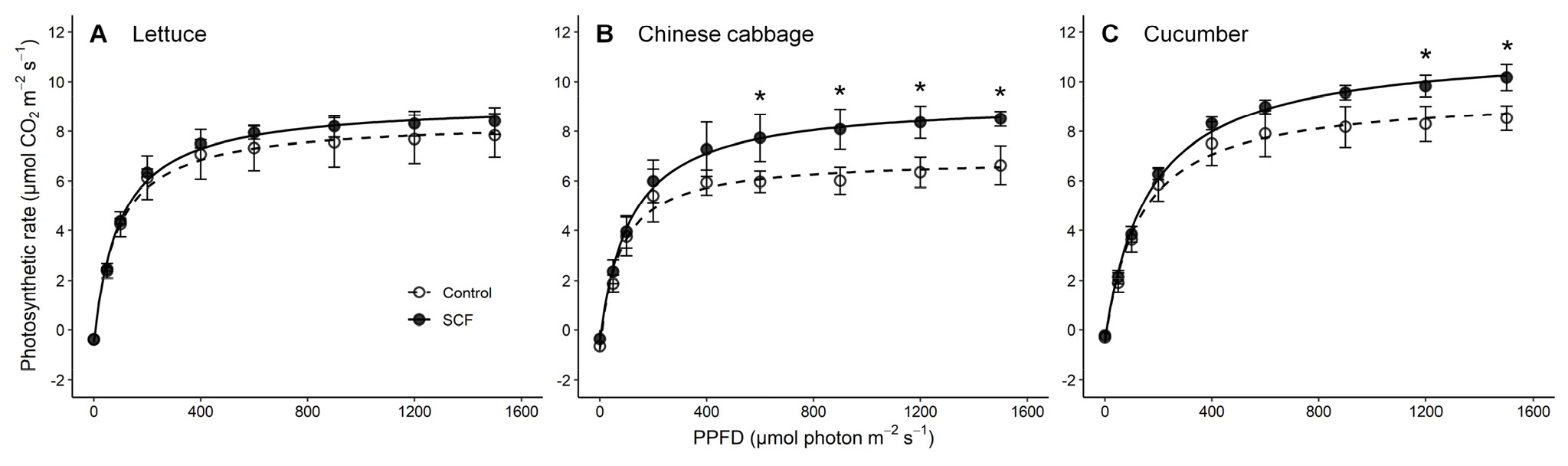
Fig. 2
Light-response curves of net photosynthesis (Pn) in the fully expanded leaves of the romaine lettuce (A), Chinese cabbage (B), and cucumber (C) seedlings grown under the spectrum conversion film (SCF) and poly-ethylene film (Control) for 31, 31, and 41 days, respectively. The regression curves were obtained by Eq. (4) (Refer to Table 4 for the parameters). The vertical bars indicate SD, n = 4. The asterisk indicates significant differences via Studentꞌs t-test, *p < 0.05.
Table 2.
The parameters and coefficients of determination (R2) for photosynthetic light-response curves of the romaine lettuce, Chinese cabbage, and cucumber seedlings grown under the SCF and poly-ethylene film (Control) for 31, 31 and 41 days, respectively.
|
Plant
|
Film
| Rdz(μmol CO2·m-2·s-1)
| Pmax (μmol CO2·m-2·s-1)
| θ(μmol CO2·m-2·s-1)
|
R2 |
|
Lettuce
|
Control
|
0.509
|
8.89
|
0.105
|
0.939
|
|
SCF
|
0.522
|
9.68
|
0.101
|
0.987
|
|
Chinese cabbage
|
Control
|
0.753
|
7.85
|
0.100
|
0.921
|
|
SCF
|
0.451
|
9.66
|
0.086
|
0.962
|
|
Cucumber
|
Control
|
0.522
|
9.94
|
0.079
|
0.964
|
|
SCF
|
0.386
|
11.83
|
0.072
|
0.992
|
단위 면적당 엽록소 함량을 나타내는 SPAD 값은 상추와 배추 묘에서는 필름 처리에 따른 차이가 나타나지 않았으나, 오이 묘에서는 SCF 처리구에서 유의적으로 7.2% 증가하였다(Tables 3, 4). 청색광이 엽록소 생합성에 미치는 주요 효과는 이전 연구에서 보고된 바 있으며(Hogewoning 등, 2010), 그 효과는 자외선 또는 적색광의 유무, 적색 대 청색(R/B) 비 등에 따라 결과가 상이하였다(Son과 Oh, 2013; Huché-Thélier 등, 2016). 한편 이전 연구들에서 복합 광원 하에서는 원적색광이 적을수록, 즉 R/FR이 증가했을 때 SPAD 값이 증가된다고 보고한 바 있다(Jeong 등, 2020a; Zhang 등, 2020). 본 연구에서는 SCF 처리구 하에서 줄어든 청색광에도 불구하고, 감소한 자외선량 및 높은 R/B 비(SCF의 경우 1.8, 대조구의 경우 1.5)로 인해 오이 잎의 단위 면적당 엽록소 농도의 증가로 인해 나타난 결과로 판단된다.
Table 3.
Growth and morphology of the romaine lettuce and Chinese cabbage seedlings grown under the spectrum conversion film (SCF) and poly-ethylene film (Control) for 31 days.
|
Plant
|
Film
|
Fresh weight (g)
|
Dry weight (g)
|
SPAD value
|
|
Leaf
|
Root
|
Leaf
|
Root
|
|
Lettuce
|
Control
|
2.7 ± 0.2z |
1.0 ± 0.1
|
0.19 ± 0.01
|
0.07 ± 0.01
|
24.9 ± 1.9
|
|
SCF
|
2.7 ± 0.2
|
0.7 ± 0.1
|
0.16 ± 0.01
|
0.04 ± 0.01
|
23.5 ± 2.1
|
| |
ns
|
**
|
*
|
**
|
ns
|
|
Chinese cabbage
|
Control
|
2.4 ± 0.2
|
1.1 ± 0.0
|
0.26 ± 0.02
|
0.08 ± 0.01
|
23.7 ± 1.3
|
|
SCF
|
2.4 ± 0.1
|
1.1 ± 0.2
|
0.32 ± 0.01
|
0.08 ± 0.00
|
23.8 ± 0.3
|
| |
ns
|
ns
|
**
|
ns
|
ns
|
|
Plant
|
Film
|
Leaf area (cm2)
|
Leaf length (cm)
|
Leaf width (cm)
|
Plant height (cm)
|
|
Lettuce
|
Control
|
79.3 ± 4.9
|
11.3 ± 0.7
|
3.9 ± 0.1
|
11.1 ± 1.5
|
|
SCF
|
80.1 ± 6.5
|
13.8 ± 1.3
|
3.7 ± 0.3
|
14.8 ± 1.9
|
| |
ns
|
*
|
ns
|
*
|
|
Chinese cabbage
|
Control
|
75.0 ± 4.7
|
9.5 ± 0.9
|
4.4 ± 0.4
|
9.4 ± 0.8
|
|
SCF
|
73.2 ± 4.9
|
8.9 ± 0.2
|
4.5 ± 0.1
|
8.2 ± 0.6
|
| |
ns
|
ns
|
ns
|
ns
|
Table 4.
Growth and morphology of the cucumber seedlings grown under the spectrum conversion film (SCF) and poly-ethylene film (Control) for 41 days.
|
Film
|
Fresh weight (g)
|
Dry weight (g)
|
SPAD value
|
|
Leaf
|
Petiole and stem
|
Root
|
Leaf
|
Petiole and stem
|
Root
|
|
Control
|
2.8 ± 0.3
|
2.3 ± 0.2
|
1.9 ± 0.6
|
0.63 ± 0.09
|
0.25 ± 0.03
|
0.22 ± 0.03
|
28.4 ± 0.8
|
|
SCF
|
2.6 ± 0.1
|
1.9 ± 0.3
|
2.0 ± 0.1
|
0.63 ± 0.04
|
0.23 ± 0.02
|
0.22 ± 0.01
|
30.5 ± 0.9
|
|
ns
|
*
|
ns
|
ns
|
ns
|
ns
|
*
|
|
Film
|
Leaf area
(cm2)
|
Leaf length
(cm)
|
Leaf width
(cm)
|
Plant height
(cm)
|
Petiole length
(cm)
|
Internode length
(cm)
|
|
Control
|
114.5 ± 16.0
|
8.7 ± 0.8
|
10.5 ± 0.2
|
20.4 ± 2.4
|
3.2 ± 0.2
|
5.2 ± 0.9
|
|
SCF
|
130.9 ± 11.5
|
8.9 ± 0.5
|
10.1 ± 0.2
|
15.4 ± 3.0
|
2.5 ± 0.4
|
4.5 ± 1.4
|
|
ns
|
ns
|
*
|
*
|
*
|
ns
|
3. 묘의 생육 및 형태형성
대조구 필름과 SCF 하에서 자란 묘의 생육 및 형태 변화는 작물별로 다른 양상을 나타내었다(Tables 3, 4, Fig. 3). 대조구 필름 대비 SCF 하에서 자란 상추 묘의 경우, 뿌리의 생체중과 건물중, 잎의 건물중이 유의적으로 감소하였으며, 엽장이 길어짐에 따라 초장이 증가하였다. 반면에 SCF 하에서 자란 배추 묘의 경우, 대조구 필름 대비 잎의 건물중이 유의적으로 21.3% 증가하였으며 엽형태의 경우 큰 차이를 보이지 않았다. 오이 묘의 경우, 필름 처리에 따라 줄기의 건물중은 차이 없으나 SCF 처리구에서 초장은 유의적으로 24.5% 감소하였으며 엽병과 줄기의 생체중이 20.5% 유의적으로 감소하였는데, 이는 엽병 길이의 20.1% 유의적 감소에 의한 것으로 추정되었다. 유사하게 광전환필름 하에서의 엽병 길이 감소는 파프리카를 대상으로 한 이전 연구에서도 나타났다(Yoon 등, 2020a). 엽병 생장은 피토크롬(phytochrome)에 의해 조절되는 반응으로 일반적으로 R/FR 비가 낮은 음지 환경에서 나타난다(Lötscher와 Nösberger, 1997; Ranwala 등, 2002). 또한 식물은 수광량을 높이기 위한 전략으로 엽병 길이가 증가되기도 한다(Duursma 등, 2012; Takenaka, 1994). 따라서 본 연구에서 SCF하에서 높은 R/FR 비와 형광 소재에 의한 적색 산란광에 의해 오이 묘의 엽병 길이 신장이 억제되었다고 추측된다.

Fig. 3
Representative images of the romaine lettuce, Chinese cabbage, and cucumber seedlings grown under the spectrum conversion film (SCF) and poly-ethylene film (Control) for 31, 31 and 41 days, respectively.
대조구 필름과 SCF 하에서 자란 묘의 품질을 나타내는 비엽면적과 충실도, 왜화율은 Fig. 4에 나타내었다. SCF 처리구에서 배추의 충실도는 유의적으로 38.3% 증가하고 왜화율은 10.3%로 나타났다. 마찬가지로 SCF 하에서 자란 오이 묘의 충실도는 31.7% 증가했고, 왜화율은 24.2%로 높았다. 충실도는 전체 건물중에 지상부의 초장을 나눈 값으로, 그 값이 높을수록 묘의 품질이 우수하다고 보고되고 있다(Jo 등, 2021; Lee 등, 2016). 왜화율은 수치가 높을수록 대조구에 비해 초장이 감소하여 생장 억제 효과가 있는 것으로 보며, 묘의 도장이 줄어듦을 나타낸다(Jeong 등, 2020b). 잎의 두께를 간접적으로 나타내는 비엽면적은 값이 클수록 잎의 두께가 얇은 것을 의미하는데, 상추에서 유의적으로 증가하였으며, Kim 등(2021)은 왕고들빼기에서 광도가 높을수록 비엽면적이 감소한다고 보고한 바 있다. 또한 SCF 하에서 자란 상추 묘의 충실도가 유의적으로 감소하고, 왜화율이 음의 값을 나타내어 묘소질이 저하되었다. 이는 SCF에서의 낮은 PPFD에 의해 상추 묘가 도장한 결과로 보인다. 반면에 SCF 처리구에서의 배추와 오이 묘의 품질 향상은 낮은 PPFD에도 불구하고 태양광의 광질 변화로 인한 광합성 속도 증가와 형태형성적 변화 유도에 따른 결과로, 광전환 필름이 일반 상업용 필름에 비해 배추와 오이 묘의 도장 억제 및 묘소질 향상에 효과적임을 나타낸다.
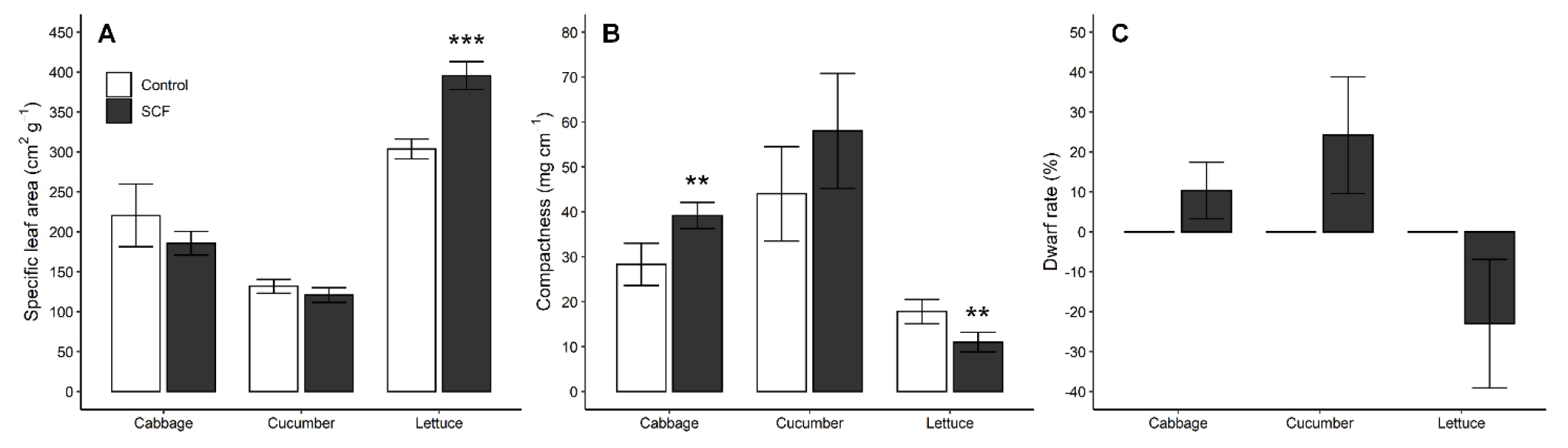
Fig. 4
Specific leaf area (A), compactness (B), and dwarf ratio (C) of the romaine lettuce, Chinese cabbage and cucumber seedlings grown under the spectrum conversion film (SCF) and poly-ethylene film (Control) for 31, 31 and 41 days, respectively. The parameters were calculated by Eqs. (1), (2), (3). The vertical bars indicate SD, n = 4. The asterisk indicates significant differences via Studentꞌs t-test, **p < 0.01; ***p < 0.001.
Acknowledgements
이 연구는 산업통상자원부 및 산업기술평가관리원(KEIT) 지원으로 수행되었음(10052798).
References
Dieleman J.A., P.H.B. de Visser, E. Meinen, J.G. Grit, and T.A. Dueck 2019, Integrating morphological and physiological responses of tomato plants to light quality to the crop level by 3D modeling. Front Plant Sci 10:1-12. doi:10.3389/fpls.2019.00839
10.3389/fpls.2019.0083931354751PMC6637845Duursma R.A., D.S. Falster, F. Valladares, F.J. Sterck, R.W. Pearcy, C.H. Lusk, K.M. Sendall, M. Nordenstahl, N.C. Houter, B.J. Atwell, N. Kelly, J.W.G. Kelly, M. Liberloo, D.T. Tissue, B.E. Medlyn, and D.S. Ellsworth 2012, Light interception efficiency explained by two simple variables: a test using a diversity of small- to medium-sized woody plants. New Phytol 193:397-408. doi:10.1111/j.1469-8137.2011.03943.x
10.1111/j.1469-8137.2011.03943.x22066945Hidaka K., K. Yoshida, K. Shimasaki, K. Murakami, D. Yasutake, and M. Kitano 2008, Spectrum conversion film for regulation of plant growth. J Fac Agric Kyushu Univ 53:549-552. doi:10.5109/12872
10.5109/12872Hogewoning S.W., E. Wientjes, P. Douwstra, G. Trouwborst, W. van Ieperen, R. Croce, and J. Harbinson 2012, Photosynthetic quantum yield dynamics: From photosystems to leaves. Plant Cell 24:1921-1935. doi:10.1105/tpc.112.097972
10.1105/tpc.112.09797222623496PMC3442578Hogewoning S.W., G. Trouwborst, H. Maljaars, H. Poorter, W. Ieperen, and J. Harbinson 2010, Blue light dose-responses of leaf photosynthesis, morphology, and chemical composition of
Cucumis sativus grown under different combinations of red and blue light. J Exp Bot 61:3107-3117. doi:10.1093/jxb/erq132
10.1093/jxb/erq13220504875PMC2892149Huché-Thélier L., L. Crespel, J.L. Gourrierec, P. Morel, S. Sakr, and N. Leduc 2016, Light signaling and plant responses to blue and UV radiations-Perspectives for applications in horticulture. Environ Exp Bot 121:22-38. doi:10.1016/j.envexpbot.2015.06.009
10.1016/j.envexpbot.2015.06.009Jeong H.W., H.R. Lee, H.M. Kim, H.M. Kim, H.S. Hwang, and S.J. Hwang 2020a, Using light quality for growth control of cucumber seedlings in closed-type plant production system. Plants 9:639. doi:10.3390/plants9050639
10.3390/plants905063932429540PMC7284851Jeong H.W., H.R. Lee, H.S. Hwang, E.B. Kim, and S.J. Hwang 2020b, Growth suppression of tomato plug seedlings as affected by material type for brushing stimulation. Prot Hortic Plant Fact 29:313-319. doi:10.12791/KSBEC.2020.29.4.313
10.12791/KSBEC.2020.29.4.313Jo H.G., H.W. Jeong, H.R. Lee, S.M. Kwon, H.S. Hwang, and S.J. Hwang 2021, Growth of tomato and pepper grafted plug seedlings under different shading condition during acclimatization after graft-taking. J Bio-Environment Control 30:10-18. doi:10.12791/KSBEC.2021.30.1.010
10.12791/KSBEC.2021.30.1.010Kang W.H., J. Kim, H.I. Yoon, and J.E. Son 2020, Quantification of spectral perception of plants with light absorption of photoreceptors. Plants 9:556. doi:10.3390/plants9050556
10.3390/plants905055632349252PMC7285096Kim J.K., D.C. Jang, H.M. Kang, K.J. Nam, M.H. Lee, J.K. Na, and K.Y. Choi 2021, Effects of light intensity and electrical conductivity level on photosynthesis, growth and functional material contents of
Lactuca indica L. ‘Sunhyang’ in hydroponics. J Bio-Environment Control 30:1-9. doi:10.12791/KSBEC.2021.30.1.001
10.12791/KSBEC.2021.30.1.001Lamnatou C., and D. Chemisana 2013, Solar radiation manipulations and their role in greenhouse claddings: Fluorescent solar concentrators, photoselective and other materials. Renew Sustain Energy Rev 27:175-190. doi:10.1016/j.rser.2013.06.052
10.1016/j.rser.2013.06.052Lee J.E., Y.S. Shin, H.W. Do, J.D. Cheung, and Y.H. Kang 2016, Effect of seedling quality and growth after transplanting of Korean melon nursed under LED light sources and intensity. Prot Hortic Plant Fact 25:294-301. doi:10.12791/KSBEC.2016.25.4.294
10.12791/KSBEC.2016.25.4.294Lee S.-H., R.K. Tewari, E.-J. Hahn, and K.-Y. Paek 2007, Photon flux density and light quality induce changes in growth, stomatal development, photosynthesis and transpiration of
Withania Somnifera (L.) Dunal. plantlets. Plant Cell Tissue Organ Cult 90:141-151. doi:10.1007/s11240-006-9191-2
10.1007/s11240-006-9191-2Li Y., W. Tu, C. Liu, W. Liu, G. Hu, X. Liu, Z. Chen, and C. Yang 2017, Light conversion film promotes CO
2 assimilation by increasing cyclic electron flow around Photosystem I in
Arabidopsis thaliana. Int J Hydrogen Energy 42:8545-8553. doi:10.1016/j.ijhydene.2017.01.108
10.1016/j.ijhydene.2017.01.108Lobo F. de A., M.P. de Barros, H.J. Dalmagro, Â.C. Dalmolin, W.E. Pereira, É.C. de Souza, G.L. Vourlitis, and C.E. Rodríguez Ortíz 2013, Fitting net photosynthetic light-response curves with Microsoft Excel - A critical look at the models. Photosynthetica 51:445-456. doi:10.1007/s11099-013-0045-y
10.1007/s11099-013-0045-yLötscher M., and J. Nösberger 1997, Branch and root formation in Trifolium repens is influenced by the light environment of unfolded leaves. Oecologia 111:499-504. doi:10.1007/s004420050263
10.1007/s00442005026328308110McCree K.J. 1971, The action spectrum, absorptance and quantum yield of photosynthesis in crop plants. Agric Meteorol 9:191-216. doi:10.1016/0002-1571(71)90022-7
10.1016/0002-1571(71)90022-7Nishimura Y., Y. Fukumoto, H. Aruga, and Y. Shimoi 2009, Growth and developmental characteristics of vegetables grown under spectrum conversion film. Hortic Environ Biotechnol 50:416-421.
Park K.S., J.K. Kwon, D.K. Lee, and J.E. Son 2016, Microclimate and crop growth in the greenhouses covered with spectrum conversion films using different phosphor particle sizes. Prot Hortic Plant Fact 25:111-117. doi:10.12791/KSBEC.2016.25.2.111
10.12791/KSBEC.2016.25.2.111Ranwala N.K.D., D.R. Decoteau, A.P. Ranwala, and W.B. Miller 2002, Changes in soluble carbohydrates during phytochrome-regulated petiole elongation in watermelon seedlings. Plant Growth Regul 38:157-163. doi:10.1023/A:1021272902811
10.1023/A:1021272902811Schulze E.-D., E. Beck, N. Buchmann, S. Clemens, K. Müller-Hohenstein, and M. Scherer-Lorenzen 2019, Light. In: Plant Ecology. Springer, Berlin, Heidelberg, pp 57-90. doi:10.1007/978-3-662-56233-8_3
10.1007/978-3-662-56233-8_3Smith H. 2000, Phytochromes and light signal perception by plants - An emerging synthesis. Nature 407:585-591. doi:10.1038/35036500
10.1038/3503650011034200Son K.-H., and M.-M. Oh 2013, Leaf shape, growth, and antioxidant phenolic compounds of two lettuce cultivars grown under various combinations of blue and red light-emitting diodes. HortScience 48:988-995. doi:10.21273/HORTSCI.48.8.988
10.21273/HORTSCI.48.8.988Takenaka A. 1994, Effects of leaf blade narrowness and petiole length on the light capture efficiency of a shoot. Ecol Res 9:109-114. doi:10.1007/BF02347485
10.1007/BF02347485Yoon H.I., J.H. Kang, W.H. Kang, and J.E. Son 2020a, Subtle changes in solar radiation under a green-to-red conversion film affect the photosynthetic performance and chlorophyll fluorescence of sweet pepper. Photosynthetica 58:1107-1115. doi:10.32615/ps.2020.057
10.32615/ps.2020.057Yoon H.I., J.H. Kim, K.S. Park, J.W. Namgoong, T.G, Hwang, J.P. Kim, and J.E. Son 2020b, Quantitative methods for evaluating the conversion performance of spectrum conversion films and testing plant responses under simulated solar conditions. Hortic Environ Biotechnol 61:999-1009. doi:10.1007/s13580-020-00286-y
10.1007/s13580-020-00286-yZhang M., Y. Park, and E.S. Runkle 2020, Regulation of extension growth and flowering of seedlings by blue radiation and the red to far-red ratio of sole-source lighting. Sci Hortic 272:109478. doi:10.1016/j.scienta.2020.109478
10.1016/j.scienta.2020.109478







