서 론
재료 및 방법
1. 식물 재료 및 생육 조건
2. 백색광 LED 처리
3. 생장 분석
4. 통계 분석
결과 및 고찰
서 론
접목은 과채류 재배에 많이 사용되고 있으며, 토양성 전염병(Louws 등, 2010)을 방지하고 비생물적 스트레스에 내성이 있다고 보고되었으며(Kumar 등, 2015; Rouphael 등, 2016; Schwarz 등, 2010), 접목묘를 사용하여 재배할 경우 실생묘에 비해 수확량이 증가하였다(Oda, 1999; Yetisir와 Sari, 2003). 최근 접목묘 생산의 노동력과 접목에 소요되는 시간을 줄일 수 있는 접목 로봇이 개발되고 있다(Lee 등, 2010b; Xie 등, 2020). 접목 로봇을 이용할 경우 성공적인 접목을 위해 균일한 대목과 접수의 생산은 필수 적이다(Tian 등, 2017). 특히 배축장과 경경의 균일성은 접목의 효율성을 향상시킬 뿐만 아니라 활착률을 높인다(Jang 등, 2011; Suzuki 등, 1995).
광 환경 제어를 통한 과채류 묘의 생장 및 발달 조절 연구는 광도, 일장, 광질 등에서 활발히 이루어지고 있다(An 등, 2020; Hwang 등, 2020; Wang 등, 2009). 작물 생산을 위한 인공 광원으로 각광받고 있는 Light Emitting Diode(LED)는 설치가 쉽고 광질의 조절이 용이하다(Mitchell 등, 2015). 적색 및 청색의 단색광 LED는 원예작물 재배에 적용되고 있으며, 조합에 대한 연구가 수행되고 있다(Bula 등, 1991; Yorio 등, 2001). LED 광원을 사용하여 작물 재배 시, 적색광과 청색광의 혼합이 중요함을 알고 있지만 적색 및 청색 단독광 혹은 조합한 광원 만을 사용하여 작물을 재배할 경우 식물의 상태를 구별하기 어렵다는 단점이 있지만(Massa 등, 2008), 최근 식물의 생장 정도와 병해를 쉽게 감지할 수 있고, 색 온도에 따라 다양한 파장을 구현할 수 있는 백색 LED가 인공광을 이용한 식물공장에 널리 적용되고 있다(Lee 등, 2020). 기존 연구에 따르면 백색 LED 중 Cool white LED와 Warm white LED는 스펙트럼의 차이로 작물의 발달에 영향을 미친다고 알려졌다(Cope 등, 2014). Warm white와 Cool white 칩의 조합을 통해 작물의 재배에 적합한 bar type LED를 제작한다면 인공광원으로써 상용화가 수월할 것으로 판단한다. 따라서 본 연구는 warm white LED와 cool white LED칩의 비율에 따른 오이, 수박 및 고추의 대목 및 접수의 생육 반응을 확인하고, 균일한 묘 생산을 위한 bar type LED광원의 개발을 위해 수행되었다.
재료 및 방법
1. 식물 재료 및 생육 조건
오이 접수(Cucumis sativus cv. Joeunbaegdadagi, Seminis Korea, Seoul, Korea) 및 대목(Cucurbita ficifolia cv. Heukjong, Hungnong Seeds, Ansung, Korea), 수박 접수(Citrullus vulgaris cv. Sambokkul, Hungnong Seeds) 및 대목(Lagenaria siceraria cv. Bulrojangsaeng, Syngenta Korea, Seoul, Korea), 토마토 접수(Solanum lycopersicum cv. Dotaerangdia, Takii Korea, Seoul, Korea) 및 대목(S. lycopersicum cv. B-blocking, Takii Korea)의 종자를 128공 셀 트레이에 육묘용 상토(Bio Plug, Farm Hannong Co., Ltd., Seoul, Korea)를 충진 한 후 파종 하였고, 광원으로 LED를 사용하는 폐쇄형 육묘시스템에서 시험을 수행하였다. 발아 후 주야간 기온 27/22℃, 상대습도 60%, 일장 16h·d-1 조건에서 육묘하였다. CO2 농도는 및 600μmol·mol-1 였으며 2 또는 3일마다 한국 원시 양액 NO3-N 16.0, NH4-N 1.3, PO4-P 4.0, K 8.0, Mg 4.0, SO4-S 4.0me·L-1(Park과 Kim, 1998)을 pH 6.5, 전기 전도도(EC) 0.5-1.5dS∙m-1로 저면 관수 하였다.
2. 백색광 LED 처리
발아 후 광 처리를 시작하였으며, 처리구는 warm white LED 칩(AT533PKPNS, Dongbu LED Co., Ltd., Hwaseong, Korea)과 cool white LED 칩(AT533LDPN1, Dongbu LED Co., Ltd.)의 비율을 조절한 4가지 광원 W1C0(warm white), W1C1(warm white:cool white = 1:1), W3C1(warm white: cool white=3:1) 및 W5C2(warm white:cool white= 5:2)을 이용하였다. 광합성 유효 광량자속(PPFD)은 오이 100μmol·m-2·s-1, 수박과 토마토 250μmol·m-2·s-1로 설정하였으며, PPFD는 광 센서(LI-190R, LI-COR Inc., Lincoln, NE, USA) 및 일사계 센서(LI-200, LI-COR Inc.)를 일사량 측정기(LI-250A, LI-COR Inc.)에 결합하여 광원에서 20cm 거리에서 측정하였다.
3. 생장 분석
오이는 파종 후 7일, 수박은 파종 후 9일, 토마토는 파종 후 14일에 배축장, 경경, 엽수 엽면적 및 생체중을 측정하였다. 묘의 경경은 Vernier caliper(CD-20CPX, Mitutoyo Co., Kawasaki, Japan)를 사용하여 배축 가장 두꺼운 부분에서 측정하였고, 엽면적은 엽면적측정기(LI-3000, LI-COR Co., Inc.)를 이용하여 측정하였다.
4. 통계 분석
난괴법 3반복으로 각 12주의 생장 데이터를 SAS 윈도우 9.4버전(SAS Institute Inc., Cary, NC, USA)을 이용하여 p < 0.05에서 Duncan의 다중 범위 테스트를 사용하여 분석하였으며, 광원의 적색/청색 비율과 묘의 배축장 간의 회귀 분석을 실시하였다. 그래프는 sigmaplot 12.5(Systat Software, San Jose, CA, USA)를 사용하여 작성하였다.
결과 및 고찰
기존 bar type LED(2.0m)의 경우 가장자리의 PPFD가 평균보다 최소 70μmol·m-2·s-1 낮았다. 이 문제를 극복하기 위해 LED 칩의 밀도를 가장자리에 증가시킨 광원을 제작하였다(Fig. 1). 양쪽 630mm 부분의 칩 간격을 기존 17.5mm에서 13.2mm로 감소시켜 12개의 칩을 추가로 배치하였다. 광도 프로파일링의 결과, 250μmol·m-2·s-1조건에서 개선된 LED의 경우 가장자리의 PPFD가 30μmol·m-2·s-1이상 증가했으며, 표준 편차는 10μmol·m-2·s-1 이상 감소하였다(Fig. 2). Warm white 및 cool white 칩의 조합 처리에 따른 스펙트럼 분포와 적색(600-700nm)/청색(400-500nm) 및 적색/원적색(700-800nm) 비율의 차이를 분석하였다(Fig. 3, Table 1). Warm white chip의 비율이 높을 수록 적색광의 비율이 높았으며, 청색광의 비율이 감소하였고, W1C0 처리에서 적색/청색 비율이 가장 높았고(4.4), W1C1 처리에서 적색/청색 비율이 가장 낮았다(1.1). 시험에 사용된 광원의 적색/원적색 비율은 W1C0 처리에서 가장 낮았으며(4.5) W1C1 처리에서 가장 높았고(6.5), Holmes와 Smith(1977)의 보고와 비교했을 때 연구에 사용한 모든 처리구가 태양광의 적색/원적색 비율(0.6-1.3)에 비해 높았다. 상추의 경우 원적색광 보광에 의해 지상부 및 지하부의 생육이 증가한 연구 보고가 있었다(Lee 등, 2016).
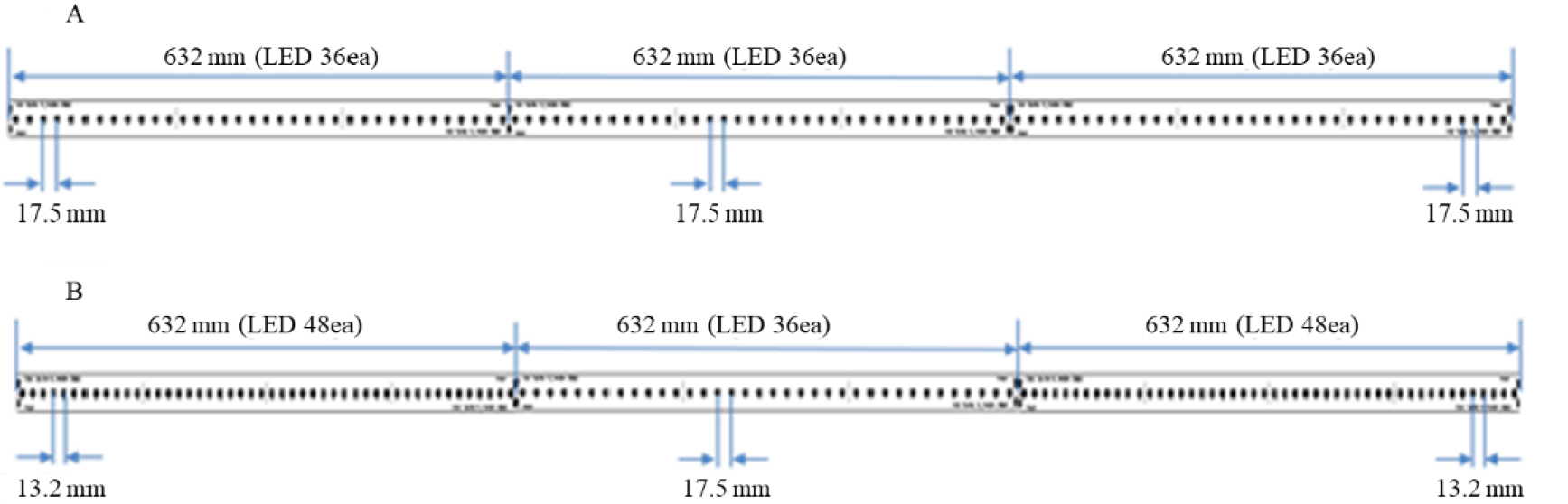
Fig. 1.
LED lamp design for improving light distribution. Previous (A) and improved (B) LED lamp design.
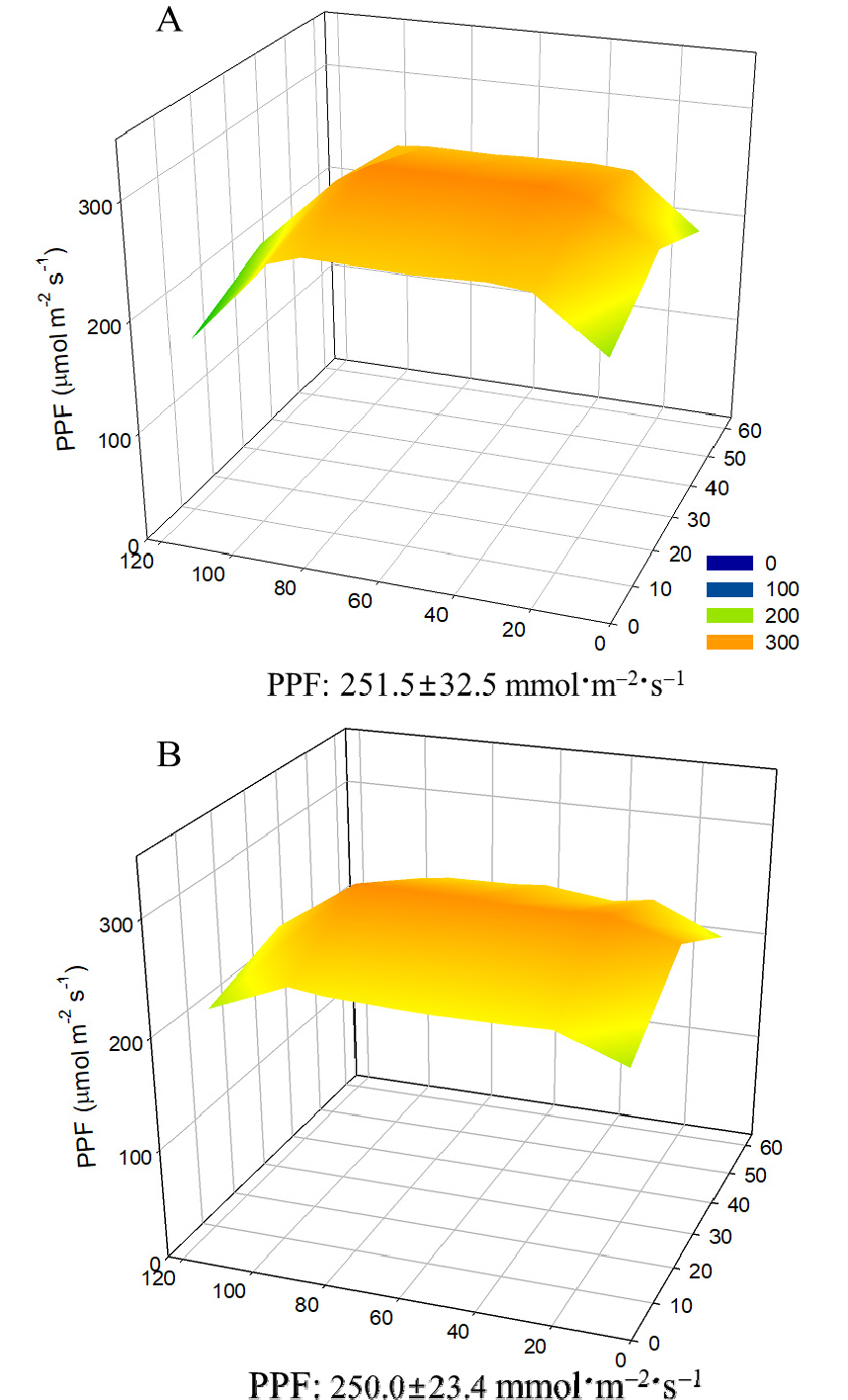
Fig. 2.
Light intensity distribution of previous (A) and improved (B) LEDs at 250 mol·m2·s1.
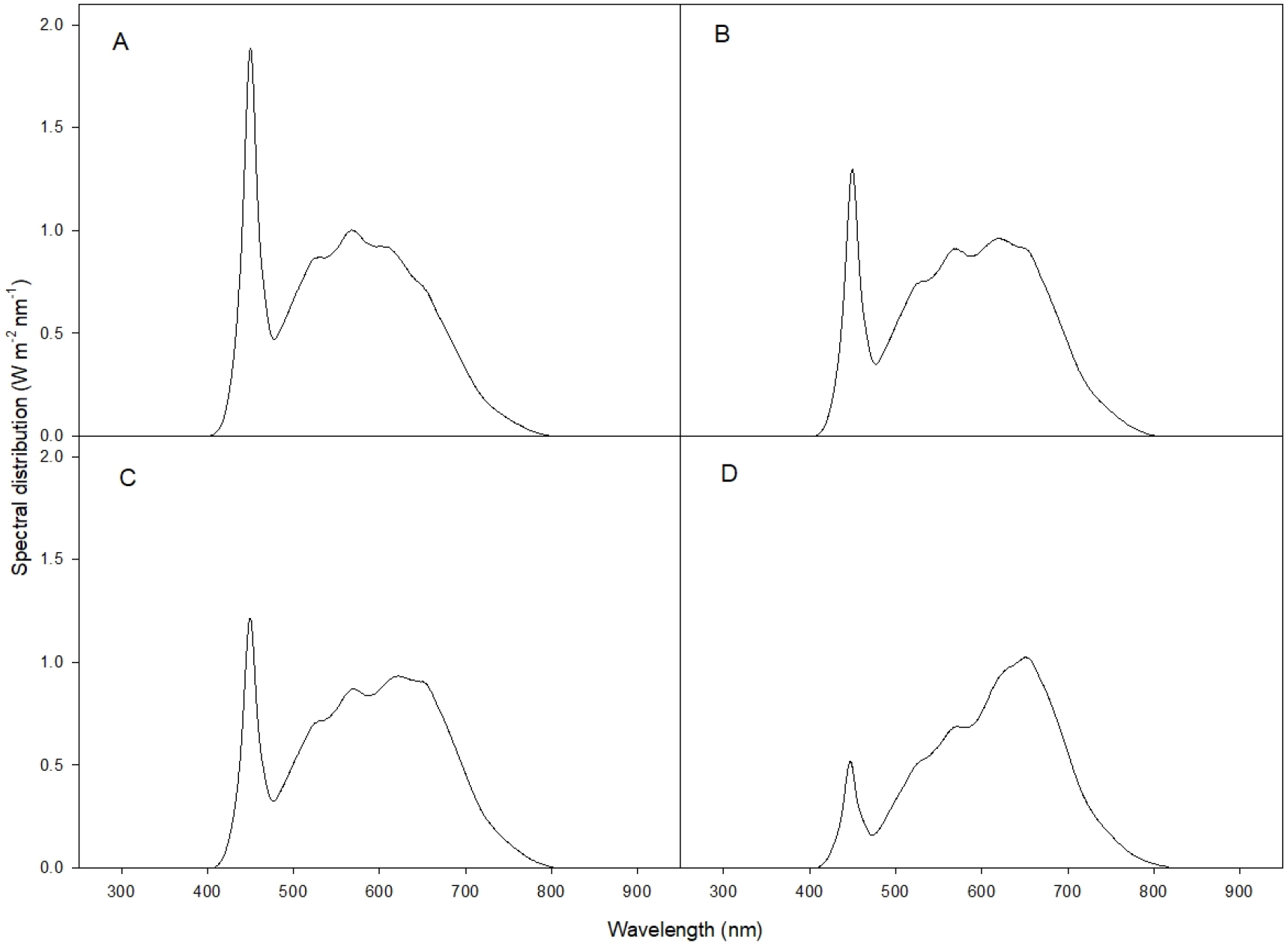
Fig. 3.
Spectral distribution of W1C1 (A), W5C2 (B), W3C1 (C), and W1C0 (D) LEDs. Spectral scans were conducted at the center of the tray with a light intensity at 250 μmol‧m-2‧s-1.
Table 1.
Light intensity of W1C1 (warm-white: cool-white=1: 1), W5C2 (warm-white: cool-white=5: 2), W3C1 (warm-white: cool-white=3: 1), and W1C0 (only warm-white) LEDs.
|
Plant
|
Treatment
|
PPFDz (μmol∙m-2∙s-1)
|
Red/blue
ratioy |
Red/Far-red
ratiox |
|
400-500 nm
|
500-600 nm
|
600-700 nm
|
700-800 nm
|
Total
|
|
Cucumber
|
W1C1
|
27.0 ± 1.4
|
38.4 ± 2.0
|
29.8 ± 1.5
|
4.6 ± 0.2
|
99.8 ± 5.1
|
1.1
|
6.5
|
|
W5C2
|
19.8 ± 1.3
|
34.8 ± 2.2
|
36.2 ± 2.3
|
6.6 ± 0.4
|
97.4 ± 6.2
|
1.8
|
5.5
|
|
W3C1
|
19.7 ± 1.1
|
35.7 ± 2.0
|
38.4 ± 2.2
|
7.2 ± 0.4
|
101.1 ± 5.7
|
1.9
|
5.3
|
|
W1C0
|
10.9 ± 0.4
|
31.4 ± 1.1
|
47.9 ± 1.7
|
10.7 ± 0.4
|
100.9 ± 3.6
|
4.4
|
4.5
|
Watermelon and
tomato
|
W1C1
|
69.1 ± 3.4
|
98.3 ± 4.8
|
76.2 ± 3.8
|
11.7 ± 0.6
|
255.3 ± 12.6
|
1.1
|
6.5
|
|
W5C2
|
50.9 ± 2.9
|
89.7 ± 5.2
|
93.1 ± 5.4
|
17.1 ± 1.0
|
250.7 ± 14.5
|
1.8
|
5.4
|
|
W3C1
|
49.1 ± 2.2
|
88.9 ± 4.1
|
95.5 ± 4.4
|
18.0 ± 0.8
|
251.5 ± 11.5
|
1.9
|
5.3
|
|
W1C0
|
26.9 ± 1.1
|
77.6 ± 3.3
|
118.2 ± 5.0
|
26.4 ± 1.1
|
249.1 ± 10.5
|
4.4
|
4.5
|
세 작물 모두, 대목의 엽면적은 광질 처리에 따른 유의적인 차이가 보이지 않았다. 오이 접수와 수박 접수 엽면적은 청색광 비율이 가장 높은 W1C1 처리구에서 가장 낮았다(Table 2). 이전 상추의 연구에서도 적색광과 청색광 혼합 처리 시, 적색광의 비율이 높을수록 엽면적은 증가하였다(Lee 등, 2010a). 무와 콩의 경우에도 청색광의 비율이 증가할수록 엽면적은 감소하는 연구결과가 보고되었다(Cope와 Bugbee, 2013). 백색 LED의 적색광 청색광의 비율 조정을 통해 엽면적은 조절이 가능할 것으로 판단한다.
Table 2.
Growth of cucumber scions and rootstocks at 7 days after sowing (DAS), watermelon scions and rootstocks at 9 DAS, and tomato scions and rootstocks at 14 DAS under different LED lights.
|
Plant
|
Treatment
|
Hypocotyl length
(cm)
|
Leaf area
(cm2)
|
Stem diameter
(mm)
|
Shoot FW
(g/plant)
|
Root FW
(g/plant)
|
Cucumber
(scion)
|
W1C1
|
3.03 c
|
10.31 b
|
1.69 a
|
0.42 b
|
0.05 c
|
|
W5C2
|
3.47 bc
|
11.72 a
|
1.75 a
|
0.47 ab
|
0.09 a
|
|
W3C1
|
3.80 ab
|
11.03 ab
|
1.63 a
|
0.46 ab
|
0.07 b
|
|
W1C0
|
4.37 az |
11.00 ab
|
1.80 a
|
0.48 a
|
0.07 b
|
Cucumber
(rootstock)
|
W1C1
|
6.05 b
|
19.93 a
|
3.08 a
|
1.69 b
|
0.35 a
|
|
W5C2
|
6.77 a
|
15.92 a
|
2.91 a
|
2.06 a
|
0.40 a
|
|
W3C1
|
6.65 a
|
18.53 a
|
2.93 a
|
1.78 b
|
0.35 a
|
|
W1C0
|
6.85 a
|
19.19 a
|
2.91 a
|
1.80 b
|
0.34 a
|
Watermelon
(scion)
|
W1C1
|
4.78 c
|
8.24 b
|
1.72 a
|
0.60 b
|
0.29 a
|
|
W5C2
|
5.68 b
|
9.32 ab
|
1.81 a
|
0.67 ab
|
0.12 a
|
|
W3C1
|
5.23 bc
|
10.48 a
|
1.88 a
|
0.72 a
|
0.14 a
|
|
W1C0
|
6.85 a
|
8.67 b
|
2.03 a
|
0.74 a
|
0.09 a
|
Watermelon
(rootstock)
|
W1C1
|
5.45 c
|
10.22 a
|
2.48 b
|
0.98 c
|
0.23 a
|
|
W5C2
|
6.55 b
|
10.85 a
|
2.46 b
|
1.18 ab
|
0.26 a
|
|
W3C1
|
6.52 b
|
11.24 a
|
2.53 b
|
1.11 b
|
0.24 a
|
|
W1C0
|
7.52 a
|
11.70 a
|
2.83 a
|
1.23 a
|
0.25 a
|
Tomato
(scion)
|
W1C1
|
3.80 c
|
5.60 a
|
1.48 b
|
0.42 a
|
0.05 a
|
|
W5C2
|
4.08 c
|
5.41 a
|
1.52 b
|
0.42 a
|
0.05 a
|
|
W3C1
|
4.75 b
|
5.31 a
|
1.60 b
|
0.45 a
|
0.05 a
|
|
W1C0
|
5.23 a
|
6.44 a
|
1.79 a
|
0.50 a
|
0.04 a
|
Tomato
(rootstock)
|
W1C1
|
3.45 c
|
5.49 a
|
1.41 b
|
0.39 a
|
0.04 a
|
|
W5C2
|
4.25 b
|
5.83 a
|
1.55 b
|
0.43 a
|
0.03 a
|
|
W3C1
|
4.18 b
|
5.80 a
|
1.55 b
|
0.42 a
|
0.05 a
|
|
W1C0
|
4.67 a
|
5.53 a
|
1.64 a
|
0.40 a
|
0.04 a
|
오이 접수와 대목, 수박의 접수의 경경은 처리에 따른 유의적인 차이를 보이지 않았으나, 수박 대목, 토마토 접수와 대목의 경경은 가장 작았던 W1C1처리구에 비해 W1C0 처리가 14%, 21% 및 16% 더 컸다. Chen 등(2014)은 파종 후 50일 상추의 경경이 적색광 단독 처리구에서 청색광 및 적색광/청색광 혼합처리에 비해 각각 20와 54% 증가함을 보고하였다. W1C1처리구의 경경이 컸던 이유는 청색광의 비율이 나머지 처리에 비해 낮았기 때문이라 판단한다.

Fig. 4.
Seedlings of cucumber scions (A) and rootstocks (B) at 7 days after sowing (DAS), watermelon scions (C) and rootstocks (D) at 9 DAS, and tomato scions (E) and rootstocks (F) at 14 DAS under different LED lights.
수박 접수와 대목의 생체중은 적색광 비율이 가장 높은 W1C0처리구에서 가장 컸다. 오이 접수를 제외한 나머지 작물에서 광질에 따른 뿌리 생체중은 유의적인 차이를 보이지 않았다. 오이 접수의 생체중은 청색광 비율이 높은 W1C1에서 가장 낮았다. 적색/청색 비율에 따른 작물의 반응은 재배 단계별 영향을 크게 받을 수 있으며(Chen 등, 2014; Lee 등, 2010a), 청색광의 광도와 비율의 영향을 동시에 확인한 Cope와 Bugbee(2013)의 연구결과에 따르면 청색광에 의한 엽면적 감소 효과와 동시에 발생하는 수광 효율의 증가 때문에 생육량의 증진 효과는 크게 나타나지 않을 수 있다.
이번 연구에서 오이, 수박 및 토마토 묘의 배축장은 적색/청색 비율이 1.1에서 4.4로 증가할 수록 길어졌으며 R2값이 0.9 이상이었다(Fig. 5). 수박의 경우 적색/청색 비율에 따른 접수와 대목의 회귀선 기울기는 다른 작물에 비해 높았으며, 그 값은 각각 1.45와 1.50이었다. 적색/청색 비율과 배축 길이의 회귀 곡선 기울기는 양수였으며, 적색/청색 비율이 증가할수록 오이 접수와 토마토 대목을 제외한 모든 시험구에서 배축장이 증가하는 것으로 나타났다. 이러한 결과는 배축 신장 억제에 영향을 미치는 cool white LED의 효과로 판단한다. 식물의 청색광 수용체인 크립토크롬은 N-말단과 C-말단 도메인으로 나뉘며 N-말단 도메인은 청색광 신호전달을 담당하는 반면, C-말단 도메인은 발색단에 결합하고 CRY 탈이체화를 매개한다(Yang 등, 2000). 아라비돕시스에서 CRY1 도메인의 N-말단은 청색광에 대한 반응에서 배축 신장의 억제를 매개한다고 보고되었다(He 등, 2015). Hernández와 Kubota(2016)의 연구에 따르면 오이의 배축장은 청색광 단독광 처리가 적색광 단독광에 비해 69% 증가하였고, 적색광 단독처리구가 75%청색광 25% 적색광 혼합처리에 비해 164% 증가하였다. 이번 연구에서, 단독광이 아닌 백색 LED내에서도 적색광의 비율이 높아질수록 배축장은 증가하는 것을 확인할 수 있었다.
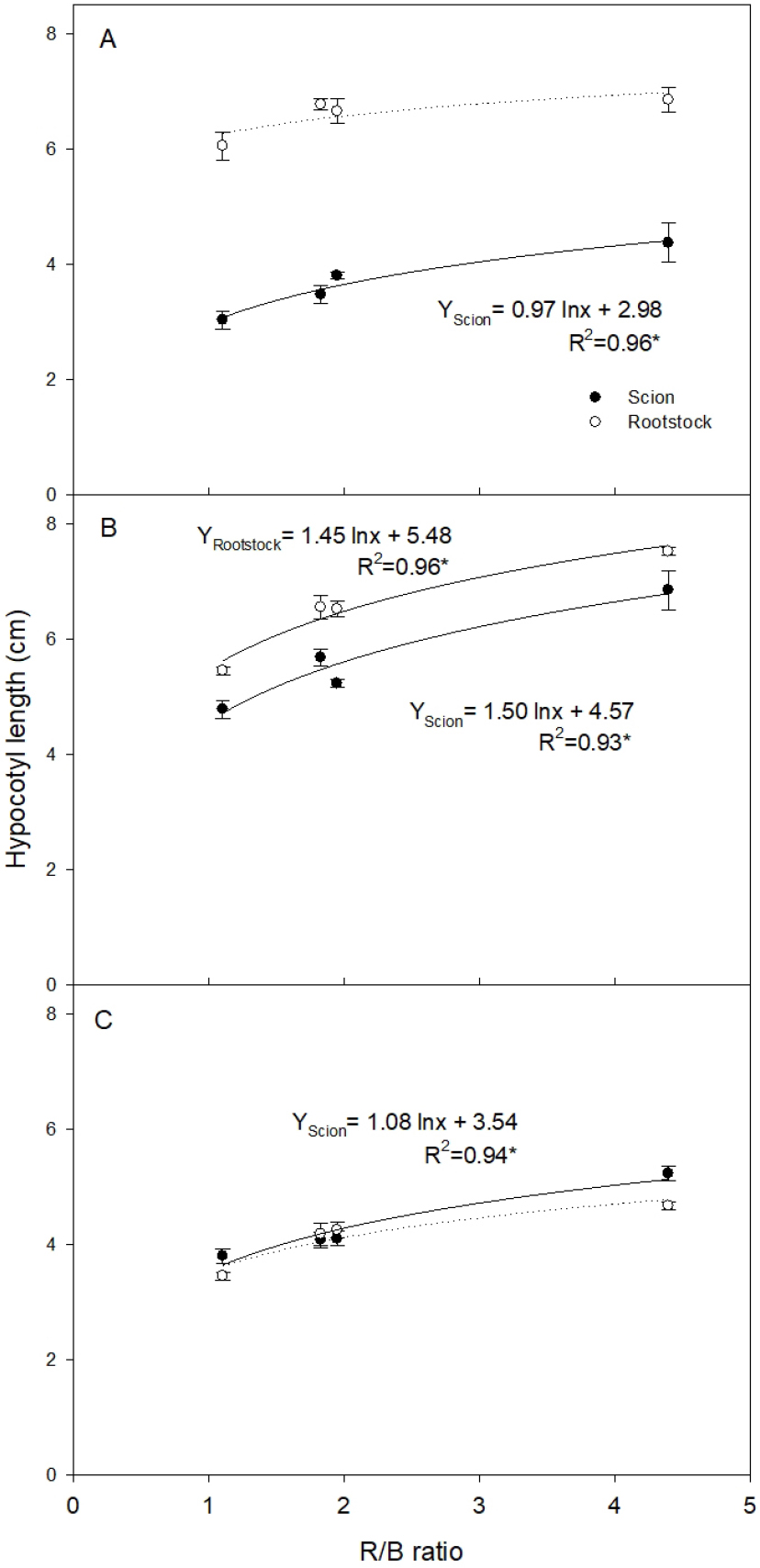
Fig. 5.
Hypocotyl lengths of cucumber scions and rootstocks (A) at 7 days after sowing (DAS), watermelon scions and rootstocks (B) at 9 DAS, tomato scions and rootstocks (C) at 14 DAS under different LED lights.
백색 LED의 광 스펙트럼 차이는 과채류 묘의 경경, 생체중, 엽면적에 영향을 주었지만 작물에 따라 그 변화가 다양하여 뚜렷한 경향을 보이지 않은 반면 배축장은 R/B ratio가 낮아질수록 짧아졌다. 본 연구의 결과를 통해 광원의 재배치를 통해 균일한 광도를 얻을 수 있었고, warm white LED와 cool white LED의 조합 비율을 조절하여 원하는 배축장을 갖는 대목과 접수의 생산이 가능하리라 판단한다.
Acknowledgements
본 연구는 농촌진흥청 연구사업 “접목 로봇에 적합한 과채류 접수 및 대목 규격묘 생산을 위한 적정 광 환경 구명 및 식물공장형 육묘시스템 개발”(PJ013840)의 지원에 의해 이루어진 것임.
References
An S., S.W. Park, and Y. Kwack 2020, Growth of cucumber scions, rootstocks, and grafted seedlings as affected by different irrigation regimes during cultivation of 'joenbaekdadagi' and 'heukjong' seedlings in a plant factory with artificial lighting. Agronomy 10:1943. doi:10.3390/agronomy10121943
10.3390/agronomy10121943Bula R., R. Morrow, T. Tibbitts, D. Barta, R. Ignatius, and T. Martin 1991, Light-emitting diodes as a radiation source for plants. HortScience 26:203-205. doi:10.21273/HORTSCI.26.2.203
10.21273/HORTSCI.26.2.20311537727Chen X.L., W.Z. Guo, X.Z. Xue, L.C. Wang, and X.J. Qiao 2014, Growth and quality responses of 'Green Oak Leaf' lettuce as affected by monochromic or mixed radiation provided by fluorescent lamp (FL) and light-emitting diode (LED). Sci Hortic 172:168-175. doi:10.1016/j.scienta.2014.04.009
10.1016/j.scienta.2014.04.009Cope K.R., and B. Bugbee 2013, Spectral effects of three types of white light-emitting diodes on plant growth and development: absolute versus relative amounts of blue light. HortScience 48:504-509. doi:10.21273/HORTSCI.48.4.504
10.21273/HORTSCI.48.4.504Cope K.R., M.C. Snowden, and B. Bugbee 2014, Photobiological interactions of blue light and photosynthetic photon flux: Effects of monochromatic and broad‐spectrum light sources. J Photochem Photobiol 90:574-584. doi:10.1111/php.12233
10.1111/php.1223324372324He S.B., W.X. Wang, J.Y. Zhang, F. Xu, H.L. Lian, L. Li, and H.Q. Yang 2015, The CNT1 domain of
Arabidopsis CRY1 alone is sufficient to mediate blue light inhibition of hypocotyl elongation. Mol Plant 8:822-825. doi:10.1016/j.molp.2015.02.008
10.1016/j.molp.2015.02.00825721730Hernández R., and C. Kubota 2016, Physiological responses of cucumber seedlings under different blue and red photon flux ratios using LEDs. Environ Exp Bot 121:66-74. doi:10.1016/j.envexpbot.2015.04.001
10.1016/j.envexpbot.2015.04.001Holmes M.G., and H. Smith 1977, The function of phytochrome in the natural environment-I. Characterization of daylight for studies in photomorphogenesis and photoperiodism. Photochem Photobiol 25:533-538. doi:10.1111/j.1751-1097.1977.tb09124.x
10.1111/j.1751-1097.1977.tb09124.xHwang H., S. An, M.D. Pham, M. Cui, and C. Chun 2020, The combined conditions of photoperiod, light intensity, and air temperature control the growth and development of tomato and red pepper seedlings in a closed transplant production system. Sustainability 12:9939. doi:10.3390/su12239939
10.3390/su12239939Jang Y., E. Goto, Y. Ishigami, B. Mun, and C. Chun 2011, Effects of light intensity and relative humidity on photosynthesis, growth and graft-take of grafted cucumber seedlings during healing and acclimatization. Hort Environ Biotechnol 52:331-338. doi:10.1007/s13580-011-0009-8
10.1007/s13580-011-0009-8Kumar P., L. Lucini, Y. Rouphael, M. Cardarelli, R.M. Kalunke, and G. Colla 2015, Insight into the role of grafting and arbuscular mycorrhiza on cadmium stress tolerance in tomato. Front Plant Sci 6:477. doi:10.3389/fpls.2015.00477
10.3389/fpls.2015.00477Lee H., S.W. Park, M.D. Pham, H. Hwang, and C. Chun 2020, Effect of the light spectrum of white LEDs on the productivity of strawberry transplants in a plant factory with artificial lighting. Hort Environ Biotechnol 61:971-979. doi:10.1007/s13580-020-00284-0
10.1007/s13580-020-00284-0Lee J.G., S.S. Oh, S.H. Cha, Y.A. Jang, S.Y. Kim, Y.C. Um, and S.R. Cheong 2010a, Effect of red/blue light ratio and short-term light quality conversion on growth and anthocyanin. J Bio-Env Con 19:351-359. (in Korean)
Lee J.M., C. Kubota, S.J. Tsao, Z. Bie, P.H. Echevarria, L. Morra, and M. Oda 2010b, Current status of vegetable grafting: diffusion, grafting techniques, automation. Sci Hortic 127: 93-105. doi:10.1016/j.scienta.2010.08.003
10.1016/j.scienta.2010.08.003Lee M.J., K.H. Son, and M.M. Oh 2016, Increase in biomass and bioactive compounds in lettuce under various ratios of red to far-red LED light supplemented with blue LED light. Hort Environ Biotechnol 57:139-147. doi:10.1007/s13580-016-0133-6
10.1007/s13580-016-0133-6Louws F.J., C.L. Rivard, and C. Kubota 2010, Grafting fruiting vegetables to manage soilborne pathogens, foliar pathogens, arthropods, and weeds. Sci Hortic 127:127-146. doi:10.1016/j.scienta.2010.09.023
10.1016/j.scienta.2010.09.023Massa G.D., H.H. Kim, R.M. Wheeler, and C.A. Mitchell 2008, Plant productivity in response to LED lighting. HortScience 43:1951-1956. doi:10.21273/HORTSCI.43.7.1951
10.21273/HORTSCI.43.7.1951Mitchell C.A., M.P. Dzakovich, C. Gomez, R. Lopez, J.F. Burr, R. Hernández, C. Kubota, C.J. Currey, Q. Meng, E.S. Runkle, C.M. Bourget, R.C. Morrow, and A.J. Both 2015, Light-emitting diodes in horticulture. Hortic Rev 43:1-87. doi:10.1002/9781119107781.ch01
10.1002/9781119107781.ch01Oda M. 1999, Grafting of vegetables to improve greenhouse production. Ext Bul 480:1-11
Park K.W., and Y.S. Kim 1998, Hydroponics in horticulture. Academybook, Seoul, Korea, pp 76-90.
Rouphael Y., E. Rea, M. Cardarelli, M. Bitterlich, D. Schwarz, and G. Colla 2016, Can adverse effects of acidity and aluminum toxicity be alleviated by appropriate rootstock selection in cucumber? Front Plant Sci 7:1283. doi:10.3389/fpls.2016.01283
10.3389/fpls.2016.01283Schwarz D., Y. Rouphael, G. Colla, and J.H. Venema 2010, Grafting as a tool to improve tolerance of vegetables to abiotic stresses: thermal stress, water stress, and organic pollutants. Sci Hortic 127:162-171. doi:10.1016/j.scienta.2010.09.016
10.1016/j.scienta.2010.09.016Suzuki M., K. Kobayashi, K. Inooku, K. Miura, and K. Hirata 1995, Development of grafting robot for cucurbitaceous vegetables (Part 1). J Jpn Soc Agric Mach 57:67-76. (in Japanese) doi:10.11357/jsam1937.57.2_67
10.11357/jsam1937.57.2_67Tian S., Z. Wang, J. Yang, Z. Huang, R. Wang, L. Wang, and J. Dong 2017, Development of an automatic visual grading system for grafting seedlings. Adv Mech Eng 9:1-12. doi:10.1177/1687814016686265
10.1177/1687814016686265Wang H., M. Gu, J.X. Cui, K. Shi, Y.H. Zhou, and J.Q. Yu 2009, Effects of light quality on CO
2 assimilation, chlorophyll-fluorescence quenching, expression of Calvin cycle genes, and carbohydrate accumulation in
Cucumis sativus. J Photochem Photobiol B 96:30-37. doi:10.1016/j.jphotobiol.2009.03.010
10.1016/j.jphotobiol.2009.03.01019410482Xie Z., S. Gu, Q. Chu, B. Li, K. Fan, Y. Yang, Y. Yang, and X. Liu 2020, Development of a high-productivity grafting robot for Solanaceae. Int J Agric & Biol Eng 13:82-90. doi:10.25165/j.ijabe.20201301.5209
10.25165/j.ijabe.20201301.5209Yang H.Q., Y.J. Wu, R.H. Tang, D. Liu, Y. Liu, and A.R. Cashmore 2000, The C termini of
Arabidopsis cryptochromes mediate a constitutive light response. Cell 103:815-827. doi:10.1016/S0092-8674(00)00184-7
10.1016/S0092-8674(00)00184-7Yetisir H., and N. Sari 2003, Effect of different rootstock on plant growth, yield, and quality of watermelon. Austral J Exp Agric 43:1269-1274. doi:10.1071/EA02095
10.1071/EA02095Yorio N.C., G.D. Goins, H.R. Kagie, R.M. Wheeler, and J.C. Sager 2001, Improving spinach, radish, and lettuce growth under red light-emitting diodes (LEDs) with blue light supplementation. HortScience 36:380-383. doi:10.21273/HORTSCI.36.2.380
10.21273/HORTSCI.36.2.38012542027








