서 론
재료 및 방법
1. 실험 재료 및 재배 환경
2. 부정근 조사
3. 통계분석
결과 및 고찰
1. 부정근 발생
2. 부정근의 개수 및 길이
서 론
지구온난화는 대기 중의 이산화탄소의 농도가 높아지면서 발생하는 현상으로 홍수, 가뭄, 사막화, 해수면 상승 등 기후변화의 주 원인이다(Cho 등, 2013; Kim 등, 2021). 지구온난화 현상 중 하나인 사막화는 건조·반건조·건조아습윤 지역에서 기후변화와 인간의 활동 등 자연적, 인위적인 요소가 요인으로 작용하여 토지가 황폐화되는 것을 의미한다(Rubio와 Bochet, 1998; Vendruscolo 등, 2021). 사막화로 인해 매년 약 423억 달러의 직접적인 경제적 손실이 발생하고(Shili 등, 2006), 사회적으로 사막화를 막기 위한 토양개량(Wezel와 Rath, 2002), 태양열 관개용수 기술(Burney 등, 2010), 식물 식재로 바람에 의한 침식 예방(Michels 등, 1998) 등 많은 방법을 이용하여 문제를 해결하기 위해 세계적으로 연구가 이루어지고 있다(D’Odorico 등, 2013; Yang 등, 2005). 다양한 대안책으로 제시된 방법 중 하나인 생물공학적 녹화 공법(revegetation technology of biological engineering)은 식물 뿌리의 재생력 및 저항력을 이용하여 토양 침식과 토양 속 수분의 증발을 억제시켜 생태계 유지 및 야생동물의 서식처를 제공하는 것을 목적으로 하고 있다(Cha 등, 2008; Kim와 Lee, 1998). 특히, 사막화 방지를 위한 식물로 목본류를 사용하면 바람으로부터 견디는 힘이 좋고, 뿌리의 생장이 빨라 방풍림을 조성하거나 토양침식을 예방할 수 있어 생물공학적 녹화 공법 중 하나로 이용되고 있다(Jeong와 Lee, 2020; Kim와 Lee, 1999). 대량으로 녹화공법을 수행하기 위해서는 대상 작물의 영양번식체인 삽수에 대한 초기 부정근의 발달 정도는 삽수 수확기나 삽수의 생육에 큰 차이를 유발 시킬 수 있기 때문에 매우 중요한 과정이라고 할 수 있다(Buwalda 등, 1995).
버드나무(Salix koreensis)는 버드나무과(Salicaceae)에 속하는 낙엽 활엽교목으로 전세계에 약 300-500종이 분포하고 있다(Lee 등, 2001; Yun 등, 2016). 환경 적응력이 뛰어나 영하의 온도인 북극 지역뿐만 아니라 아열대부터 온대 기후지역까지 널리 번식하고 있으며, 정착되면 빠르게 성장하고 다양한 환경에 내성을 지니고 있다(Argus, 1986; Kuzovkina와 Quigley, 2005). 버드나무과 식물은 탄화수소(hydrocarbon), 염소화 복합물(chlorinated compound) 및 니트로방향족(nitroaromatics)을 포함한 금속, 준금속, 방사성 폐기물 및 농약으로 인해 오염된 토양을 정화할 수 있다(Pulford 등, 2002; Roy 등, 2005; Stoltz와 Greger, 2002; Vandecasteele 등, 2005; Watson 등, 2003; Yergeau 등, 2018). 버드나무과 식물은 목본류 중에서 근권부 생장속도가 빠르고, 줄기 길이와 직경, 줄기 수, 목재 밀도 등 성장요소와 관련된 바이오매스 생산량이 많은 장점으로 토지 개간, 토양 정화, 산림의 녹화공법 분야에 사용된다(Chae 등, 2020; Kuzovkina와 Volk, 2009).
3개의 산소원자로 이루어진 오존(O3)은 공기와 전기적인 힘이 반응하여 생성되는 물질로 활성산소종(reactive oxygen species, ROS)으로도 알려져 있다(Behzadi 등, 2012; Kim 등, 2008). 오존은 자연계에 존재하는 원소 중 불소 다음으로 강력한 산화제로 박테리아 제거(Kim 등, 2020; Koseki와 Isobe, 2006), 바이러스 파괴(Ebihara 등, 2011) 등 처리 효과를 나타낸다(Kim 등, 2008). 부정근의 발생 및 뿌리 발육은 오옥신과 같은 호르몬의 불균형뿐만 아니라 상처나 스트레스에 기인하여 촉진된다(Gaspar 등, 1997). 또한 과산화수소나 GABA(g-aminobutyric acid)와 같은 외생적 화합물은 오옥신이 없는 상태에서도 줄기로 부터 부정근의 발달을 촉진할 수 있다고 하였다(Gaspar 등, 2002; Hausman 등, 1997). 산화적 스트레스를 유발시키는 과산화수소(H2O2)와 O2-, 하이드록시 라디칼(OH-) 등은 오존의 분해과정에서 발생되는 활성산소종으로(Somiya, 2004) 물속에 용해된 오존은 버드나무 삽수의 부정근 발달을 유도할 수 있을 것이다. 그동안 오존수를 사용하여 식물 생장 및 국화삽수의 부정근 촉진에 대한(Ishii 등, 2021; Park 등, 2009) 연구들이 발표되었지만, 목본류 삽수의 발근과 처리시간 및 농도에 대한 연구는 보고된 바가 없다. 따라서 본 연구에서는 오존수를 농도 및 처리시간에 따라 버드나무의 삽수의 부정근 발근에 미치는 영향을 구명하고자 수행되었다.
재료 및 방법
1. 실험 재료 및 재배 환경
오존수 농도 및 침지처리 시간에 따른 버드나무 삽수의 부정근 발생에 관한 연구를 위해, 정아가 있는 버드나무(Salix koreensis) 삽수 540개를 세종시 수복나무시장에서 구매하였다. 그 중 삽수의 길이가 9-10cm, 두께가 0.5cm와 유사한 180개를 실험에 이용하였다. 오존발생기(Weco Co. Ltd., WOW-030-CN, Korea)를 이용하여 생성된 오존수를 반응조에서 500ml 비커에 담아서 용존 오존 농도를 오존수 농도 측정기(Okitrotec Co. Ltd., OZM-7000LN, Japan)를 이용하여 측정하였다. 용존 오존농도 1, 5, 10, 20ppm을 500ml 유리 비커에 담아 삽수 30개씩 5분 혹은 2시간 동안 침지시켰으며, 수돗물 침지처리를 대조구로 두었다. 오존수 및 수돗물 침지처리한 삽수는 원예용 상토(Bogeumjari, Nongwoobio Co., Ltd., Korea)를 채운 60공 플러그 트레이에 깊이 4cm로 식재하였다. 습도 유지를 위하여 각 플러그 트레이의 꼭짓점에 나무로 만든 대를 세우고 랩을 씌웠으며 직경 2cm 크기의 구멍을 뚫어 포화 수증기압 조건에 도달하지 않도록 하였다. 부정근 발근 처리실의 재배환경은 온도 23 ± 1℃, 습도 70 ± 10%, CO2 600 ± 100mol·mol-1 조건으로 설정하여 4주간 유지 하였으며, 적색, 청색 LED 칩(PCL-D9BBN10SC, Powerlight Co. Ltd., Korea), 백색 LED 칩(H9WCN10SC, Powerlight Co, Ltd., Korea)으로 구성된 백색 광원(Red:Blue:Green = 2:1:1-PPFD기준)을 이용하여 광 강도 80 ± 8μmol·m-2·s-1 의 광강도와 주야간 12h/12h씩 광조사하여 4주간 버드나무 삽수의 부정근 발근을 진행하였다. 삽수 근권부의 pH와 EC의 변화를 줄이기 위해 매일 오전 10시에 수돗물로 5분간 저면관수하였다.
2. 부정근 조사
삽수의 부정근 발육 조사를 위해 식재 후 2, 3, 4주차에 각 처리구당 버드나무 삽수 5주를 무작위로 수확하여 분석하였다. 버드나무 삽수의 부정근 개수 및 길이를 측정하였으며 부정근의 길이는 캘리퍼스(SD500-300PRO, Shin Con CO. Ltd., Korea)를 이용하여 측정하였다.
3. 통계분석
실험은 완전임의배치법으로 설계하여 2반복으로 실시하였으며, 측정 데이터의 통계분석은 처리구별 평균 간 비교를 위해 SPSS 프로그램(SPSS Statistic 26, IBM Co. Ltd., USA)을 사용하여 ANOVA 변량분석을 수행하였으며, 평균간 유의성 검증을 위해 Duncan의 다중검정법으로 유의수준 p ≤ 0.05에서 분석하였다.
결과 및 고찰
1. 부정근 발생
식재 후 4주차에 버드나무의 외관을 관찰한 결과 오존수 5분간 침지처리구의 경우, 대조구 및 오존수 처리농도가 낮은 1과 5ppm에서 형태학적으로 부정근 발근 및 생육이 저조하였다(Fig. 1). 오존수 농도 10, 15, 20ppm으로 처리된 삽수는 4주차가 되었을 때 지상부 생장점에서 측지의 발달이 이루어진 모습을 확인할 수 있었다. 수돗물에 침지한 대조구의 삽수는 부정근 발근이 잘 이루어지지 않았고, 생장점에서 측지가 발생한 개체는 1개 였으며, 이는 오존수 1ppm 처리한 삽수와 동일하였다. 2시간 침지처리한 결과 5, 10ppm 처리한 삽수의 부정근 발생이 잘 이루어지고 지상부에서 측지가 1-2개 발생한 대조구와 1ppm 처리구에 비해 잘 발달된 모습을 나타내었다(Fig. 2). 그러나, 15와 20ppm 농도로 침지처리한 삽수의 부정근은 발생되지 않았고, 지상부 생장점에서 측지는 발생하였지만, 잎 표면의 손상과 고사를 관찰할 수 있었다.

Fig. 1.
Photos of Salix koreensis grown in different ozonated water concentration treatments for 4 weeks after 5 minutes.

Fig. 2.
Photos of Salix koreensis grown in different ozonated water concentration treatments for 4 weeks after 2 hours.
오존수 수중에 용존된 O3는 기화되는데, 대기 중의 오존은 식물 잎을 통해 들어와 기공을 폐쇄하여 잎의 노화를 촉진하거나 갈변의 원인이 되며(Paoletti와 Grulke, 2005; Sandermann Jr, 1996; Wang 등, 2016), 뿌리 바이오매스를 감소시켜 지상부 생장에 영향을 준다고 보고되었다(Grantz 등, 2006; Mrak 등, 2019). 2시간 침지한 실험에서 지상부 생장이 저하되고 4주차에 잎이 괴사한(Fig. 3) 것은 오존수 처리중에 기화되는 오존 가스에 노출되어 발생한 현상으로 사료된다. 오존을 식물에 처리할 경우 에틸렌의 생산 속도가 촉진되고(Craker, 1971), IAA 생합성 유전자의 발현에 영향을 끼쳐 뿌리 생장점의 IAA 함량을 증가시켜 근권 생장 촉진시키며(Strader 등, 2010), 뿌리 세포와 오존의 직접적인 상호작용의 부산물로 방어기작에 의해 세포를 증식시켜 뿌리 발생 및 길이가 증가한다고 보고되었다(Iizuka와 Saito, 2016). 또한, 오존의 자가분해로 인해 용존산소의 농도가 높아지고 뿌리의 호흡을 자극해 물과 미네랄 영양소 흡수의 증가로 인해 식물 생장에 긍정적인 영향을 미치고 품질과 수확량을 향상시킬 수 있다는 연구가 수행되었다(Ohashi-Kaneko 등, 2009; Park 등, 2009). 부정근 발생은 뿌리의 총 흡수 표면적을 증가시켜 생장 및 발달에 중요한 역할을 하며(Park 등, 2009), 부정근의 길이가 길수록 영양소 흡수에 효율적이며 수확량 및 바이오매스가 증가한다(Oosterhuis와 Zhao, 1994; Sousa 등, 2021). 따라서 본 실험에서 에틸렌의 함량을 측정하지 않았지만, 오존수가 부정근 유도 및 형성에 영향을 미쳤을 것으로 추측할 수 있으며, 식물 외관을 고려할 때 5분 침지 처리는 15-20ppm, 2시간 침지 처리는 5-10ppm 농도로 침지하면 발근 및 생육에 긍정적으로 작용할 것으로 생각된다.
2. 부정근의 개수 및 길이
오존수에 5분 동안 침지처리 후 2주차에서 20ppm 농도로 처리된 삽수의 평균 부정근 개수가 가장 많았으나 대조구 및 각 처리에 따른 유의한 차이는 없었다(Fig. 3A). 3주차는 10ppm 농도로 처리된 삽수의 부정근 개수는 대조구보다 185% 증가하였지만 통계적 유의차가 없었으며, 1ppm 처리구 대비 9배 유의하게 증가하였다. 4주차에는 20ppm 농도로 처리된 평균 부정근 개수는 5개로 대조구보다 525% 증가하였으며, 저농도인 1ppm 처리 된 삽수의 부정근 개수보다 11.5배 증가했다. 처리된 오존수 농도 중에서 10ppm처리는 2-4주로 시간이 경과함에 따라 증가하는 경향을 나타내었고, 15와 20ppm 처리는 2, 3주에서 차이는 없었지만 4주차에서 각각 2주차 대비 183, 127% 증가하였다. 2시간 동안 오존수에 침지한 결과 1ppm농도로 처리한 삽수의 부정근 개수는 2, 3주차에서 높았지만 다른 처리구와는 유의한 차이를 보이지 않았다(Fig. 3B). 4주차에서는 10ppm 농도 처리의 삽수 개수가 대조구보다 약 88% 증가하였지만 유의한 차이는 없었다. 15와 20ppm 처리구는 10ppm 처리구보다 각각 325%, 580% 유의적으로 부정근 개수가 감소하였다. 10ppm 농도 처리는 시간이 경과함에 따라 증가하는 경향을 보였으나, 나머지 처리구는 3주차에서 증가 또는 비슷하였으며, 4주차에서 감소하였다. 특히 버드나무 삽수를 2시간 동안 침지처리할 경우 15와 20ppm에서 유의하게 낮은 결과를 나타냈다.
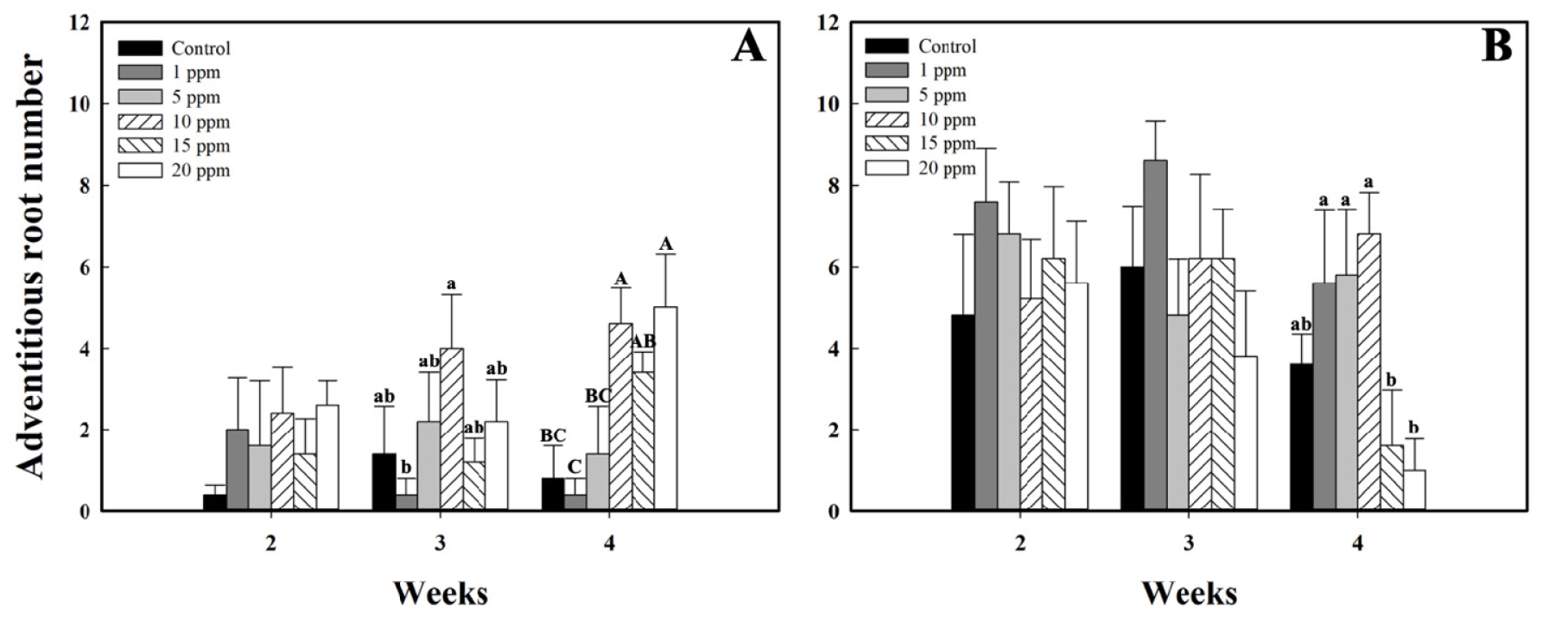
Fig. 3.
The number of adventitious roots of Salix koreensis for 4 weeks after 5 minutes (A), 2 hours (B) of different ozonated water concentration treatments. The data represents the means and the vertical bars indicate standard errors (n=5). Different letters at the top of bars indicate significances of Salix koreensis (p ≤ 0.05).
오존수에 농도별로 5분 동안 침지한 버드나무 삽수를 플러그 트레이에 식재 후 부정근의 길이를 측정한 결과 2주차에서는 20ppm 농도로 침지처리한 삽수의 부정근 평균 길이가 대조구보다 318%, 3주차에서는 10과 20ppm 농도로 처리한 삽수가 대조구보다 각각 138%, 132% 증가하였지만 유의한 차이는 없었다(Fig. 4A). 오존수 처리 4주차에서 10ppm 농도로 처리한 삽수의 부정근 길이가 대조구보다 600% 유의하게 증가하였다. 식재 후 발근 기간인 4주 동안 분석한 결과 대조구와 1ppm으로 처리된 삽수에서 발생된 부정근의 평균 길이는 주차별로 차이를 보이지 않았으며, 5, 10, 15ppm으로 처리된 삽수는 2주차에서 4주차로 시간이 경과 함에 따라 각각 15, 131, 156%씩 증가하였다. 2시간 동안 오존수를 침지처리한 결과 2주차는 15ppm처리가 3주차는 5ppm처리가 다른 실험구와 비교하여 높은 값을 나타냈지만, 대조구와 다른 처리구들과는 유의한 차이가 없었다(Fig. 4B). 4주차에서 5ppm 농도로 처리된 삽수의 길이가 2.83cm로 대조구 대비 유의적으로 103% 증가하였다. 발근 처리 기간인 4주간을 고려할 때 5ppm 처리의 경우 2주차에서 4주차로 시간이 경과할 때 131.9% 증가한 반면에, 15와 20ppm의 경우 2주차에서 4주차로 시간이 경과할 때 각각 74%와 82% 감소하였다.
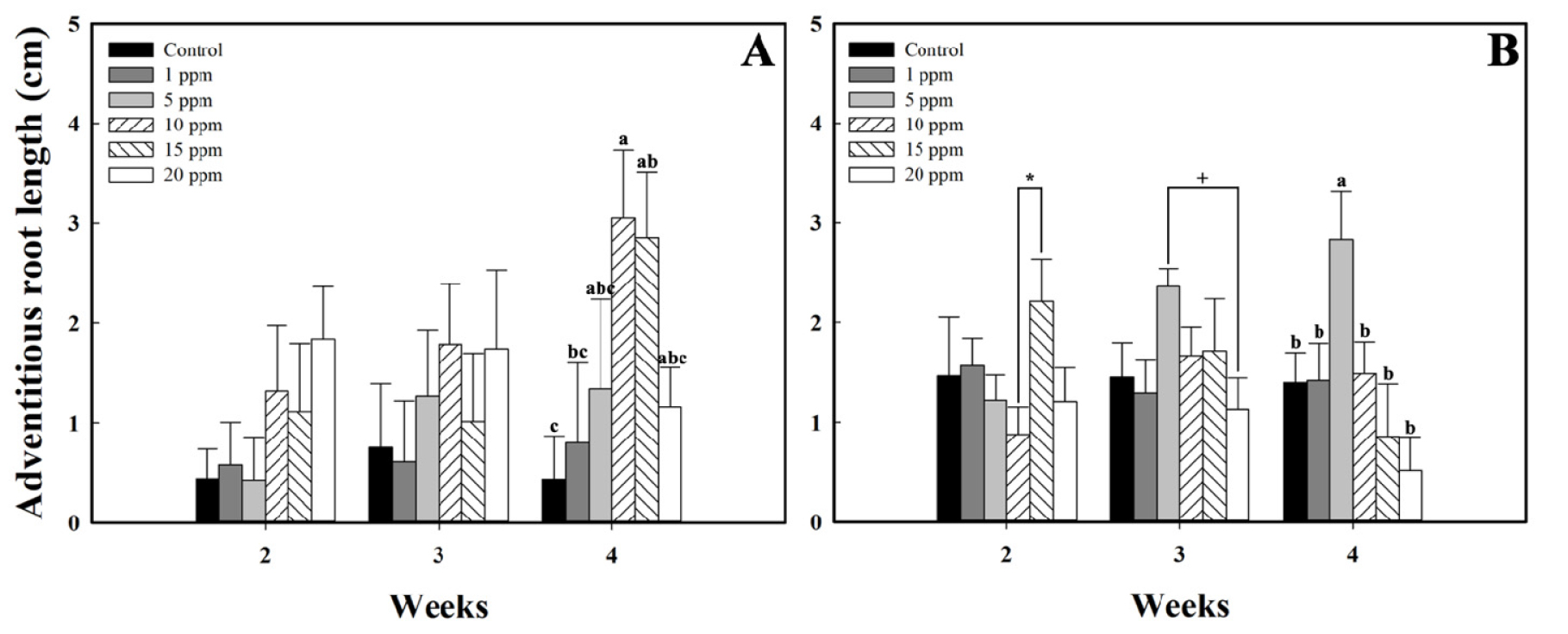
Fig. 4.
The average adventitious roots length of Salix koreensis for 4 weeks after 5 minutes (A), 2 hours (B) of different ozonated water concentration treatments. The data represents the means and the vertical bars indicate standard errors (n=5). Different letters, asterisk, plus sign at the top of bars indicate significances of Salix koreensis (p ≤ 0.05).
오존수에서 방출된 O3 가스는 시간에 지남에 따라 대기 중으로 방출되고, 기공을 통해 들어가 하이드록실 라디칼(OH-), 과산화수소(H2O2)등의 식물 발달, 뿌리 생장 및 호흡 등에 관여하는 활성산소종을 생성한다(Carol 등, 2005; Gapper와 Dolan, 2006; Heath와 Taylor, 1997; Krasuska 등, 2016; Krasuska와 Gniazdowska, 2015). 또한, 오존을 뿌리에 처리하면 호흡을 개선시키거나 뿌리가 썩는 것을 감소시켜 영양소 흡수와 바이오매스의 생산을 증가(Edwards, 1991; Ohashi- Kaneko 등, 2009; Scagel과 Andersen, 1997; Sudhakar 등, 2008) 또는 감소(Edwards, 1991; Shan 등, 1996)가 했다고 보고되어 식물체에 다양한 처리 방법 및 적정 농도와 시간은 실험마다 차이가 있으나, 오존이 뿌리 호흡에 영향을 미치는 것으로 알려져있다. 오존수가 버드나무 삽수 발근에 미치는 영향을 분석한 결과 오존수 농도 및 처리시간에 따라 5분은 10-15ppm, 2시간은 5ppm에서 부정근 발근이 이루어지는 결과를 보여줬다. 그러나 본 실험에서 관측된 지상부 괴사 및 생장점의 발달에 대해서는 정확한 분석이 이루어지지 않았으며, 처리된 오존수의 농도에 따라서 지나친 산화 작용으로 절단 기저부가 손상을 입어 발근이 이루어지지 않은 개체들이 발생했으므로 추후 오존수가 삽수의 지상부 생육에 미치는 영향, 근권 및 지상부로 배출되는 오존의 양을 측정하는 실험이 수행되어야 할 것으로 사료된다.
Acknowledgements
본 연구는 산림청(한국임업진흥원) 산림생명자원 소재발굴연구(R&D)개발 사업의 지원을 받아 수행된 연구임(2020202A00-2122-BA01).
References
Argus G.W. 1986, The genus
Salix (Salicaceae) in the southeastern United States. Systematic Botany Monographs 9:1-170. doi:10.2307/25027618
10.2307/25027618Behzadi H.R., N. Samadi, A. Samadi, M. Safar, S. Shahi, and M. Qaryan 2012, The ozone application for control of the root knot nematode in tomato greenhouse. Elixir Agriculture 48:9387-9389.
Burney J., L. Woltering, M. Burke, R. Naylor, and D. Pasternak 2010, Solar-powered drip irrigation enhances food security in the Sudano-Sahel. Proc Natl Acad U S A 107:1848-1853. doi:10.1073/pnas.0909678107
10.1073/pnas.090967810720080616PMC2806882Buwalda F., K.S. Kim, R. Frenck, B. Locker, and B.V.D. Berg-De Vos 1995, Effects of irrigation frequency and type of root medium and the growth of chrysanthemum cuttings. Acta Hort 401:193-200.
10.17660/ActaHortic.1995.401.23Carol R.J., S. Takeda, P. Linstead, M.C. Durrant, H. Kakesova, P. Derbyshire, S. Drea, V. Zarsky, and L. Dolan 2005, A RhoGDP dissociation inhibitor spatially regulates growth in root hair cells. Nature 438:1013-1016. doi:10.1038/nature04198
10.1038/nature0419816355224Cha D.S., J.H. Oh, B.Y. Ji, K.H. Cho, and H.J. Lee 2008, Development of the soil bioengineering techniques for restoring of degraded forest area (V)-pull-out resistance characteristics of shrubs' roots. J For Sci 24:111-118. (in Korean)
Chae S.M., K.M. Ja, S.Y. Kim, and L.C. Heon 2020, Early growth response and nutrient absorption characteristics of willows (
Salix sp.) treated with nitrogen source. J Korean Env Res Tech 23:63-79. doi:10.13087/kosert.2020.23.3.63
10.13087/kosert.2020.23.3.63Cho K.T., R.H. Jang, S.H. Lee, Y.S. Han, and Y.H. You 2013, Effects of global warming and environmental factors of light, soil moisture, and nutrient level on ecological niche of
Quercus acutissima and
Quercus variabilis. Korean J Ecology and Environment 46:429-439. doi:10.11614/KSL.2013.46.3.429
10.11614/KSL.2013.46.3.429Craker L.E. 1971, Ethylene production from ozone injured plants. Environmental Pollution(1970) 1:299-304. doi:10.1016/0013-9327(71)90022-X
10.1016/0013-9327(71)90022-XD'Odorico P., A. Bhattachan, K.F. Davis, S. Ravi, and C.W. Runyan 2013, Global desertification: drivers and feedbacks. Adv Water Resour 51:326-344. doi:10.1016/j.advwatres.2012.01.013
10.1016/j.advwatres.2012.01.013de Sousa S.M., C.A. de Oliveira, D.L. Andrade, C.G. de Carvalho, V.P. Ribeiro, M.M. Pastina, I.E. Marriel, U.G. de Paula Lana, and E.A. Gomes 2021, Tropical
Bacillus strains inoculation enhances maize root surface area, dry weight, nutrient uptake and grain yield. J Plant Growth Regul 40:867-877. doi:10.1007/s00344-020-10146-9
10.1007/s00344-020-10146-9Ebihara K., H. Stryczewska, T. Ikegami, F. Mitsugi, and J. Pawlat 2011, On-site ozone treatment for agricultural soil and related applications. Przeglad Elektrotechniczny 87:148-152.
Edwards N.T. 1991, Root and soil respiration responses to ozone in
Pinus taeda L. seedlings. New Phytol 118:315-321. doi:10.1111/j.1469-8137.1991.tb00983.x
10.1111/j.1469-8137.1991.tb00983.x33874182Gapper C., and L. Dolan 2006, Control of plant development by reactive oxygen species. Plant Physiol 141:341-345. doi:10.1104/pp.106.079079
10.1104/pp.106.07907916760485PMC1475470Gaspar T., C. Kevers, and J.F. Hausman 1997, Indissociable chief factors in the inductive phase of adventitious rooting. Biology of Root Formation and Development 65:55-63. doi:10.1007/978-1-4615-5403-5_9
10.1007/978-1-4615-5403-5_915321313Gaspar T., O. Faivre-Rampant, C. Kevers, J. Dommes, and J.F. Hausman 2002, Auxins in the biology of roots. Plant roots: The hidden half, 3rd ed. Marcel Dekker, Inc., New York, pp 383-403.
10.1201/9780203909423.pt5Grantz D., S. Gunn, and H.B. Vu 2006, O
3 impacts on plant development: a meta‐analysis of root/shoot allocation and growth. Plant Cell Environ 29:1193-1209. doi:10.1111/j.1365-3040.2006.01521.x
10.1111/j.1365-3040.2006.01521.x17080943Hausman J.F., D. Evers, C. Kevers, and T. Gaspar 1997, Conversion of putrescine to γ-aminobutyric acid, an essential pathway for root formation by poplar shoots in vitro. Biology of Root Formation and Development 65:133-139. doi:10.1007/978-1-4615-5403-5_21
10.1007/978-1-4615-5403-5_21Heath R.L., and G.E. Taylor Jr 1997, Physiological processes and plant responses to ozone exposure. Forest Decline and Ozone 127:317-368. doi:10.1007/978-3-642-59233-1_10
10.1007/978-3-642-59233-1_10Iizuka S., and H. Saito 2016, Growth promotion of Komatsuna (
Brassica rapa var.
perviridis) by ozonated water supplied intermittently to underground roots. Plasma Med 6:255-264. doi:10.1615/PlasmaMed.2016018691
10.1615/PlasmaMed.2016018691Ishii M., V.P. Lam, K. Fujiwara, and J.S. Park 2021, Intermittent root flushing with ozonated water promotes growth of Japanese mustard spinach (
Brassica rapa var. perviridis) grown in a nutrient film technique hydroponic culture-preliminary results. Ozone Sci Eng 1-9. doi:10.1080/01919512.2021.1967723
10.1080/01919512.2021.1967723Jeong S.H., and S.H. Lee 2020, Effects of windbreak forest according to tree species and planting methods based on wind tunnel experiments. Forest Sci Technol 16:188-194. doi:10.1080/21580103.2020.1823896
10.1080/21580103.2020.1823896Kim H.J., and J.H. Lee 1998, A study on the
Salix's biotechnical application. Journal Korea Institute of Landscape Architecture 26:143-151. (in Korean)
Kim H.J., and J.H. Lee 1999, A study on the selection of
Salix live branches in the case of slope revegetation technology of biological engineering. J Korean Env Res & Reveg Tech 2:32-37. (in Korean)
Kim T.W., J.W. Lee, J.M. Kim, G.Y. Kim, and J.H. Kim 2021, High power-density LDC design for ultra-compact electric vehicles. Trans Korean Inst Power Electron 26:199-204. (in Korean) doi:10.6113/TKPE.2021.26.3.199
10.6113/TKPE.2021.26.3.199Kim W.S., B. Choi, M.K. Kim, S.H. Chae, and I.S. Kwak 2020, Expression of heat shock protein 70 gene and body color changes in non-biting midge larvae (
Glyptotendipes tokunagai) effected by O
3 treatment. Korean J Ecology and Environment 53:324-330. (in Korean) doi:10.11614/KSL.2020.53.4.324
10.11614/KSL.2020.53.4.324Kim Y.S., I.S. Park, A.Y. Kim, K.M. Jeon, Y.M. Seo, S.H. Choi, Y.J. Lee, H.C. Choi, D.H. Jeon, H.I. Kim, and S.D. Ha 2008, Application, utilization and management of ozone water in food manufacturing. J Fd Hyg Safety 23:98-107. (in Korean)
Koseki S., and S. Isobe 2006, Effect of ozonated water treatment on microbial control and on browning of iceberg lettuce (
Lactuca sativa L.). J Food Prot 69:154-160. doi:10.4315/0362-028X-69.1.154
10.4315/0362-028X-69.1.15416416913Krasuska U., and A. Gniazdowska 2015, ROS-RNS-Phytohormones network in root response strategy. Reactive Oxygen Species and Oxidative Damage in Plants Under Stress pp 321-339. doi:10.1007/978-3-319-20421-5_13
10.1007/978-3-319-20421-5_13Krasuska U., O. Andrzejczak, P. Staszek, W. Borucki, and A. Gniazdowska 2016, Toxicity of canavanine in tomato (
Solanum lycopersicum L.) roots is due to alterations in RNS, ROS and auxin levels. Plant Physiol Biochem 103:84-95. doi:10.1016/j.plaphy.2016.03.005
10.1016/j.plaphy.2016.03.00526986929Kuzovkina Y.A., and M.F. Quigley 2005, Willows beyond wetlands: uses of
Salix L. species for environmental projects. Water Air Soil Pollut 162:183-204. doi:10.1007/s11270-005-6272-5
10.1007/s11270-005-6272-5Kuzovkina Y.A., and T.A. Volk 2009, The characterization of willow (
Salix L.) varieties for use in ecological engineering applications: co-ordination of structure, function and autecology. Ecol Eng 35:1178-1189. doi:10.1016/j.ecoleng.2009.03.010
10.1016/j.ecoleng.2009.03.010Lee I.S., P.H. Lee, S.G. Son, C.S. Kim, and K.H. Oh 2001, Distribution and community structure of
Salix species along the environmental gradients in the Nam-River watershed. Korean J Ecol 24:289-296. (in Korean)
Michels K., J. Lamers, and A. Buerkert 1998, Effects of windbreak species and mulching on wind erosion and millet yield in the Sahel. Exp Agric 34:449-464. doi:10.1017/S0014479798004050
10.1017/S0014479798004050Mrak T., I. Štraus, T. Grebenc, J. Gričar, Y. Hoshika, G. Carriero, E. Paoletti, and H. Kraigher 2019, Different belowground responses to elevated ozone and soil water deficit in three European oak species (
Quercus ilex,
Q. pubescens and
Q. robur). Sci Total Environ 651:1310-1320. doi:10.1016/j.scitotenv.2018.09.246
10.1016/j.scitotenv.2018.09.24630360263Ohashi-Kaneko K., M. Yoshii, T. Isobe, J.S. Park, K. Kurata, and K. Fujiwara 2009, Nutrient solution prepared with ozonated water does not damage early growth of hydroponically grown tomatoes. Ozone Sci Eng 31:21-27. doi:10.1080/01919510802587523
10.1080/01919510802587523Oosterhuis D.M., and D. Zhao 1994, Increased root length and branching in cotton by soil application of the plant growth regulator PGR-IV. Plant Soil 167:51-56. doi:10.1007/BF01587597
10.1007/BF01587597Paoletti E., and N.E. Grulke 2005, Does living in elevated CO
2 ameliorate tree response to ozone? A review on stomatal responses. Environ Pollut 137:483-493. doi:10.1016/j.envpol.2005.01.035
10.1016/j.envpol.2005.01.03516005760Park J.S., T. Isobe, S. Kusakari, and K. Fujiwara 2009, Promotion of adventitious roots in Chrysanthemum cuttings by soaking in ozonated water. Ozone Sci Eng 31:15-20. doi:10.1080/01919510802587143
10.1080/01919510802587143Pulford I.D., D. Riddell-Black, and C. Stewart 2002, Heavy metal uptake by willow clones from sewage sludge-treated soil: the potential for phytoremediation. Int J Phytoremediation 4:59-72. doi:10.1080/15226510208500073
10.1080/15226510208500073Roy S., S. Labelle, P. Mehta, A. Mihoc, N. Fortin, C. Masson, R. Leblanc, G. Châteauneuf, C. Sura, C. Gallipeau, C. Olsen, S. Delisle, M. Labrecque, and C. W. Greer 2005, Phytoremediation of heavy metal and PAH-contaminated brownfield sites. Plant Soil 272:277-290. doi:10.1007/s11104-004-5295-9
10.1007/s11104-004-5295-9Rubio J.L., and E. Bochet 1998, Desertification indicators as diagnosis criteria for desertification risk assessment in Europe. J Arid Environ 39:113-120. doi:10.1006/jare.1998.0402
10.1006/jare.1998.0402Sandermann Jr H. 1996, Ozone and plant health. Annu Rev Phytopathol 34:347-366. doi:10.1146/annurev.phyto.34.1.347
10.1146/annurev.phyto.34.1.34715012547Scagel C.F., and C.P. Andersen 1997, Seasonal changes in root and soil respiration of ozone-exposed ponderosa pine (
Pinus ponderosa) grown in different substrates. The New Phytol 136:627-643. doi:10.1046/j.1469-8137.1997.00779.x
10.1046/j.1469-8137.1997.00779.x33863111Shan Y., Z. Feng, T. Izuta, M. Aoki, and T. Totsuka 1996, The individual and combined effects of ozone and simulated acid rain on growth, gas exchange rate and water-use efficiency of
Pinusarmandi Franch. Environ Pollut 91:355-361. doi:10.1016/0269-7491(95)00039-9
10.1016/0269-7491(95)00039-9Shili W., M. Yuping, H. Qiong, and W. Yinshun 2006, Coping strategies with desertification in China. Managing Weather and Climate Risks in Agriculture pp 317-341. doi:10.1007/978-3-540-72746-0_18
10.1007/978-3-540-72746-0_18Somiya I. 2004, Ozone Handbook. Japan Ozone Association, Tokyo, Japan.
Stoltz E., and M. Greger 2002, Accumulation properties of As, Cd, Cu, Pb and Zn by four wetland plant species growing on submerged mine tailings. Environ Exp Bot 47:271-280. doi:10.1016/S0098-8472(02)00002-3
10.1016/S0098-8472(02)00002-3Strader L.C., G.L. Chen, and B. Bartel 2010, Ethylene directs auxin to control root cell expansion. Plant J 64:874-884. doi:10.1111/j.1365-313X.2010.04373.x
10.1111/j.1365-313X.2010.04373.x21105933PMC3735369Sudhakar N., D. Nagendra-Prasad, N. Mohan, and K. Murugesan 2008, A preliminary study on the effects of ozone exposure on growth of the tomato seedlings. Aust J Crop Sci 2:33-39.
Vandecasteele B., E. Meers, P. Vervaeke, B. De Vos, P. Quataert, and F.M. Tack 2005, Growth and trace metal accumulation of two
Salix clones on sediment-derived soils with increasing contamination levels. Chemosphere 58:995-1002. doi:10.1016/j.chemosphere.2004.09.062
10.1016/j.chemosphere.2004.09.06215664607Vendruscolo J., A.M. Perez Marin, E. dos Santos Felix, K.R. Ferreira, W.C.S. Cavalheiro, and I.M. Fernandes 2021, Monitoring desertification in semiarid Brazil: using the desertification degree index (DDI). Land Degrad Dev 32:684-698. doi:10.1002/ldr.3740
10.1002/ldr.3740Wang X., E. Agathokleous, L. Qu, M. Watanabe, and T. Koike 2016, Effects of CO
2 and O
3 on the interaction between root of woody plants and ectomycorrhizae. J Agric Meteorol 72:95-105. doi:10.2480/agrmet.D-14-00045
10.2480/agrmet.D-14-00045Watson C., I.D. Pulford, and D. Riddell‐Black 2003, Development of a hydroponic screening technique to assess heavy metal resistance in willow (
Salix). Int J Phytoremediation 5:333-349. doi:10.1080/15226510309359041
10.1080/1522651030935904114750561Wezel A., and T. Rath 2002, Resource conservation strategies in agro-ecosystems of semi-arid West Africa. J Arid Environ 51:383-400. doi:10.1006/jare.2001.0968
10.1006/jare.2001.0968Yang X., K. Zhang, B. Jia, and L. Ci 2005, Desertification assessment in China: An overview. J Arid Environ 63:517-531. doi:10.1016/j.jaridenv.2005.03.032
10.1016/j.jaridenv.2005.03.032Yergeau E., J. Tremblay, S. Joly, M. Labrecque, C. Maynard, F.E. Pitre, M. St-Arnaud, and C.W. Greer 2018, Soil contamination alters the willow root and rhizosphere metatranscriptome and the root-rhizosphere interactome. ISME J 12:869-884. doi:10.1038/s41396-017-0018-4
10.1038/s41396-017-0018-429330533PMC5864237Yun Y.H., G.R. Ahn, S.K. Yoon, H.H. Kim, S.Y. Son, and S.H. Kim 2016, New rust disease of Korean willow (
Salix koreensis) caused by
Melampsora yezoensis, unrecorded pathogen in Korea. Mycobiology 44:335-337. doi:10.5941/MYCO.2016.44.4.335
10.5941/MYCO.2016.44.4.33528154494PMC5287169







