서 론
망고(Mangifera indica L.)는 세계 30대 주요 작물 중 하나로 열대 혹은 아열대 지역에서 주로 재배된다. 국내 에 널리 알려진 노란색 망고의 품종은 카라바오 망고 (Carabao mango)로 약간의 신맛을 낸다(Naef 등, 2006). 다른 주요 품종으로는 어윈 망고(Mangifera indica L. cv. Irwin)가 있으며, 껍질이 붉기 때문에 애플 망고 (Apple mango)라고도 부른다. 어윈 망고는 당도가 높고 즙이 많으며, 향기가 진한 특징을 나타낸다. 최근 이러 한 풍미를 갖는 어윈 망고에 대한 수요가 증가하고 있 으나, 국내에서는 제주도와 여수, 통영 등의 일부 지역 에서 25ha 정도의 면적에서 재배되고 있는 실정이다(An 등, 2015; Park 등, 2014).
일본의 오키나와에서는 1984년부터 상업적인 목적으로 망고를 온실에서 재배하기 시작했다(Akinaga와 Hasbullah, 2002). 한국과 일본은 망고의 생육에 적합하지 않은 기 후 특성을 갖고 있으며, 특히 겨울철 동해 피해가 쉽게 일어날 수 있다. 따라서 대부분의 망고 재배 농가는 가 온 시스템을 겸비한 온실에서 재배하고 있다(Honsho 등, 2012). 화석연료를 사용하는 가온 방식은 농가의 난방비 부담을 늘린다는 단점 때문에 일부 열대 과수 재배 농 가는 지열을 이용한 히트펌프를 사용하거나 화력발전소 에서 온배수의 형태로 배출되는 폐열을 열원으로 이용하 고 있다(Lee 등, 2006; Ryou 등, 2012). 가온을 실시하 는 망고 재배 온실은 열 손실을 막기 위해서 밀폐성이 높은 보온 구조를 가지고 있다. 또한 제주도 지역의 온 실은 잦은 태풍으로 인한 피해를 방지하기 위해 다량의 철골 구조물을 사용하고 있다. 이와 같이 온실 내부의 공간적 제약으로 인하여, 망고 과수는 인공적인 유인과 전정을 통해 낮은 수고를 갖는 배상형으로 재배된다 (Yonemoto, 2006). 실제로 배상형으로 재배 시에도 애플 망고는 수고 2m 이상 자라기 때문에, 상단부와 하단부 잎에 도달하는 광량이 다르다. 그러나 현재까지 망고 재 배 온실의 특징적인 환경에 대한 체계적인 연구가 진행 되지 않고 있다.
과수 작물의 생산량을 증가시키기 위해서는 광합성에 의한 동화산물이 증대되어야 하며, 이러한 측면에서 군 락 광합성속도는 매우 중요하다. ‘Kensington’ 망고의 경 우, 짧은 시간 동안 고농도의 CO2 환경에 노출시킬 때 CO2 농도가 증가함에 따라 광합성속도가 증가된다는 보 고되었다. 그러나 광강도 1200μmol·mol-1 에서 광합성속 도가 포화를 나타내는 광포화점을 보였으며, 이는 광합 성의 생화학적 반응의 최대치에 도달했기 때문으로 해석 하였다(Schaffer 등, 1997; Whiley와 Schaffer, 1997). 이 외에도 Chamchaiyaporn 등(2013)은 직각 쌍곡선 함수를 이용하여 광도의 증가에 따른 광합성속도 증가를 표현하 였으나, 37°C의 고온에서 측정한 광합성속도이기 때문에 최대광합성속도가 약 3.5μmol·m-2·s-1로 매우 낮게 나온 결과를 보여주었다. 이와 같은 망고의 광합성 측정 결과 들은 국내의 망고 재배 시설 농가에서 활용하기에 부적 절한 경우가 많으며, 다양한 환경 요인에 대해 반영하지 못하고 있다는 단점이 있다. 본 연구는 어윈 망고의 수 관 위치 별 엽 광합성속도를 정량화하여 측정한 후, 광 도와 CO2 농도의 2변수 함수로 나타내어 엽 광합성 모 델 개발을 목표로 하였다.
재료 및 방법
1 재배 조건
어윈 망고의 엽광합성 속도 조사를 위하여 제주특별자 치도 서귀포시 안덕면 화순리에 위치한 행복나눔영농조 합(33.304°N, 126.626°E)의 면적 2,640m2 연동 플라스틱 필름 온실에서 실시하였다. 측정에 사용한 어윈 망고는 6년생으로 대형 용기(높이 40cm, 지름 80cm)에서 재배 하며, 관수는 4-5일에 한번 하루 15분간 30L의 관수를 실시하였다. 재배 시설은 폴리에틸렌폼과 부직포가 혼합 된 보온커튼이 설치되었으며, 내부 기온은 25-30°C, 습 도는 55-60% 정도로 유지되었다. 측정 시기인 1-2월의 개화기에 수분을 실시하며, 2월 중순 이후 과실이 비대 하여 5월경 수확할 수 있도록 재배하였다. 1년에 한 번 정단부에서 새로 자란 가지를 전정하여 3개의 측지가 발생하도록 유도하며, 온실 철골 구조물에 유인줄을 이 용하여 가지를 유인하였다.
2 엽 광합성속도 측정
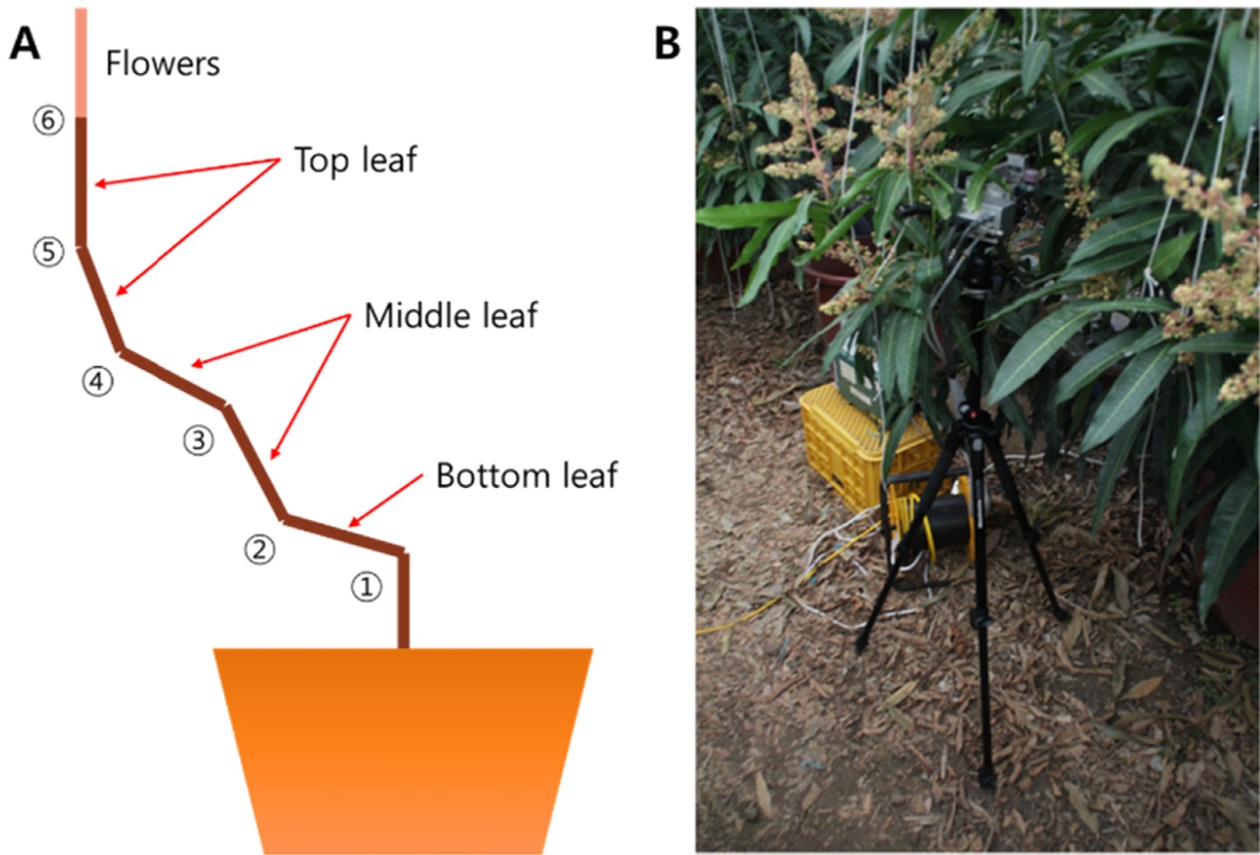
엽 광합성속도(이후, 광합성속도) 측정은 3회에 걸쳐서 측정하였다. 1차 측정은 2015년 1월 22일에 실시하였으 며, 적합한 광합성 모델을 결정하기 위하여 실시하였다. 측정에 적용된 광도 조건은 0, 25, 50, 100, 200, 400, 800, 1200μmol·m-2·s-1로 실시하였으며, CO2 농도는 800μmol·mol-1로 유지하였다. 측정은 Fig. 1A에 나타낸 마디 수 기준으로 상단부(4~6마디) 와 중단부(2~4마디), 하단부(1~2마디)에 대하여 각각 다른 엽으로 3반복 측정 하였다. 측정에는 광합성 측정장치 (LI-6400, LI-COR, Lincoln, NE, USA)을 이용하였다(Fig. 1B).
2차 측정은 2015년 2월 23-24일 오전 10시부터 오후 5시까지 실시하였으며, 1차 측정에서 결정된 모델을 이 용하여 2변수 광합성속도 모델을 확립하기 위하여 실시 하였다. 광도 조건은 1차 측정에서 나타난 포화 조건을 고려하여 0, 50, 100, 200, 300, 400, 600, 800μmol·m- 2·s-1을 설정하였다. CO2 농도는 기존 연구 결과를 고려 하여 100, 400, 800, 1200, 1600μmol·mol-1을 설정하였 다(Schaffer 등, 1997). 측정 방법은 1차 측정과 동일하 며, 광도 8조건, CO2 농도 5조건 (총 360 측정)에 대하 여 측정을 실시하였다.
3차 측정은 2015년 4월 3일 오후 3시부터 오후 6시까지 실시하였으며, 2차 측정에서 확립한 모델을 검증하기 위한 광합성속도의 실측값을 얻고자 하였다. 광도 조건은 50, 200, 400, 600μmol·m-2·s-1, CO2 농도는 100, 800, 1600μmol·mol-1을 설정하였다. 측정 방식은 2회차와 동일 하며, 각 위치 별 임의의 엽에 대하여 광도 4조건, CO2 농도 3조건(총 36 조합)에 대하여 측정을 실시하였다.
3 광합성 모델 선정
광도 변화에 따른 광합성속도를 표현하는 모델 식을 선택하기 위하여, 기존에 광포화 곡선에 대하여 가장 널 리 사용되는 두 가지 모델인 Rectangular hyperbola 모델( 식 1)과 Negative exponential 모델(식 2)을 선정하였다.
여기서 P는 광합성속도(μmol·m-2·s-1)이고, PPFD는 400- 700 nm의 광합성유효광양자속밀도(μmol·m-2·s-1), a~c는 회귀분석을 통해 얻어지는 계수를 의미한다. CO2 농도 변화에 따른 광합성속도 또한 Negative exponential 모 델로 표현하였다.
또한 광도와 CO2 농도를 포함하는 2변수 모델(식 4)을 구성하였다. 두 모델의 곱으로 표현한 2변수 모델은 형태 가 단순하여 사용하기에 쉬운 장점이 있다(Jones 등, 1991).
여기서, d는 회귀분석을 통해 얻어지는 계수를 의미한다.
결과 및 고찰
1 적정 광합성 모델 결정
1차 측정에서 위치 별 광도에 따른 광합성속도를 측정 한 후에 2 종류의 모델을 사용하여 회귀분석 하였다(Fig. 2). 광합성속도는 상단부에서 하단부로 갈수록 낮아지는 경향을 나타내었다. 상단부 엽은 광도 400μmol·m-2·s-1, 중단부와 하단부 엽은 광도 200μmol·m-2·s-1에서 광합성 속도가 포화되었다. 회귀분석 결과 상단부와 중단부, 하 단부 엽 모두 Rectangular hyperbola 모델에 비해 Negative exponential 모델에서 R2 값이 높게 나타났다 (Table 1). 따라서 2차 측정 시 적용할 모델은 Negative exponential 모델로 결정하였다.
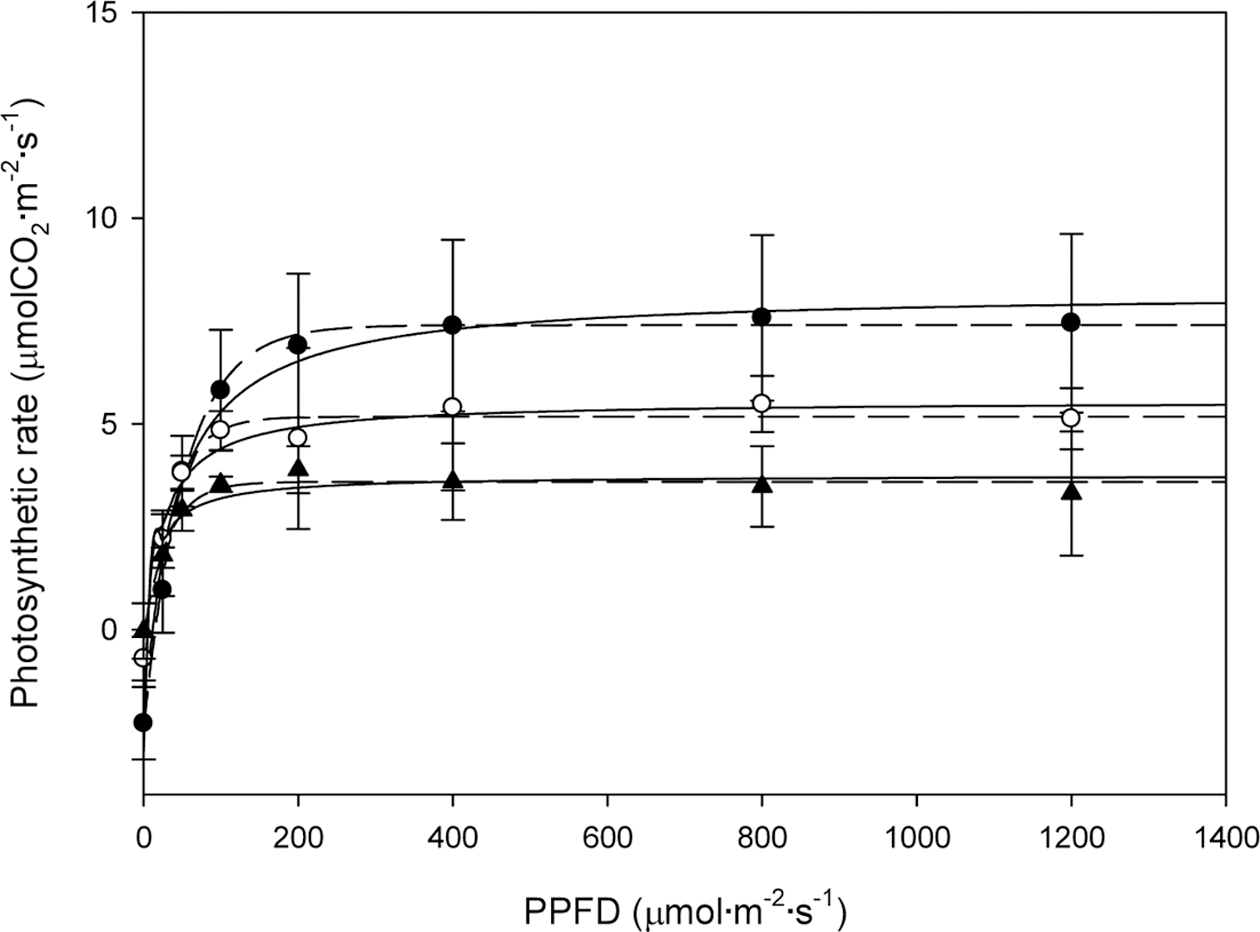
Fig. 2.
Comparison of spatial leaf light curves between rectangular hyperbola (solid line) and negative exponential (dashed line) models. Solid circle, void circle, and solid triangle indicate the top, middle, and bottom leaves, respectively. PPFD is an abbreviation of photosynthetic photon flux density.
2 위치 별 2변수 광합성 모델 개발
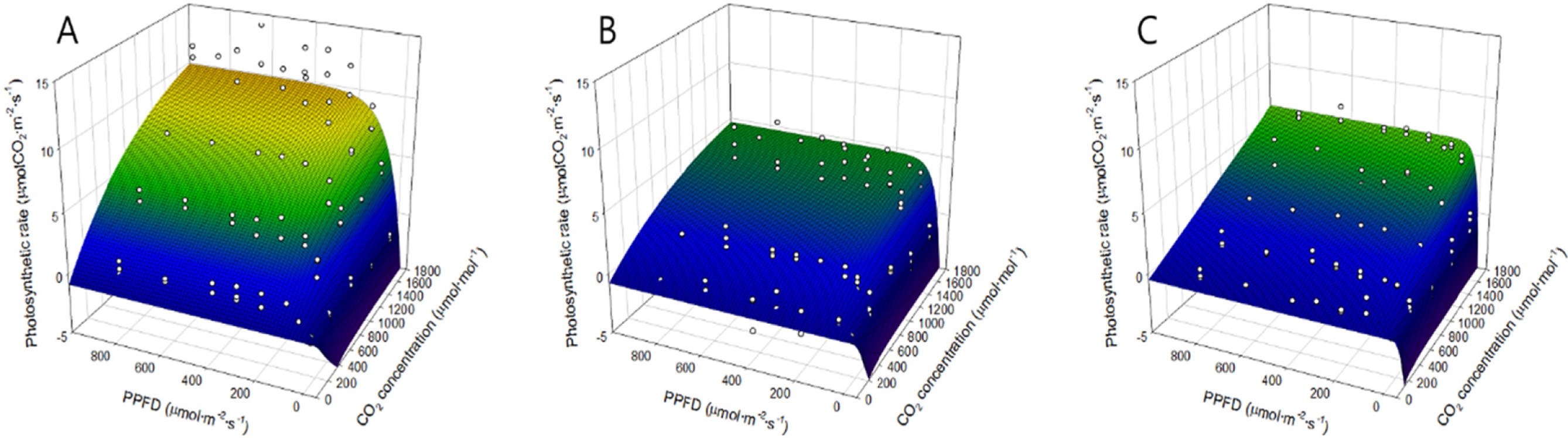
2차 측정에서 위치 별 광도에 따른 광합성속도를 측정 한 후에 Negative exponential 모델에 적용하여 회귀분 석 하였다(Fig. 3). 1차 측정과 동일하게 상단부에서 하 단부로 갈수록 광합성속도가 낮아졌다. 광포화점은 상단 부 엽은 광도 400μmol·m-2·s-1, 중단부와 하단부 엽은 광 도 200μmol·m-2·s-1에서 광합성속도가 포화되었다. 특정 위치의 엽에서 CO2 농도가 증가할수록 광합성속도는 증 가하는 경향을 보였다. 위치 별 CO2 농도에 따른 광합 성속도를 측정한 후, Negative exponential 모델을 사용 하여 회귀분석 하였다(Fig. 4). 상단부 엽은 CO2 농도 1600μmol·mol-1에 이르기까지 광합성속도가 포화되지 않 았고, 광도가 증가할수록 광합성속도가 증가하였다. 반면 중단부와 하단부 엽은 광도가 증가하여도 광합성속도가 거의 증가하지 않았다. 회귀분석 결과, 각 위치 별 엽에 대한 R2 값은 0.60이상으로 나타났다.
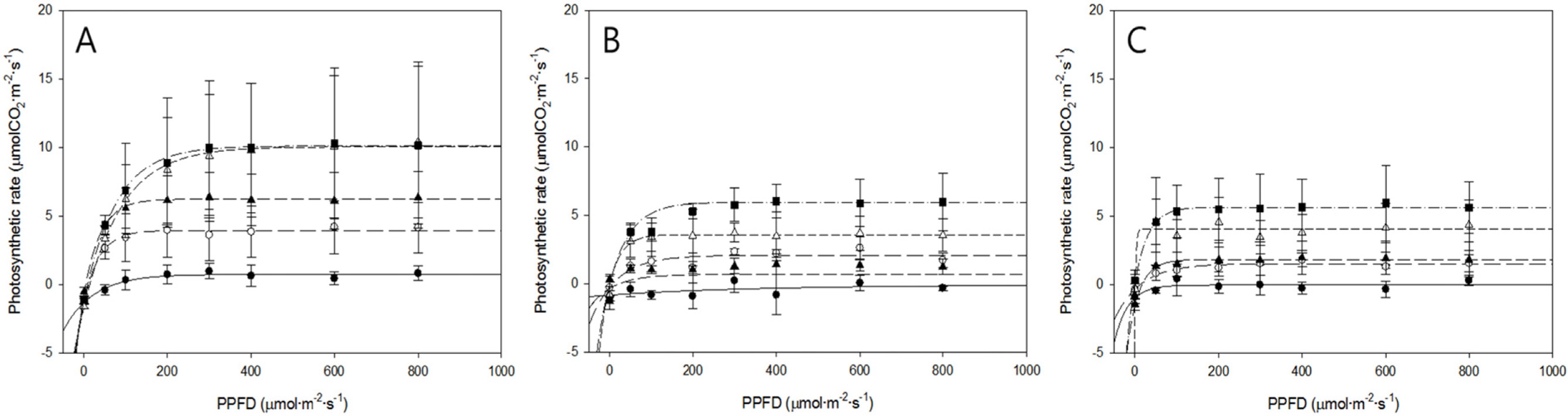
Fig. 3.
Spatial leaf photosynthetic curves (light curve) at different CO2 concentrations of 100 (solid line + solid circle), 400 (long dash line + void circle), 800 (medium dash line + solid triangle), 1200 (short dash line + void triangle), and 1600 (dash-dot line + solid square) μmol·mol-1. A, B, and C mean the top, middle, and bottom leaves, respectively. PPFD is an abbreviation of photosynthetic photon flux density.
위치 별 광도에 대한 2변수 광합성 모델에 대해 회귀 분석을 실시하였다(Fig. 5). 회귀분석을 통해 추정된 모 델의 계수들과 R2 값은 Table 2과 같다. 상단부와 하단 부 엽에 대한 R2 값은 0.72이상이었으나, 중단부 엽은 0.64로 상단부와 하단부 엽에 비해 상대적으로 낮았다.
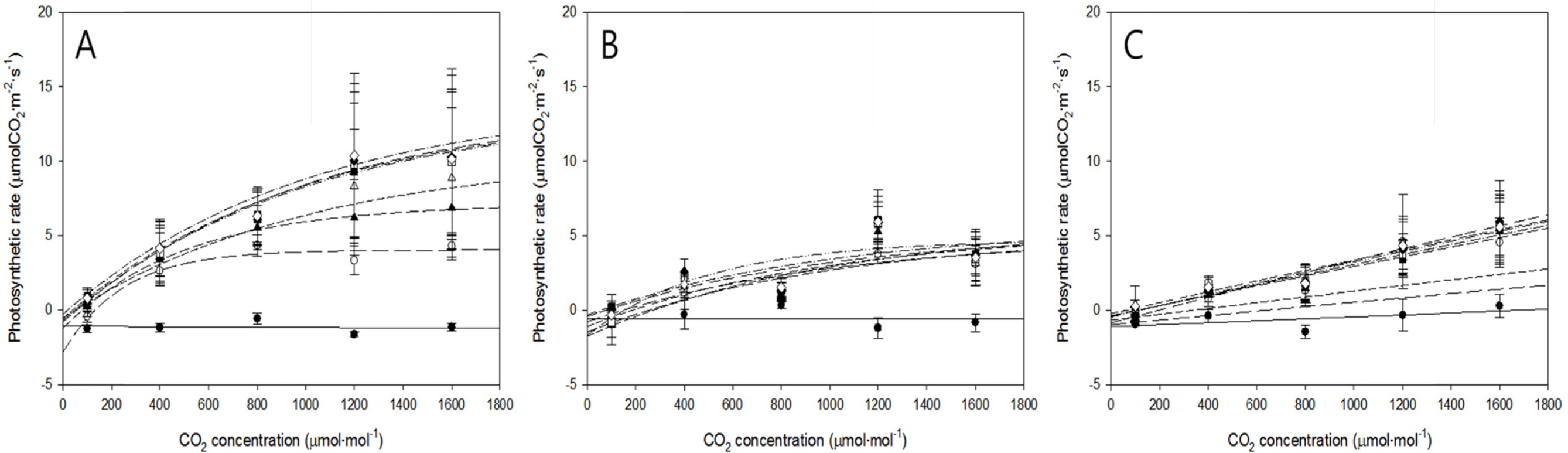
Fig. 4.
Spatial leaf photosynthetic curves (A-Ci curve) at different light intensities of 0 (solid line + solid circle), 50 (long dash line + void circle), 100 (medium dash line + solid triangle), 200 (short dash line + void triangle), 300 (dash-dot line + solid square), 400 (dash-dotdot line), 600 (medium-medium line), and 800 (short-short-short line) μmol·m-2·s-1. A, B, and C mean the top, middle, and bottom leaves, respectively. PPFD is an abbreviation of photosynthetic photon flux density.
Table 2.
Parameters and R2 values of the two variable spatial leaf photosynthetic model.
| Leaf position | a | b | c | d | R2 |
|---|---|---|---|---|---|
| Top | 12.928 | 0.014 | 0.001 | -0.889 | 0.72 |
| Middle | 6.513 | 0.029 | 0.001 | -0.787 | 0.64 |
| Bottom | 2316.887 | -0.045 | 1.60*10-6 | -0.515 | 0.75 |
하단부 광합성 모델에서 추정된 계수 a의 경우 2316.887로 상단부와 중단부 엽에 비해 매우 큰 값을 나타내었다. 이는 Fig. 4에서 실시한 회귀분석 결과에서, CO2 농도에 따른 광합성속도 증가 양상이 포화 곡선으 로 나타나지 않았기 때문에 2변수 광합성 모델에서도 유사한 결과가 나타난 것으로 판단된다. 다양한 작물에 서 수관 하단부에 존재하는 음엽의 경우 Rubisco 함량 과 RuBP 재생산 용량이 감소하는 경향이 나타난다고 보고되었다(Baker와 McKiernan, 1988; Evans, 1993; Osborne 등, 1998). 이러한 이유로 수관 하단부의 음엽 은 광합성 능력이 감소하고 엽 내의 질소 함량이 감소 한다. 결과적으로 음엽은 CO2 농도를 증가시켜 주어도 광합성을 충분히 수행하지 못하게 된다(Del Pozo 등, 2007). 추후 본 연구의 2변수 모델 이외에 Nonrectangular hyperbola 등의 더욱 정교한 모델을 사용할 필요가 있다고 판단된다(Thornley, 2002).
3 위치 별 2변수 광합성 모델 검증
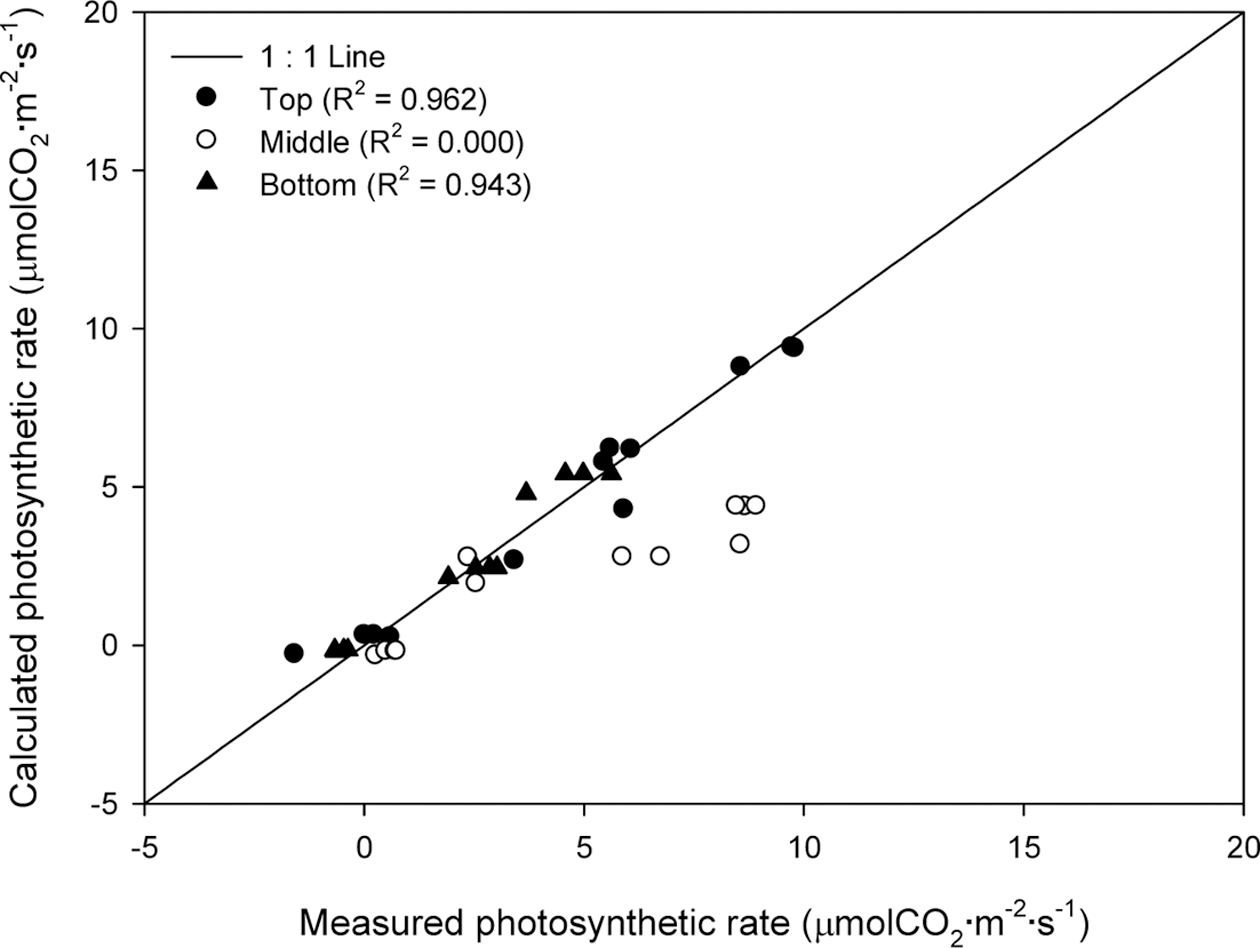
임의의 광도와 CO2 농도에서 2변수 광합성 모델의 예 측 광합성속도와 실측값을 1:1 선에 대하여 회귀분석을 실시하였다(Fig. 6). 검증 결과, 상단부와 하단부 엽에 대한 2변수 광합성 모델은 R2 값이 각각 0.96와 0.94로 나타났으나, 중단부 엽은 R2 값이 0으로 나타났다. 이는 모델에 의해 예측된 광합성속도에 비해 실측값이 높게 나타났기 때문으로 보인다. 3D 시뮬레이션을 활용한 기 존 연구에 따르면, 망고 과수의 중단부 엽은 부위별로 수광 특성이 큰 폭으로 변동하는 것으로 나타났다 (Sinoquet 등, 1998). 따라서 중단부 엽을 세분화하여 수 광량이 높은 외부와, 수광량이 낮은 내부 엽에 대해 각 각 광합성 모델을 적용할 필요가 있다.
본 연구에서 확립한 위치 별 2변수 광합성 모델을 사 용하면 어윈 망고 온실 재배 시 광합성량을 극대화 시 킬 수 있는 광도와 CO2 농도 조건을 결정하는 데 도움 이 될 것이다.