서 론
재료 및 방법
1. 실험재료
2. 식물재배 및 재배환경
3. 수확량 및 과실특성 조사항목 및 조사방법
4. 생육조사 항목 및 측정방법
5. 엽록소형광변수 측정방법
6. 통계분석
결과 및 고찰
1. 방울토마토 수확량 변화
2. 방울토마토 생장상 변화
3. 생육후기의 엽록소형광변수
서 론
시설재배에서 정밀한 환경관리와 생육조절을 통해 작물의 생산성을 높일 수 있다(OMAFRA, 2010). 수경재배법을 이용한 방울토마토 시설재배는 이미 보편화되어 있지만 경영비 소요가 많아 적은 투자 비용 대비 생산량을 극대화할 수 있는 방법이 필요하다. 토마토 접목묘는 재배 후반기까지 세력을 유지할 수 있어(Stanghellini 등, 2019) 생산성을 높이기 위해 접목묘를 사용하는 재배가 늘어나고 있다(OMAFRA, 2010). 토마토 접목은 비생물적 스트레스에 대한 내성을 높이고 양수분 흡수를 높여 수확량을 높일 수 있으며 수확 기간을 늘릴 수 있다(Lee와 ODA, 2003). 토마토 대목의 뿌리는 실생의 뿌리보다 양수분을 흡수할 수 있는 능력이 높으며(Fernández-García 등, 2003) 접목한 식물체는 양수분 흡수 능력이 좋은 것으로 보고된다(Leonardi와 Giuffrida, 2006; Chaplin과 Westwood 1980; Kato와 Lou 1989). 그러므로 토마토에서 접목을 통해 높은 수확량을 얻기 위해서는 적합한 대목과 접수의 사용이 필요하다(Khah 등, 2006). 여러 가지 접목조합에 따라 접목묘의 생육 및 수량 변화를 통해 그 차이를 확인할 수 있는데(Leonardi와 Giuffrida, 2006), 대목과 접수의 친화성이 높은 접목 토마토를 사용하면 수확 기간 및 수확량이 늘어나 농가 소득증대로 이어질 것으로 판단된다.
토마토는 영양생장과 생식생장을 동시에 하는 작물로 두 생장의 균형을 생육 후기까지 맞춰주는 것이 수량을 높이는데 중요하다. 토마토 식물 생육지표를 통해 작물이 영양생장인지 생식생장인지 생장의 균형을 이루는지 판별할 수 있다(OMAFRA, 2010). 작물의 뿌리 상태는 작물의 생장과 수량에 영향을 주는데(Khah 등, 2006), 토마토 대목은 접목한 접수의 생장과 수량에 영향을 주는 것으로 보고된다(Lee와 ODA, 2003). 이와 같이 접목한 토마토의 대목은 뿌리활력이 좋아 대목 종류에 따라 균형있는 생장을 하는지 생장상을 조사하여 이를 실증한 연구가 필요하다. 토마토 생육 진단을 위한 주요 지표를 정의하고 진단에 따른 정보를 제공하는 연구는(Lee, 2015) 있었지만 생육지표을 통한 생장상의 변화와 실제 수량을 비교하는 연구는 부족한 실정이다. 따라서 본 연구는 방울토마토 대목사용에 따른 생육지표를 활용한 생장상의 변화에 있어서 나타나는 수량의 변화를 비교 분석하고자 수행하였다.
잎의 광합성은 과실 생장의 중심이 되는 역할을 한다(Liu 등, 2011). 최근 광합성 기구의 이해와 광합성 효율 분석을 위해 비파괴적 방법인 엽록소형광 분석법이 많이 이용되고 있다(Kang 등, 2016). 엽록소형광 유도곡선을 이용한 엽록소형광 분석은 단시간에 대량으로 분석이 가능하여 식물생장 분석에 활용도가 높다(Yoo 등, 2013). 엽록소형광유도곡선은 엽록소가 암상태를 거치고 원래의 상태로 돌아오는 형광유발 시점(Origin, O) 이후 최소형광변동 지점(Jump, J)을 지나 형광 중간수준(Intermediate, I)에서 최대 형광점에서의 형광유도량(Peak, P)을 표현하는 방식으로 OJIP라고 부른다(Yoo 등, 2013; Govindjee, 1995). OJIP 엽록소형광변수인 PIabs는 광합성계 내부의 전자수용체 환원 정도를 나타내며(Yoo 등, 2013) 광합성 기구의 전반적인 활력도로 사용될 수 있다(Živčák 등, 2008; Strasser 등, 2000). 또 다른 OJIP 엽록소형광변수인 ETo/RC는 퀴논A(QA)를 퀴논A(QA-)로 환원시킬 수 있는 광계2의 전자전달효율을 뜻한다(Yoo 등, 2013). 포도나무 잎의 광합성률은 뿌리의 형태와 생화학적인 특성의 영향을 받아 수분이용 효율이 증가하여 기공전도율이 높아져 광합성률이 높아졌다는 보고가 있으며(Iacono 등, 1998), 작물의 생산량은 태양에너지를 광합성에 얼마나 사용할 수 있는지에 대한 효율에 따라 달라진다(Amthor, 2007). OJIP 엽록소형광변수를 측정하여 방울토마토 접목조합별로 광합성 효율의 차이를 알아보고 광합성 효율과 생산량이 연관되어 있는지 알아보고자 수행하였다.
재료 및 방법
1. 실험재료
방울토마토(Solanum lycopersicum var. cerasiforme) 접목을 위해 대목 품종 4종류와 접수 품종 1종류를 사용하여 접목한 처리구 4개와 접목하지 않은 처리구 1개를 실험에 사용하였다. 대목 품종 4종류는 ‘파워가드’(National Institute of Horticultural and Herbal Science, Korea), ‘T1’(Bunongseed, Korea), ‘L1’(Bunongseed, Korea), ‘B.blocking’(Takii, Japan)을 사용하였고 접수 품종은 ‘노나리’(Namnong, Korea)를 사용하였다. 방울토마토 육묘를 위해 접목할 대목 및 접수 종자는 2019년 7월 4일에 파종하였고 실생묘는 접목묘와 같은 식물체 크기로 정식하기 위해 일주일 후인 7월 11일에 파종하였다. 파종 21일 후 접수 ‘노나리’에 대목 품종 4종류를 합접법을 사용하여 접목하였다. 접목 직후 온도 24°C 및 습도 80% 이상을 유지한 접목 활착실에 6일간 처리하였다.
2. 식물재배 및 재배환경
본 실험은 전북 정읍에 위치한 폭 7m, 길이 110m, 측고 4.5m 및 동고 6m 크기의 연동형 비닐하우스에서 수행하였다. 방울토마토 접목한 4개의 처리구와 접목하지 않은 1개의 처리구를 15주씩 3반복 난괴법으로 배치하여 2019년 8월 24일에 정식하였으며 2020년 5월 22일까지 수확하였다. 거터 사이는 160cm, 주 간 거리는 25cm로 재식거리를 두어 코코피트 배지(Duck Yang Coco, Korea, 가로 20cm, 세로 100cm, 높이 10cm)에 정식하였다. 실험에 사용한 배양액은 pH 6.0, EC 1.8dS·m-1 수준으로 조정한 Yamazaki 토마토 배양액[KNO3 40.4kg, Ca(NO3)2·4H2O 35.4kg, NH4H2PO4 7.6kg, MgSO4· 7H2O 24.6kg, Fe-EDTA 1.53kg]을 사용하였으며, 온실 내부 평균온도가 15°C인 겨울철에는 EC를 2.4에서 2.5dS·m-1을 유지하였다. 배양액 공급은 자동공급장치(MAGMA 1000 V2.0, Green Control System Ltd, Korea)를 이용하였으며, 겨울철 급액은 하루 5회(80cc/주) 오전 9시 30분부터 일몰 4시간 전까지 급액하였고 증산량이 많은 여름철에는 하루 17회(100cc/주) 오전 8시부터 일몰 2시간 전까지 급액하였다. 방울토마토 식물체 관리는 정식 후 측지를 주기적으로 제거하고 엽수는 약광기에 15매에서 20매, 강광기에 10매에서 15매의 엽수를 유지하였다. 화방의 꽃 또는 과실은 12개에서 15개로 모든 처리구를 동일한 개수로 적화 또는 적과하였다. 온실 내부 온도와 일사량은 복합 환경 제어 시스템(MAGMA multivariable controller Ver 2.4, Green Control System Ltd, Korea)를 이용하여 수집하였다. 방울토마토 재배기간 동안 수집한 온실 내부 평균온도(Table 1)와 일일 평균적산일사량(Table 2)을 월별로 나타내었다.
Table 1.
Monthly average temperature during the experimental period in plastic greenhouse.
| Temperature (℃) | ||||||
| Dec. | Jan. | Feb. | Mar. | Apr. | May | |
| Temperature | 15.7 | 15.3 | 16.8 | 18.2 | 19.4 | 20.7 |
Table 2.
The monthly average of integrated solar radiation during the experimental period in plastic greenhouse.
| Integrated solar radiation (J/cm2) | ||||||
| Dec. | Jan. | Feb. | Mar. | Apr. | May | |
| Integrated solar radiation | 666.3 | 582.4 | 986.9 | 1477.1 | 1974.8 | 1757.3 |
3. 수확량 및 과실특성 조사항목 및 조사방법
방울토마토 수확량은 2019년 12월 6일부터 2020년 5월 22일까지 총 25주간 반복 당 5개체를 선택하여 과실이 착색되는 속도에 따라 1주에서 2주마다 조사하였다. 저온약광기에는 생육이 느려 2주마다 조사하였고 그 외 기간에는 1주마다 조사하였다. 수확한 방울토마토는 개체별로 개수, 과중, 당도, 과경 및 과폭을 측정하였다. 과중은 전자저울(KS-308, DRETEC, Japan)로 조사하였으며 당도는 당도계(PR-32a, ATAGO, Japan)로 조사하였고 과경 및 과폭은 디지털 버니어 캘리퍼스 300mm(IP67, FUTURO, Switzerland)를 이용하여 수확한 과실 5반복을 조사하였다.
4. 생육조사 항목 및 측정방법
방울토마토 생육조사는 생육초기와 생육후기로 나누어 개화위치, 생장강도, 개화속도, 엽장 및 엽폭을 조사하였다. 생육초기의 생육조사는 정식 후 62일에 시작하여 3주 동안 7일 간격으로 조사하였고 생육후기의 생육조사는 정식 후 252일에 시작하여 3주 동안 7일 간격으로 조사하였다. 개화위치는 한 개 이상의 만개한 꽃이 있는 최상위 화방과 생장점 사이 길이를 측정하였다. 생장강도는 7일 전 생장점이 있던 위치를 표시한 유인줄의 줄기 직경을 측정하였으며 측정할 부위가 마디라면 마디 바로 아랫부분을 측정하였다(Lee 등, 2020; Kim 등, 2010). 개화속도는 완전히 개화된 꽃 수를 7일 간격으로 측정하여 금주의 개화 수에서 전주의 개화 수를 뺀 값을 사용하였다(Lee 등, 2020; Kim 등, 2014). 생육조사를 하는 시기에는 화방당 15개의 꽃을 가지도록 적화하였고 전주에 1화방의 9번째 꽃까지 개화했다면 0.6으로 표현하였다. 금주에 2화방의 3번째 꽃까지 개화했다면 1.2로 표현하였다. 이와 같은 상황에서 개화속도를 계산하면 1.2에서 0.6을 뺀 값인 0.6을 개화속도로 나타내었다. 엽장과 엽폭은 개화한 최상위 화방의 하부엽의 정단엽의 가로와 세로 길이를 자로 측정하였다.
5. 엽록소형광변수 측정방법
생육후기에 방울토마토 처리 별 엽의 광합성 효율을 평가하기 위해 OJIP 엽록소형광을 측정하였다. OJIP 엽록소형광 측정은 정식 273일 후 휴대용 엽록소형광 측정기(Fluorpen FP-110, Photon Systems Instruments, Czech Republic)를 이용하여 측정하였다. 측정 시 개화한 최상위 화방의 하부엽의 정단엽을 대상으로 측정하였다. 잎은 다크클립을 사용하여 1시간 암처리 후 9반복하여 엽록소 형광을 측정하였다. 엽록소형광 측정 결과를 통해 OJIP 엽록소형광변수인 PIabs(전자수용체 환원의 정도)와 ETo/RC(광계2의 전자전달효율)을 산출하여 제시하였다.
6. 통계분석
통계분석은 R 프로그램을 이용하여 ANOVA(analysis of variance)를 통해 실시하였다. 평균 간 비교는 95% 신뢰수준에서 Duncan’s Multiple Range Test(DMRT) 검정을 이용하여 차이를 확인하였다.
결과 및 고찰
1. 방울토마토 수확량 변화
방울토마토의 주 당 평균 총 수확량을 조사한 결과 대목을 사용한 처리구 ‘B.blocking’, ‘T1’, ‘L1’의 수확량이 각각 3,347.2g, 3,270.2g, 3,248.6g 순으로 수확량이 높았으며, 대목 ‘파워가드’를 사용한 처리구와 대목을 사용하지 않은 처리구는 각각 3,120.6g, 3,044.3g으로 낮은 수확량을 보였다(Fig. 1). 이 같은 결과는 접목한 토마토가 접목하지 않은 토마토보다 높은 수확량을 보였다는 실험결과(Lee와 ODA, 2003; White, 1963)와 일치하였다. 대목 ‘파워가드’를 사용한 처리구가 가장 높은 수확량을 보인 완숙토마토품종 ‘감마’의 실험결과(Lee 등, 2020)와는 다르게 방울토마토품종 ‘노나리’에서는 대목 ‘파워가드’를 사용한 처리구가 대목을 사용한 처리구들 중 가장 낮은 수확량을 보였다. 접목묘은 대목과 접수 간의 친화성의 정도에 따라 작물성능(plant performance)이 다르다는 보고와 같이(Romano와 Paratore, 2001; Tiedemann, 1989; Yeoman와 Brown, 1976) 같은 ‘파워가드’ 대목을 사용하였음에도 수량을 나타내는 성능의 차이가 있는 이유는 접수와의 친화성 정도에 따른 결과로 판단된다.
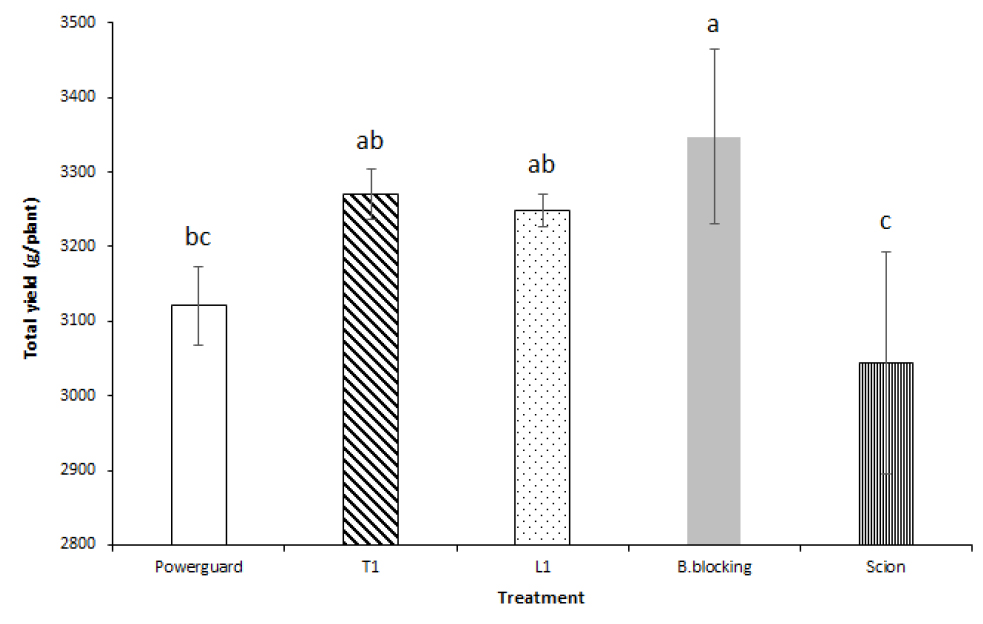
Fig. 1.
Total fruit yield of non-grafted and grafted cherry tomato plants. ‘Scion’ was used as non-grafted control, while 4 grafted cherry tomato plants ‘Powerguard’, ‘T1’, ‘L1’, and ‘B.blocking’ were used as rootstocks under plastic greenhouse. Different letters above bars indicate significant differences by Duncan’s multiple range test at p ≤ 0.05.
방울토마토의 월별 평균과중을 조사한 결과 12월의 평균과중은 17g 내지 19g을 보이다가 점차 감소하여 2월에는 10g 내지 14g의 평균과중을 보였다(Table 3). 2월 평균과중은 대목 ‘B.blocking’을 사용한 처리구의 과중이 14.2g으로 가장 높았고 대목을 사용하지 않은 처리구의 과중이 10.9g으로 낮았다(Table 3). 수확을 시작한 12월부터 2월까지 점차 과중이 줄어드는 이유는 12월부터 2월까지의 온실 내부 평균 온도가 방울토마토의 생육적온인 18°C 내지 25°C보다(RDA, 2018) 낮은 15°C 내지 16°C였기 때문이다. 낮은 온도조건에서 작물은 스스로 영양생장 하려는 경향이 있다(OMAFRA, 2010). 최적온도 이하의 온도에서 식물체 생장은 엽면적과 신엽의 발달속도가 느려지고 작물의 생장속도가 느려지면 수확량이 줄어드는 결과를 보인다(Schwarz 등, 2010). 대목은 저온에 내성이 있기 때문에(Schwarz 등, 2010) 2월의 평균과중에서 대목 ‘B.blocking’을 사용한 처리구는 생육적온 이하의 온도에서도 생장속도를 유지해 과중이 크게 감소하지 않은 것으로 판단된다. 3월의 평균온도는 생육적온인 18.2°C로 회복하여 3월과 4월의 평균과중은 14g 또는 16g으로 증가하였다(Table 3). 5월의 평균과중을 조사한 결과 대목 ‘B.blocking’을 사용한 처리구의 평균과중이 15.2g으로 가장 높았고 대목을 사용하지 않은 처리구는 13.9g으로 낮았으며 대목 ‘파워가드’, ‘T1’, ‘L1’을 사용한 처리구의 평균과중은 각각 14.1g, 14g, 14.4g으로 통계적으로 유의한 차이를 보이지 않았지만 대목을 사용하지 않은 처리구보다 과중이 높았다(Table 3). 접목한 토마토의 과중이 접목하지 않은 토마토의 과중보다 높다는 연구결과(Turhan 등, 2011)와 일치하였다.
Table 3.
Monthly average fruit weight of non-grafted and grafted cherry tomatoes.
방울토마토 월별 주 당 평균 총 수확량을 조사한 결과 수확 초기인 12월에는 실생 토마토가 467.3g으로 통계적으로 유의한 차이를 보이진 않았지만 처리구 중 가장 낮은 수확량을 보였다(Fig. 2). 완숙 토마토품종 ‘감마’의 경우 수확 초기인 12월에 실생 토마토 처리구가 중 가장 높은 수확량을 보인 결과(Lee 등, 2020)와는 달랐다. 방울토마토품종 ‘노나리’의 경우 접목 토마토를 사용하면 단기재배 시에도 수확 초기부터 높은 수확량을 얻을 수 있을 것으로 판단된다. 2월의 월별 수확량은 대목을 사용하지 않은 처리구보다 대목을 사용한 처리구의 수확량이 높았다(Fig. 2). 이는 2월의 경우 대목은 저온에 내성이 있어 생장속도를 유지해 일정 수확량을 유지한 것으로 판단된다. 3월은 온실 평균 내부온도가 생육적온으로 회복하고 일일 적산 일사량 또한 2월 대비 50% 높아져 수확량이 점점 높아졌다(Fig. 2). 5월의 주 당 평균 총 수확량을 조사한 결과 대목 ‘B.blocking’을 사용한 처리구는 417.5g으로 가장 높은 수확량을 보였고 대목을 사용하지 않은 처리구가 354.2g으로 가장 낮은 수확량을 보였다(Fig. 2). 이 같은 결과는 접목조합에 따른 식물체의 생장과 수량에 차이가 있다는 결과와 일치한다(Romano와 Paratore, 2001). 5월의 개화위치를 조사한 결과 대목 ‘B.blocking’을 사용한 처리구는 14cm 내지 17cm의 개화위치를 보인 반면 대목을 사용하지 않은 처리구는 10cm 내지 14cm의 개화위치를 보였다(Table 5). 5월 15일에 측정한 생장강도는 대목을 사용하지 않은 처리구의 생장강도가 8.43mm로 낮았다(Table 6). 접목하지 않은 대조구와 비교하여 토마토 대목에 접목한 가지는 초장, 줄기직경 및 뿌리 건물중이 증가하였다(Passam 등, 2005). 이는 작물 세력이 저하되어 수량 감소를 보이는 연구결과를(Ennis 등, 2005) 보아 대목을 사용한 처리구는 생육 후반기까지 작물의 생육이 왕성하여 실생 토마토보다 높은 수량을 얻은 것으로 판단된다.
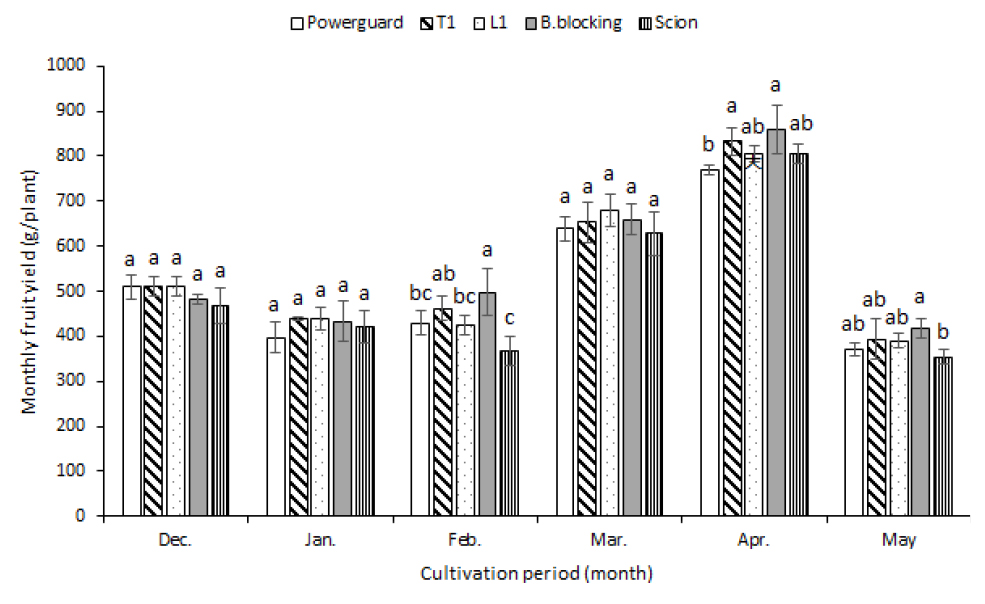
Fig. 2.
Monthly fruit yield of non-grafted and grafted tomato plants. ‘Scion’ was used as non-grafted control, while 4 grafted cherry tomato plants ‘Powerguard’, ‘T1’, ‘L1’, and ‘B.blocking’ were used as rootstocks under plastic greenhouse. Different letters above bars indicate significant differences by Duncan’s multiple range test at p = 0.05.
정식 후 240일에 대목을 사용하지 않은 처리구의 과경과 과폭은 36mm와 30.5mm로 대목을 사용한 처리구에 비해 낮았다(Table 4). 접목하지 않은 토마토의 과폭은 접목한 토마토의 과폭보다 작았다(Soe 등, 2018)는 실험결과와 일치하였다. 총 과실 개수를 조사한 결과 모든 처리구가 210에서 220개의 과실을 생산하였다. 총 과실 개수가 차이나지 않는 이유는 생육시기별로 동일한 개수로 적화 또는 적과했기 때문이다.
Table 4.
Fruit diameter, fruit length, sugar content, the total number of fruits of non-grafted and grafted cherry tomatoes.z
접목 토마토 ‘B.blocking’의 주 당 총 수확량은 3,347.2g이고 실생 토마토는 3,044.3g이다(Fig. 1). 10a 당 2,500주를 재배할 때 ‘B.blocking’은 8,368kg의 방울토마토를 생산해낼 수 있고 실생 토마토는 7,610kg을 생산해 낼 수 있다. ‘B.blocking’을 대목으로 사용한 토마토가 10a 당 758kg을 더 수확할 수 있어 방울토마토 대목을 사용하는 것이 농가 생산소득 증대에 도움이 될 것으로 기대된다.
2. 방울토마토 생장상 변화
개화위치를 측정하여 영양생장인지 생식생장인지의 작물 생장의 균형을 판단할 수 있고 줄기 직경(경경)을 측정하여 작물의 세력이 강한지 약한지를 판단할 수 있다(Lee 등, 2020; Stradiot과 Battistel, 2003). 정식 62일 후 생육초기의 개화위치를 조사한 결과 대목 ‘T1’을 사용한 처리구의 개화위치가 19.36cm로 다른 처리구에 비해 상대적으로 강한 영양생장을 보였다(Table 5). 정식 252일 후 생육 후기의 개화위치는 대목을 사용한 처리구인 ‘파워가드’, ‘T1’, ‘L1’, ‘B.blocking’은 각각 16.83cm, 17.34cm, 16.67cm, 17.6cm를 보였고 대목을 사용하지 않은 처리구의 개화위치는 14.25cm로 낮았다(Table 5). 정식 252일 후의 개화위치와 일주일 후인 정식 259일 후의 개화위치를 비교해보면 대목 ‘T1’, ‘L1’, ‘B.blocking’을 사용한 처리구의 개화위치는 2-6%의 감소율을 보였고 ‘파워가드’는 9%, 대목을 사용하지 않은 처리구는 11%의 감소율을 보였다(Table 5). 대목을 사용하지 않은 처리구가 생육 후기로 갈수록 생식생장으로의 전환이 다른 처리구에 비해 빠른 것을 볼 수 있다. 대목 ‘B.blocking’을 사용한 처리구의 생육초기 생육지표(개화위치:생장강도)는 16.17:11.07였다가 생육후기에 14.43:10.75의 생육지표를 보이며 처리구 중 가장 작은 생육지표의 변화를 보였다. 대목을 사용하지 않은 처리구의 생육초기 생육지표(개화위치:생장강도)는 16.58:10.39였다가 생육후기에는 10.56:8.43의 생육지표를 보이며 처리구 중 가장 큰 생육지표의 변화를 보이는 동시에 세력이 약하고 생식생장으로 전환된 모습을 볼 수 있다. 대목은 접목한 접수 식물체의 생장의 균형을 유지하여(Passam 등, 2005; Romano와 Paratore 2001; Bletsos, 2003) 생장상을 생육 후반기까지 유지하는 것으로 판단된다.
Table 5.
Flowering position of non-grafted and grafted cherry tomato plants.z
정식 66일 후 생육초기의 생장강도를 조사한 결과 모든 처리구가 9mm 내지 11mm의 생장강도를 보이며 처리 간 차이가 없었다(Table 6). 정식 252일 후 생육후기의 생장강도는 대목 ‘T1’을 사용한 처리구가 11.9mm로 가장 높은 값을 보였고 대목 ‘파워가드’를 사용한 처리구와 대목을 사용하지 않은 처리구의 생장강도는 각각 9.54mm와 9.24mm로 낮았다(Table 6). 약한 영양생장은 작물 세력 유지의 저하로 나타나 수량 감소를 보였다(Ennis 등, 2005). 4월과 5월에 대목 ‘파워가드’를 사용한 처리구와 대목을 사용하지 않은 처리구의 수량이 다른 처리구에 비해 감소한(Fig. 2) 이유는 작물의 세력을 오래 유지하지 못했기 때문이라고 판단된다.
Table 6.
Growth strength of non-grafted and grafted cherry tomato plants.z
정식 62일 후 생육초기의 개화속도는 1/주의 값을 보이다가 정식 252일 후인 생육 후기의 개화속도는 0.7/주로 개화속도가 느려졌으며 처리 간 차이는 없었다(Table 7). 토마토의 생장은 정식 후 약 75일까지 급격하게 증가하였다(Monte 등, 2013). 생장초기 단계에는 생장속도가 빠르게 변화하여(Stanghellini 등, 2019) 생육초기의 개화속도가 생육후기의 개화속도보다 빠른 것으로 판단된다. 생육초기의 생장강도는 10mm 내지 11mm의 줄기직경을 보이다가 일주일 후 9mm대의 줄기직경을 보였다(Table 6). 개화속도는 빠르지만 생장강도가 감소한 것은 생육초기에 작물세력이 약해진 것으로 환경관리를 통해 일정한 세력의 유지가 필요하다. 방울토마토 접수품종 ‘노나리’의 특성상 다른 품종보다 절간길이가 길어 초기에 세력이 약해보일 수 있다. 이때는 일 평균온도를 내리고 공급 EC를 낮춰주는 환경관리가 필요하다(OMAFRA, 2010). 시설 내 재배환경을 품종 특성에 맞춰 관리하는 것도 중요한 부분으로 간주된다.
정식 266일 후인 5월 15일에 엽장을 조사한 결과 대목 ‘T1’, ‘L1’, ‘B.blocking’을 사용한 처리구는 각각 8.55cm, 8.31cm, 8.51cm의 값을 나타냈고 대목 ‘파워가드’를 사용한 처리구와 대목을 사용하지 않은 처리구의 엽장은 각각 7.2cm와 7.23의 낮은 값을 나타냈다(Table 8). 접목한 머스크멜론은 접목하지 않은 처리구에 비해 생육 중기와 후기 단계에서 엽면적이 넓었다(Liu 등, 2011)는 실험결과와 비슷한 양상을 보였다. 접목을 함으로써 순광합성률이 증가되고 동화산물의 축적이 높아져 생장능력이 향상되었기(Liu 등, 2011) 때문이라고 판단된다.
Table 7.
Flowering rates of non-grafted and grafted cherry tomato plants.z
z62 days after planting, 252 days after planting. Flowering rates were expressed as subtracting ‘the number of fully-bloomed flowers last week’ from ‘the number of fully-bloomed flowers this week’. Each truss has 15 flowers, each flower was counted as 1/15. When all the flowers on that truss fully bloomed, it is ‘1’.
Table 8.
Leaf length and width of non-grafted and grafted cherry tomato plants.z
3. 생육후기의 엽록소형광변수
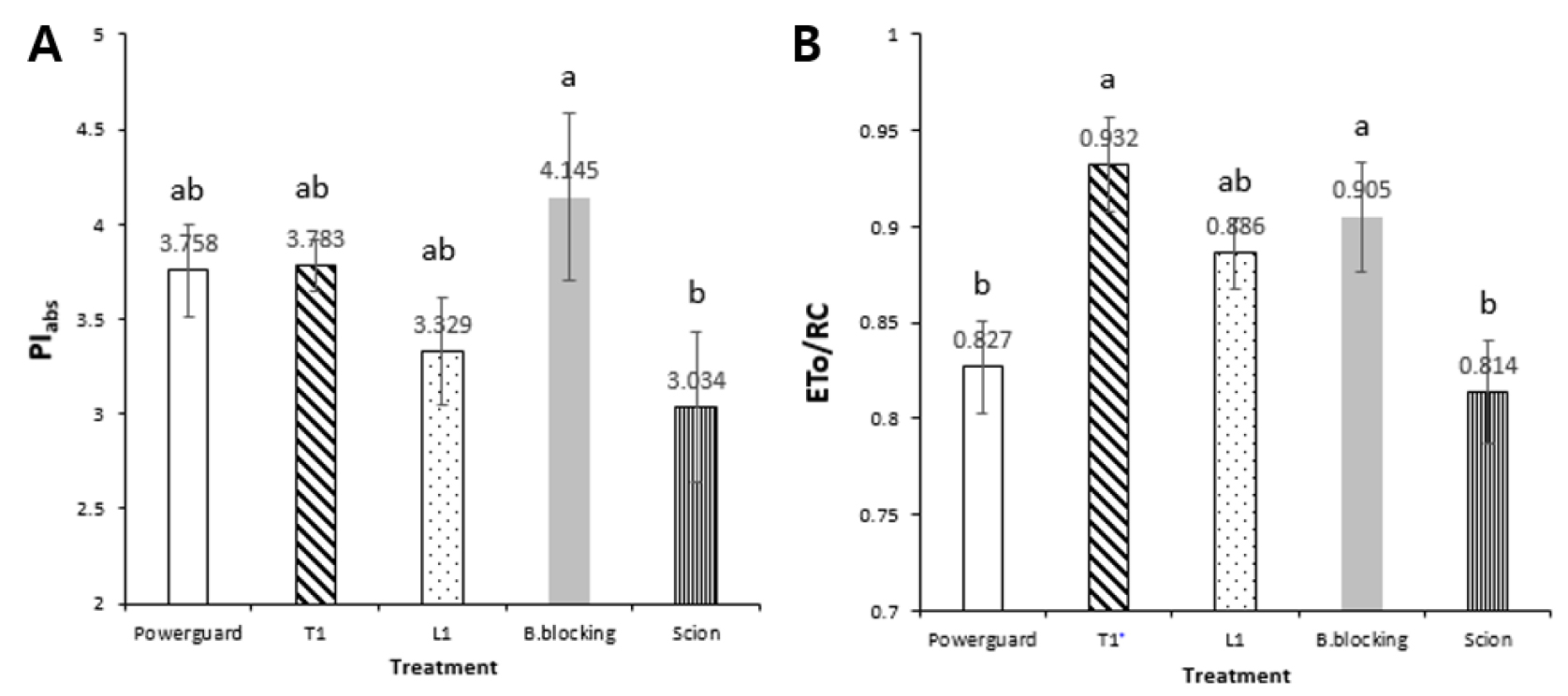
정식 273일 후(2020년 5월 22일)인 생육후기의 OJIP(엽록소형광유도곡선) 엽록소형광변수를 산출한 결과 PIabs는 대목 ‘B.blocking’을 사용한 처리구가 4.145의 가장 높은 값을 보였고 대목을 사용하지 않은 처리구는 3.034로 가장 낮은 값을 보였으며 대목 ‘파워가드’, ‘T1’, ‘L1’을 사용한 처리구는 통계적으로 유의한 차이를 보이지 않았지만 대목을 사용하지 않은 처리구보다 높은 PIabs값을 보였다(Fig. 3A). ETo/RC는 대목 ‘T1’과 ‘B.blocking’을 사용한 처리구가 각각 0.932와 0.905로 높은 값을 보였고 대목 ’파워가드‘를 사용한 처리구와 대목을 사용하지 않은 처리구가 각각 0.827과 0.814로 낮은 값을 보였다(Fig. 3B). PIabs는 광계2에 의해 흡수된 광자와 광합성계 내부의 전자수용체 환원 정도를 나타내고 광계1의 최종 전자수용체 환원 정도를 나타내는 지표임을 의미하며(Yoo 등, 2013) 작물 및 품종별 활력을 판단할 수 있는 지수로 쓰일 수 있어(Živčák 등, 2008) 광합성 기구의 전반적인 활력도를 나타내는 지수이다. 대목 ‘B.blocking’을 사용한 처리구의 활력도가 가장 높고 대목을 사용하지 않은 처리구의 활력도가 가장 낮다고 해석할 수 있다. ETo/RC는 반응중심 당 광계2의 전자전달효율을 나타내는 변수이다(Yoo 등, 2013). 대목 ‘T1’과 ‘B.blocking’을 사용한 처리구의 전자전달효율이 가장 높고 대목 ‘파워가드’를 사용한 처리구와 대목을 사용하지 않은 처리구의 전자전달효율이 가장 낮다고 해석할 수 있다. 접목을 함으로써 세포간극의 CO2 농도와 기공전도율을 높여 광합성 물질의 전달이 원활해 광합성 효율을 증가시키며 양수분 흡수능력이 향상돼 잎의 증산작용이 활발해지고, 엽록소함량과 엽면적이 증가되어 접목한 머스크멜론 잎의 순광합성률이 증가하였다(Liu 등, 2011). 포도나무 잎의 광합성률은 뿌리의 형태와 생화학적인 특성의 영향을 받아 수분이용 효율이 증가하여 기공전도율이 높아져 광합성률이 높아졌다는(Iacono 등, 1998) 보고와 일치한다. 접목한 토마토는 접목하지 않은 토마토보다 엽록소 함량이 높아 광합성 효율이 증가되고 이것은 작물 생장을 발달시키는 결과를 가져왔다(Soe 등, 2018). 접목묘은 대목과 접수 간의 친화성의 정도에 따라 작물성능(plant performance)이 달라(Romano와 Paratore, 2001; Tiedemann, 1989; Yeoman와 Brown, 1976) 대목 ‘파워가드’와 접수 ‘노나리’의 친화성은 낮은 것으로 판단된다. 5월의 월별 주당 평균 총 수확량(Fig. 2)과 엽록소 형광변수값(Fig. 3A, 3B)을 비교한 결과 대목 ‘B.blocking’을 사용한 처리구가 수확량, PIabs 및 ETo/RC 모두 높았다. 광합성 효율이 높은 처리구는 생장이 발달하여 수확량에도 영향을 미친 것으로 보인다. 위 실험 결과를 바탕으로 OJIP 엽록소형광변수 PIabs와 ETo/RC를 통해 광합성 효율을 판별해낼 수 있을 것으로 판단된다.