서 론
사과의 품질을 결정하는 요인에는 크게 맛, 크기, 색 등이 있으며, 그 중에서 착색은 소비자들을 유혹하는 중 요한 요소 중의 하나이다. 사과 과피의 착색은 유전적인 요인에 의해 가장 많은 영향을 받지만, 빛, 온도 등의 환경 요인에 의해서도 영향을 받는다(Ubi, 2004). 사과 과피의 착색은 일반적으로 고온조건에서 억제되고, 저온 조건에서 촉진되며(Xie 등, 2012), 여름 평균 온도가 높 은 지역에서 상대적으로 착색이 불량하게 나타난다 (Wang 등, 2011).
최근에는 지구 온난화로 인해 이상고온 현상이 증가하 면서 열대야 현상의 발생 빈도가 증가하고 있다(Park and Suh, 2011). 열대야는 야간 최저 기온이 25°C 이상으로 유지되는 밤을 의미하며, 2001년부터 2010년까지 평균 열대야 일수는 5.7일이고, Representative Concentration Pathways(RCP) 8.5에 의하면 21세기 말까지 연평균 55일 이상으로 증가할 것으로 예상되고 있다(Lee 등, 2012).
사과의 과실 비대는 주간온도보다 야간온도에 영향을 더 크게 받으며, 야간온도가 낮을 때 착색이 촉진된다 (Reay, 1999). 이는 사과의 주요 색소인 안토시아닌이 저온에서 합성이 촉진되기 때문으로(Ban 등, 2009), 사 과와 마찬가지로 안토시아닌을 주요 색소로 갖는 포도에 서도 야간의 고온으로 인해 착색이 불량해지는 것으로 조사되었다(Mori 등, 2005). 또한, 야간 온도에 따른 사 과 수체의 변화에 대한 연구가 상대적으로 부족하여, 열 대야 조건에서 나타나는 ‘후지’의 생리 반응에 대한 연 구가 필요한 상황이다.
따라서 본 연구는 생육기 후반기의 야간 고온이 ‘후지’ 사과에 미치는 영향을 구명하기 위해 성숙기의 과실 품 질과 시기별 안토시아닌 생합성 관련 유전자 발현량을 조사하였고, 잎과 과실의 유리당과 잎의 해부학적 특징 을 비교하여 야간 고온에 따른 생리반응을 구명하기 위 하여 수행되었다.
재료 및 방법
수원시 국립원예특작과학원내의 유리온실에서 화분에 재식한 3년생 ‘후지’/M.9 사과나무를 대상으로 2014년 7월부터 10월까지의 야간온도를 다르게 처리하여 진행하 였다. 주간에는 외기 온도와 동일하게 설정하였고, 야간 온도는 대기 온도와 동일한 처리구를 대조구로 하여 대 조구보다 야간 온도만 4°C를 낮춘 처리(‘-4°C 처리구’로 표시함)와, 대조구보다 야간온도만 4°C를 높인 처리 (‘+4°C 처리구’로 표시함)를 하여 대조구와 비교하였다. 야간 시간은 수원시 평균 일출, 일몰 시간을 계산해서 7~8월은 오후 8시부터 오전 6시, 9월은 오후 7시부터 오전 6시, 10월은 오후 6시부터 오전 7시로 설정하였다.
과실의 품질은 10월 30일에 일괄 수확하여 과중, 종경 및 횡경을 측정하였고, 주당 4과를 택해 과실을 착즙하여 당도와 적정 산도(0.1N NaOH, pH 8.1)를 조사하였다. 경도는 과실의 적도면에서 과피를 제거한 후 직경 8mm 의 probe를 장착한 Texture Analyzer(TA-XT2, Surrey, U.K.)로 분석하였다. 안토시아닌 함량은 과피를 지름 1.1cm 크기의 cork-borer로 뚫어 과실당 3~4개씩 총 10개 를 채취한 후, MeOH와 HCl을 85:15(v:v)로 혼합한 추출 액 30mL에서 15시간 추출하여 Spectrophotometer(UV- 2501PC, Shimadzu, Japan)로 530nm에서 측정하였다.
과피의 안토시아닌 생합성 관련 유전자의 발현을 분석 하기 위해 2주 간격으로 과피 시료를 채취하였으며, 과육 에서 분리하여 액체질소로 얼린 상태로 막자사발에서 분쇄 하였다. RNA 추출은 Jaakola 등(2001)의 방법을 일부 수정 해서 사용하였고, SuperscriptTM RT-PCR System(Invitrogen, Karlsruhe, Germany)으로 cDNA를 합성하였다. cDNA합성 을 위해 100ng의 RNA로 42°C 에서 반응시켰다. q- PCR은 QuantStudio Sequence Detection System(Applied Biosystems, Foster City, U.S.A.)으로 수행하였고, 최종 reaction volumne은 2μL의 cDNA template를 포함해서 총 10μL로 설정하였다. 실험에 이용한 primer와 reporter 1의 염기서열은 Table 1과 같다. PCR 조건은 95°C로 10분 후 95°C 15초, 60°C 1분의 40 cycles로 진행되었 다. 실험 결과는 Sequence Detector Software(Applied Biosystems)로 분석하였다.
Table 1.
Primer sets and reporter 1 sequences for q-PCR.
유리당 분석을 위해 처리가 시작되는 7월 첫째 주부터 2주 간격으로 한 주당 과실 1개와 잎 10장을 채취하였 고, 액체질소로 얼린 뒤 바로 동결건조 하였다. 과실은 과피를 제거하여 과육만을 사용하였고, 동결건조 후 곱게 갈아 유리당 함량 분석에 이용하였다. 유리당의 추출 과 정은 Colaric 등(2007)의 방법을 일부 수정하여 이용하였 고, 여과액을 Sep-pakTM C18 Cartridge(Waters, USA)를 이용해 한번 더 정제하였다. 이동상으로 증류수를 0.5mL/ min으로 흘리고 sugar-pak I 컬럼(6.5 × 300mm)을 이용하 여 HPLC(Waters, USA)로 분석하였다.
광학 현미경용 시료의 제작은 Park 등(2013)의 방법을 일부 수정하여 epon block을 만들었고, 초미세절편기 (Ultracut R, Leica Co., Germany)를 이용해서 1,500nm 두께로 가공하여 PAS(Periodic acid Schiff)법으로 염색, 광학현미경(Axioskop 2, Carl Zeiss Co., Germany)으로 관찰하였다.
모든 통계처리는 SAS 9.0 프로그램으로 Duncan의 다 중검정을 실시하여 처리간 비교하였다.
결과 및 고찰
1 고온처리에 의한 과실의 착색변화
야간 온도가 각각 다른 조건에서 재배된 성숙기 과실 을 비교한 결과, 과실의 착색에서 가장 큰 차이가 관찰 되었다. 안토시아닌 함량은 -4°C 처리구에서 가장 높았 고, +4°C 처리구는 대조구와 차이가 없었다(Table 2). 9 월 말부터 10월 말까지의 처리별 착색 모습을 살펴보면, -4°C 처리구가 처리구 중에서 가장 먼저 시작되어 성숙기 에 가장 진한 착색을 나타내었다(Fig. 1 and Table 2). 반 면 +4°C 처리구는 착색의 시작이 늦고, 착색을 제외한 품질 요인 중에서는 처리간의 차이가 관찰되지 않았다.
Table 2.
Fruit characteristics and quality of ‘Fuji’ apples at maturity under different night temperature conditions.
| Treatment | Fruit weight (g) | Diameter (mm) | Firmness (N) | SSC (°Bx) | Acidity (%) | AnthoCyanin concentration (μg cm-2) |
|---|---|---|---|---|---|---|
| Control | 212.0 a z | 79.3 a | 43.7 a | 15.9 a | 0.469 a | 1.21 b |
| Ambient-4°C | 282.7 a | 86.7 a | 39.1 a | 15.4 a | 0.421 a | 2.05 a |
| Ambient+4°C | 200.7 a | 77.8 a | 46.2 a | 13.5 a | 0.551 a | 1.26 b |
대조구와 -4°C 처리구의 과실 착색의 시작시기는 약 2 주 간의 차이를 보였으며, 야간의 온도 하락으로 인해 착색이 앞당겨지고 최종적으로 성숙기에 착색이 우수해 지는 효과를 확인하였다. 저온에 의해 착색이 빠르게 시 작되면 성숙기 과실의 착색이 좋았다는 ‘거봉’ 포도에서 의 연구결과와 일치하였다(Shim 등, 2007). 야간 저온이 착색을 향상시키는 것은 착색이 개시되는 시점을 앞당겨 안토시아닌이 합성되는 시기를 충분하게 확보해주는 효 과에 의한 것으로 판단되었다.
+4°C 처리구의 착색 불량은 야간 고온에 의해서 사과 의 착색이 억제된다는 기존의 보고와 일치하는 결과였으 며(Blankenship, 1987), ‘후지’에서도 동일한 결과를 보 였다. 하지만 횡경 및 과중 등의 과실품질에는 변화가 없었으며, 야간 고온에 의해 ‘북두’ 사과 과실의 크기, 과중 및 당도가 감소되었다는 보고와는 상반되는 결과를 나타내었다(Choi 등, 2001). ‘후지’의 경우 야간 고온에 의해서 착색이 큰 영향을 받지만 그 외의 품질 요인은 큰 차이가 없는 것을 확인하였다. 따라서 이상 기후로 인해 열대야의 발생 일수가 증가하고 야간 온도가 상승 하면 착색에 의한 품질하락이 가장 큰 문제가 될 것으 로 판단되었다.
2 안토시아닌 생합성 유전자 발현
사과 과피의 안토시아닌 생합성을 촉진시키는 전사인자 MdMYBA와 그 하위단계에서 전사되는 MdDFR, MdANS 및 MdUFGT의 발현량을 비교하였다(Fig. 2). -4°C 처리구 의 경우 모든 유전자의 발현이 9월 초부터 순차적으로 증가하였고, 특히 MdMYBA가 가장 먼저 증가하고, 뒤이 어 나머지 유전자들의 발현이 증가하였다. 한편, +4°C 처리구의 경우, 9월 전에 MdDFR, MdANS, MdUFGT의 발현이 먼저 증가했다가 다시 감소하였다.
이들 유전자의 발현은 +4°C 처리구에서 실제 착색이 일어나는 시기인 9월 이후부터는 상대적인 양이 감소하 였지만, 전체적으로 보았을 때 9월부터 10월에 걸쳐 대 조구와의 유전자 발현에 큰 차이가 없었다.
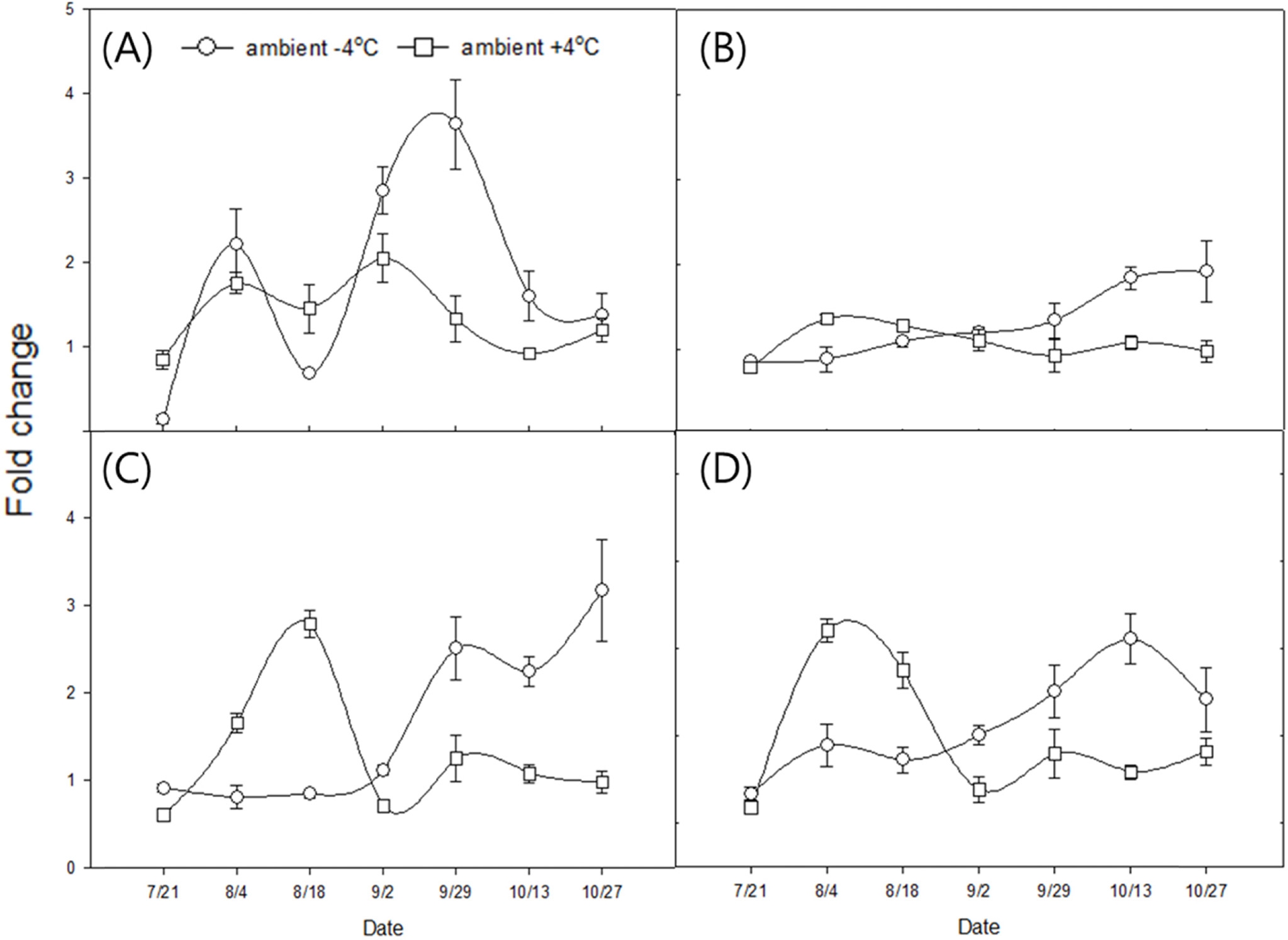
Fig. 2.
Fold changes in the expression of anthocyanin biosynthetic genes in temperature treated ‘Fuji’ apple fruit skins relative to those of control. Relative expression was determined with the 2-Ct algorithm with normalization against the apple UBIQUITIN gene. (A) MdMYBA, (B) MdDFR, (C) MdANS, and (D) MdUFGT. Mean separation within each columns by Duncan's multiple range test, 5% level.
-4°C 처리구에서 이들 유전자의 발현이 9월부터 증가 하기 시작하였고, 과피에서 특이적으로 발현되는 안토시 아닌 생합성 유전자의 전사인자 MdMYBA부터 생합성의 가장 마지막 단계에 있는 MdUFGT의 발현까지 모두 증 가하였다. 따라서 야간 저온에 의해 과피 착색이 좋아지 는 원인은 안토시아닌 생합성에 관련된 유전자의 발현이 과피의 착색이 촉진되는 시기에 증가했기 때문이고(Ban 등, 2007), 이는 저온이 안토시아닌 생합성 유전자의 발 현을 증가시켜 착색을 도왔다는 Ubi 등(2006)의 보고와 일치하였다.
야간 고온에 의해 만개 후 12주전까지 안토시아닌 생 합성 유전자의 발현이 높다가 이후 대조구의 수준으로 유지되었지만, 착색은 정상적으로 진행되지 못하였다. Wang 등(2011)은 고온에 의해 안토시아닌 생합성 유전 자의 발현이 감소했다고 보고했지만, 야간 고온처리는 주간의 고온처리처럼 안토시아닌 생합성 유전자의 발현 을 억제하지 못하였다. 따라서 야간 고온에 의해 착색이 불량해지는 것은 안토시아닌 생합성에 필요한 전사체의 양과는 관련이 없는 것으로 판단되었다. 처리가 시작된 7월부터 8월까지는 안토시아닌 합성에 대한 억제인자의 활성이 가장 높은 시기이고, 착색이 시작되기 전인 만개 후 12주전에는 Abscisic acid(ABA)나 ethylene 활성 대 비 Gibberellic acid(GA)활성에 의해 안토시아닌 합성이 억제되기 때문인 것으로 여겨진다. 따라서 야간 고온 처 리시 만개 후 12주 전에는 착색 과정에 영향을 미치는 다른 억제인자가 작용하게 되며, 이를 구명하기 위해 안 토시아닌의 전구물질인 안토시아니딘에 glucoside를 결 합시키는 MdUFGT 등의 분석이 필요하다고 판단되었다.
3 고온처리에 의한 과실과 잎의 당 함량
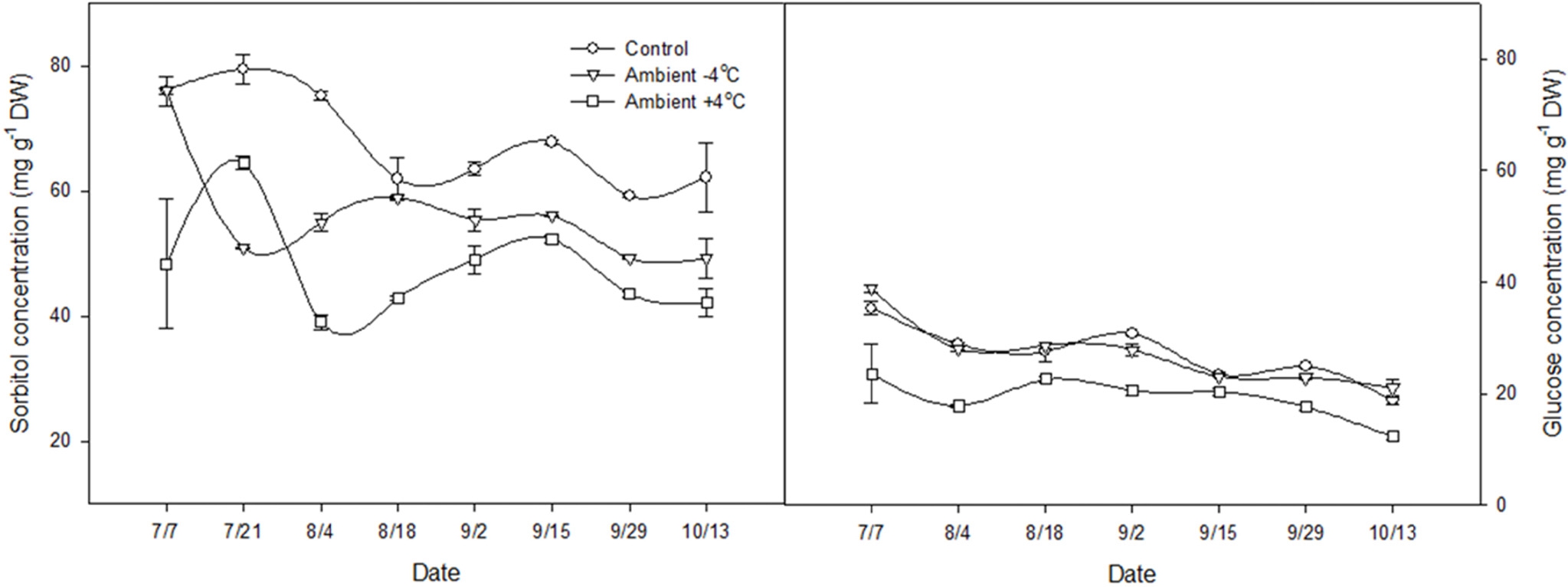
잎에 존재하는 유리당 함량의 시기별 변화를 조사한 결과, 전체 온도 처리기간 동안 sorbitol과 glucose 함량에 서 유의한 차이가 확인되었다(Fig. 3). Sorbitol 함량은 대 조구에 비해 +4°C 처리구와 -4°C 처리구가 모두 낮았고, 그 중에서도 +4°C 처리구의 sorbitol 함량이 가장 낮았다. 잎의 glucose의 함량은 대조구와 -4°C 처리구에서 차이가 없었지만, +4°C 처리구의 경우에는 대조구보다 낮았다.Fig .4
대조구와 -4°C 처리구는 책상 조직에서 전분립이 쉽게 관찰되었지만, +4°C 처리구에서는 거의 발견되지 않았다 (Fig. 5). 모든 처리구에서 잎 조직을 구성하고 있는 책 상, 해면, 유관속 및 표피조직의 형태는 차이가 없었다.
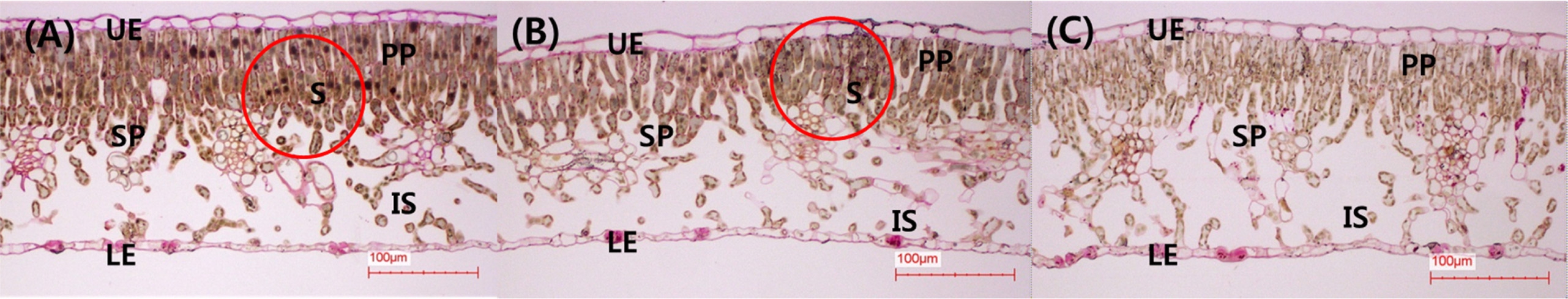
Fig. 5.
Cross sections of ‘Fuji’ apple leaves one month after the night temperature treatments. (A) control, (B) ambient -4°C, (C) ambient +4°C.The circles indicated the red colored starch granules located in the palisade parenchyma cells. IS, intercellular space; LE, lower epidermis; PP, palisade parenchyma; S, Starch; SP, spongy parenchyma; UE, upper epidermis.
사과의 잎에서 광합성 동화산물이 합성되면 약 60~70% 는 sorbitol의 형태로, 일부는 sucrose의 형태로 합성되어 각 sink 기관으로 전류가 일어난다(Bieleski, 1968). 본 실험에서도 ‘후지’의 잎에서 sorbitol이 유리당 중에서 가 장 많았고, 처리구중에서는 +4°C 처리구에서 양이 가장 적었으며 저장양분인 전분립이 존재하지 않았다. 멜론의 잎에서도 고온에 의해 전분과 당 함량이 감소하는 것으 로 보고되었으며(Acock 등, 1990), 야간의 온도가 높은 경우 호흡량이 증가해서 잎의 동화산물 소비가 많아져 동화산물의 이동과 축적이 감소하는 것으로 판단되었다.
Ro 등(2001)에 의하면 주야간을 모두 5°C씩 상승시켰 을 때 사과 잎의 전분함량이 증가하였지만, 본 실험의 결과 대조구와 -4°C 처리구에 비해 +4°C 처리구에서는 전분립을 거의 발견할 수 없었다. 이는 야간에만 고온이 작용하면 저장양분의 축적이나 전류가 일어나기보다는 호흡률의 증가가 더 커서, 양분의 소모가 많은 쪽으로 수체의 반응이 나타났다는 것을 의미한다.
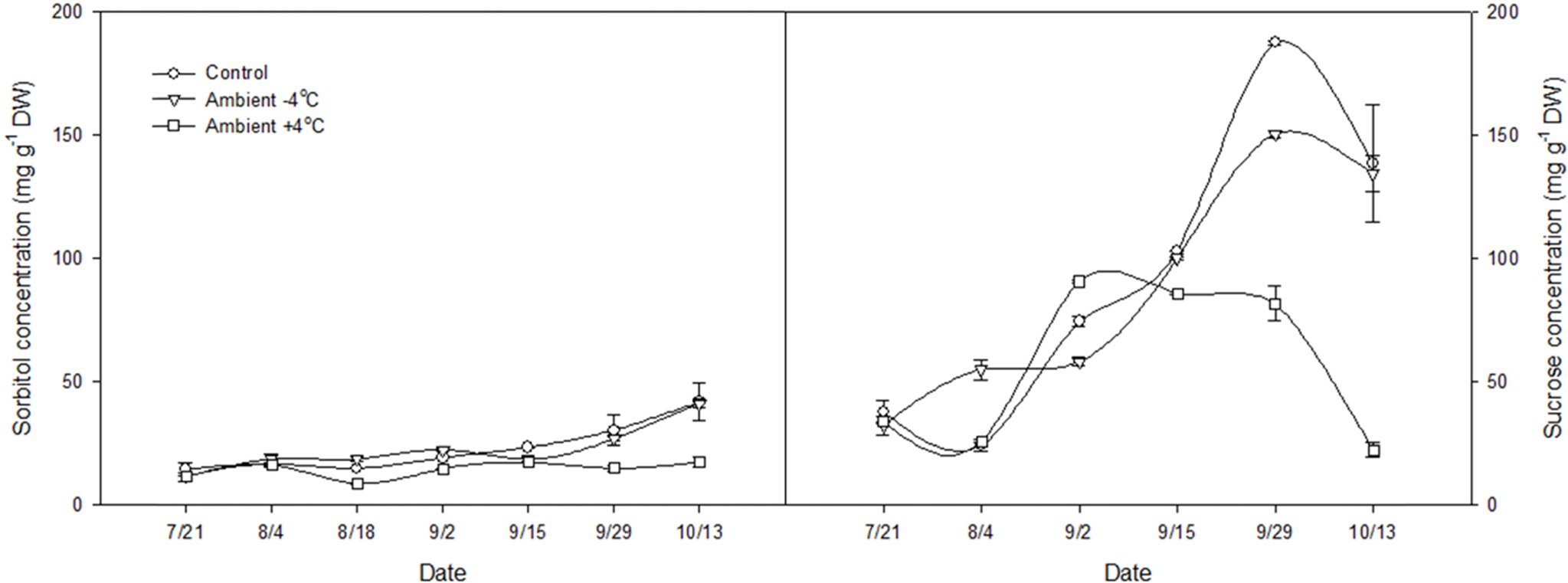
과육의 시기별 유리당 함량을 조사한 결과, sorbitol과 sucrose의 함량이 유의한 차이를 보였다(Fig. 4). 9월 중 순을 지나면서 과실의 sorbitol 값이 대조구와 -4°C 처리 구에서는 증가하는데 비해, +4°C 처리구는 비교적 일정 하게 유지되었다. 성숙기인 10월 13일에 +4°C 처리구의 sorbitol 함량은 대조구와 2배 이상의 차이를 보였다. Sucrose의 경우도 마찬가지로, 9월 중순을 기점으로 대 조구와 -4°C 처리구의 함량은 급격히 증가하는데 비해 +4°C 처리구의 함량은 오히려 감소하였다.
Sucrose는 과실의 에너지원으로서 중요할 뿐만 아니라, 안토시아닌 생합성을 촉진시키는 신호전달 물질로도 중 요한 역할을 한다(Ende and Esawe, 2014). Sucrose 특이 적인 신호전달은 세포의 칼슘 이온 흡수를 촉진시키고, 전사인자를 활성화시켜 안토시아닌 생합성 유전자의 발현 을 증가시킨다(Shin 등, 2013). 실제 과실의 sucrose 함량 은 사과 과피의 주요 안토시아닌인 cyanidin 3-galactoside 와 cyanidin 3-arabinoside 함량과 정의 상관관계가 있으며 (Liu 등, 2013), 야간 고온에 의해 과실의 sucrose 함량이 감소해 착색이 불량해졌을 것으로 생각된다.
야간 고온으로 인해 동화산물의 축적이 감소하였고, 잎과 과실의 당 조성에 변화를 나타내었다. 또한 안토시 아닌 생합성 유전자의 시기별 발현에 변화를 유발하였고 착색이 불량하였다. 야간고온에 따른 반응은 당해 년에 나타나기보다는 수년간 효과가 누적되는 경우에 나타나 므로 과실 품질의 하락이나 수체의 노화 등의 문제점이 발생할 가능성이 높기 때문에 이와 관련된 지속적인 연 구가 필요하다고 판단된다.