서 론
최근 인류는 과학기술의 발전에 힘입어 지구를 벗어나 달이나 화성 등의 태양계 천체와 심우주로의 본격적인 탐사 및 장기적 정착에 관한 계획을 구체화하고 있다. 이에 따라 단기 임무 수행을 위한 일시적 체류를 넘어 인간이 우주 공간에서 지속 가능하게 생존하고 자립할 수 있는 생명지원시스템에 관한 기반 기술이 확보되어야 미래 우주 탐사가 가능해질 것이다(Lee 등, 2021). 이러한 기술에는 식량, 산소, 물 등 생존에 필수적인 자원의 지구 의존도를 낮추고 우주 공간 혹은 임무 수행하는 외계 행성에서 자원을 자체적으로 생성·재활용할 수 있는 현지자원활용기술(In situ resource utilization; ISRU)의 발전이 선행되어야 한다. 특히 최근 우주 거주지 건설과 생명지원시스템(Life Support System, LSS) 개발이 활발히 논의되는 가운데 인류가 지구 밖 환경에서 장기간 체류하기 위해서는 자급자족이 가능한 밀폐생태계 생명지원시스템(Closed Ecological Life Support System, CELSS)의 구현이 필수적이다(De Micco 등, 2023). CELSS는 LSS의 하위 개념으로 생명 유지에 필요한 물, 산소, 식량 등을 내부 생태 순환을 통해 재생·공급하는 생물재생형 생명지원시스템(Bioregenerative Life Support System, BLSS)을 포함한다.
이러한 시스템은 인간이 실제로 거주하게 될 우주 기반 인프라(space-based infrastructure)에 적용되며 이는 인류의 생존과 활동을 지속하기 위해 구축되는 궤도 및 표면 거주 구조물을 포괄한다. 대표적으로 국제우주정거장(ISS) 과 달 궤도 정거장(Gateway) 이 단기적 유인 인프라에 해당하며(Fuller 등, 2022), 장기적 계획으로는 ESA의 Moon Village와 중국-러시아 공동의 International Lunar Research Station (ILRS) 프로젝트가 국제 협력에 기반한 자립형 달 거주지 건설을 목표로 추진되고 있다(ESA, 2016). 이러한 인프라는 단순한 무인 탐사 모듈이 아니라 인간이 직접 체류하며 물, 산소, 식량을 자율적으로 순환·재생할 수 있는 유인형 생태 인프라로 설계되고 있다.
우주는 인간을 포함한 생명체에게 필수적인 중력, 대기, 온·습도, 수분, 방사선 차폐 등의 조건이 대부분 결여된 극한 환경으로 생물학적 생존이 구조적으로 제한된다. 특히 중력 저하, 밀폐 공간, 높은 방사선, 급격한 온도 변화 등은 인간 외에도 식물과 미생물의 생존 및 기능 유지에 치명적인 영향을 미친다(Horneck 등, 2010). 더불어 지구 환경에서 당연하게 제공되는 적정한 수준의 대기압, 상대습도, 광, 이산화탄소 농도 등 다양한 환경 인자들이 우주에서는 부족하거나 완전히 결여되어 있다. 이러한 제약 속에서 식물의 정상적인 생장과 광합성을 유지하는 것은 매우 어렵다(Maffei 등, 2024).
복합적인 환경 스트레스를 극복하고 생명체의 생존을 가능하게 하기 위해 우주 내 생명유지시스템(Life Support System, LSS)은 기압, 온도, 습도, 광, 이산화탄소 등 생명 유지에 필요한 물리적 환경을 인위적으로 조절·유지하는 기술 기반 시스템으로 발전해 왔다(Ewert 등, 2012). 최근에는 물리·화학적 방식의 한계를 보완하기 위해 식물과 미생물의 생물학적 기능을 활용한 생물재생형 생명유지시스템(Bioregenerative Life Support System, BLSS) 이 차세대 우주 거주 기술로 주목받고 있다(Liu 등, 2021).
NASA의 Veggie 프로젝트나 ESA의 MELiSSA 프로그램 등은 주로 정상 기압 조건에서 식물을 활용한 산소 생성, 이산화탄소 제거 수분 순환 등의 BLSS 구성요소를 검증해 왔다(Lasseur 등, 2010; Massa 등, 2016). 그러나 실제 우주 거주 환경에서는 발사체 구조적 제약과 에너지 절약을 위해 저기압 상태(low-pressure condition) 로의 운용이 불가피하며 이는 인간과 식물 모두의 생리적 반응에 직접적인 영향을 미친다(Maffei 등, 2024). 그럼에도 불구하고 저압 환경을 LSS의 설계 변수로 다룬 연구는 매우 제한적이며 기존 연구 대부분은 정상 기압을 기준으로 한 폐쇄형 생태계 유지 실험에 집중되어 있다. 따라서 향후 달 기지, 화성 기지와 같이 장기 체류가 요구되는 임무 환경에서는 저기압 상태에서도 안정적으로 작동 가능한 BLSS 구현이 필수적이다.
이러한 필요에 따라 최근에는 식물 생장에 영향을 미치는 다양한 환경 요소(기압, 온도, 습도, 광도, CO2 농도 등)에 대한 기초 연구가 수행되고 있다 (Lembo 등, 2025). 저기압 환경은 기체 교환의 물리적 제약을 초래하며 결과적으로 기공 전도도 감소, 수분 스트레스 증가, 광합성 효율 저하 등으로 이어질 수 있다. 또한 세포 내 압력저하, 수분 이동성 변화, 이차 대사물질 생산 조절 등 식물의 구조적·생리적 반응 전체에 복합적인 영향을 미치는 요소로 작용한다(Zhou 등, 2020).
기압과 관련하여 지상 저기압 챔버를 활용한 다양한 식물 재배 실험이 수행된 바 있으며 일부 연구에서는 저기압 조건이 식물 생장 저해 및 생리적 스트레스를 유발할 수 있다는 근거를 제시하고 있다. 그러나 대부분의 연구는 단기 실험이거나 특정 작물에 국한되어 있어 다양한 식물 종을 대상으로 우주 환경을 모사한 조건에서 장기간에 걸친 정량적 시계열 분석을 수행한 사례는 매우 제한적이다. Stutte 등, (2022b)은 지상에서 수행된 실험을 통해 67kPa 및 33kPa의 저기압 조건에서 상추(Lactuca sativa)의 엽면적 및 생체량이 20-41% 감소하였음을 보고하였으며, 이러한 생장 저해는 우주 환경 하에서 식물 생장 안정성 확보의 어려움을 시사함과 동시에 장기간 정량적 분석 기반의 연구 필요성을 제기한 바 있다.
본 연구는 외계 거주지(달, 화성 등)에서의 식물 재배 모듈 내 저압 환경 조건이 생육에 미치는 영향을 규명하고 이를 통해 BLSS 구성요소로서의 식물 시스템 최적화에 필요한 기초자료를 제공하고자 한다.
본 실험은 밀폐형 저기압 식물 생장 챔버를 이용하여 표준 대기압(101.3kPa)과 비교 시 저압 조건(67kPa, 33kPa)이 케일의 생육에 미치는 영향을 정량적으로 평가하였다. 두 수준의 압력은 NASA의 선행연구 Stutte 등, (2022a)를 참고하여 설정하였으며 해당 연구에서는 “33kPa 및 67kPa 환경이 향후 우주 거주지의 감압 조건을 모사하기 위해 선택되었다”고 명시되어 있다. 실제로 NASA의 유인 달 탐사 임무에서는 70.3kPa 또는 56.5kPa 수준의 운용 기압이 제시되고 있다.
본 연구의 67kPa 조건은 실질적 운용 범위, 33kPa 조건은 극한 저압 환경에서의 식물 생리 반응 평가 구간으로 설정하였다. 따라서 본 연구는 달이나 화성 등 외계 천체의 저압 환경을 모사하여 이러한 조건이 식물의 생리적·형태적 반응에 미치는 영향을 규명하고자 한다. 이를 통해 외계 표면에서의 작물 재배 가능성과 생육 한계 범위를 실험적으로 평가하고, 향후 우주 농업 기반 생명유지시스템(BLSS)의 환경 설계에 필요한 생리적 기준을 제시하고자 한다.
재료 및 방법
1. 식물 재료 및 초기 생육 조건
본 실험에서는 케일(Brassica oleracea var. acephala)을 사용하였으며 밀폐형 환경에서 초기 생육은 인위적 환경 제어가 없는 기초 온실에서 수행하였으며 온도, 상대습도, 광량, CO2 농도는 자연 조건에 따랐다. 2024년 7월 1일부터 15일까지 약 2주간 육묘를 진행하였으며 이 기간 동안 발아 후 본엽 발생 전까지 매일 오전 10시에 정제수 20mL를 관수하였다. 이후 떡잎이 완전히 전개되고 본엽이 초기로 분화되는 개체를 선별하여 저압 식물 생장 챔버로 이식하였다.
2. 실험 설정 및 성장 챔버 설계
본 실험은 폐쇄된 저기압 환경에서 서로 다른 기압 조건이 케일의 생육에 미치는 영향을 정량적으로 분석하기 위해 수행되었다. 사용된 식물 생장 챔버는 연구 목적에 따라 자체 설계 및 제작된 장치로 구조는 Fig. 1 및 Table 1에 제시되어 있다. Fig. 2에 나타난 바와 같이 챔버는 두께 12mm의 투명 아크릴 (PMMA)로 제작된 직경 18.0cm, 높이 32.4cm의 원통형 구조이다. 상단은 동일한 소재의 아크릴 덮개로 밀폐하였고, O-링을 삽입하여 기밀성을 확보하였다. 총 6개의 챔버를 사용하였으며 2개씩 세 그룹으로 나누어 세 가지 압력 조건(101.3, 67.0, 33.0kPa)에 각각 배정하였다. 압력 조건은 대기압(101.3kPa)을 기준으로 100%, 67%, 33% 수준으로 설정하였다(Stutte 등, 2022a).
Table 1.
Specifications of components used in the low-pressure plant growth chamber.
챔버는 동일한 실내 공간에 배치하여 외부 환경의 영향을 최소화하였으며 압력 조절 시스템은 시판 부품을 조합하여 구성된 맞춤형 시스템으로 챔버 측면에 설치된 수동 볼 밸브(ball valve)를 이용하여 내부 공기를 배출하는 방식으로 운용되었다. 내부 기압은 매일 오전 10시에 수동으로 측정 및 조절하였으며 목표 압력 범위인 ±5% 이내로 유지되도록 관리하였다. 압력 측정은 챔버 외벽에 부착된 기계식 진공 게이지(DIA-60Φ, -0.1 MPa 범위, Japan Gauge Co., Japan)를 통해 실시간으로 수행하였다. 온실 내 평균 온도는 23.02 ± 2.20°C였으며 별도의 제습 또는 가습 장치는 사용하지 않았다. 광원은 적색(660nm)과 청색(450nm) LED를 4:1 비율로 혼합한 LED 스트립을 각 챔버 외벽에 두 바퀴 감아 설치하였다. 광량은 광합성유효광량(Photosynthetically Active Radiation) 기준 150μmol·m-2·s-1로 설정하였으며 LI-190R 광량 센서(LI-COR Biosciences, USA)를 이용하여 챔버 중심부에서 측정하였다. 광주기는 디지털 타이머(AC 220V, 정격 30A, DHC Co., Korea)를 사용하여 오전 6시부터 오후 6시까지 12시간 광주기(photoperiod), 이후 12시간 암기 조건으로 자동 제어하였다(Llewellyn 등, 2023). 모든 챔버에 동일한 수분 조건이 적용되었으며 실험 1일차(Day 1) 및 9일차(Day 9)에 각 개체당 정제수 20mL를 수동으로 직접 관수하였다. 실험 종료일까지 추가 관수나 배수는 실시하지 않았다.
3. 데이터 수집
생육 평가는 Day 1, 9, 19의 세 시점에 수행되었다. 측정은 챔버 상단 개방 후 측정하여 외부 환경 변화의 영향을 최소화하였다. 각 챔버 내 대표 개체의 완전히 전개된 잎을 대상으로 잎 길이(엽장)와 잎 폭을 디지털 캘리퍼스(Absolute Digimatic Caliper, Mitutoyo, Japan)를 사용하여 mm 단위로 측정하였다. 각 개체당 3회 반복 측정 후 평균값을 사용하였으며 처리구별로 총 6개체(n=6)를 평가하였다. 엽록소 함량은 동일한 대표엽의 중심부 및 엽맥 사이 영역에서 SPAD-502Plus (SPAD-502Plus, korica Minolta, Japan)를 이용해 비파괴 방식으로 측정하였다. 각 개체당 최소 3개 지점을 반복 측정하고 평균값을 대표값으로 사용하였다. 측정은 실험이 진행될 때 18시에 수행하여 광도 및 온도 변화에 의한 오차를 최소화하였다.
본 실험에서는 총 6개의 밀폐형 챔버를 사용하여 3가지 기압 조건(103.3, 67, 33kPa)에 각각 2개 챔버씩 배정하였다. 각 챔버 내에는 3개의 식재 포트가 설치되었으며, 포트당 2주의 상추가 식재되어 챔버당 총 6개체가 배양되었다. 이에 따라 처리구별 총 12개체가 배정되었으며 이 중 생육 지표 평가는 각 개체 하나당 잎 하나를 선정하여 수행하였다.
각 챔버의 내부 압력은 외부와 연결된 이중 볼 밸브를 통해 초기 감압 후 휴대용 다단식 진공 펌프(Handheld Vacuum Pump, 4PV-10, Diagraph Corporation, USA)를 이용하여 설정 기압까지 낮추었다. 감압이 완료된 후에는 밸브를 닫고 챔버를 밀봉하여 내부 압력을 유지하였으며 압력 변화는 내부에 부착된 진공 게이지를 통해 모니터링하였다.
생육 평가는 Day 1, 9, 19의 세 시점에 수행되었으며 챔버 상단을 개방한 후 빠르게 측정하여 외부 환경 변화의 영향을 최소화하였다. 대표 개체의 완전히 전개된 잎을 대상으로 잎 길이와 잎 폭을 디지털 캘리퍼스 (Absolute Digimatic Caliper, Mitutoyo, Japan)를 사용하여 mm단위로 측정하였다. 각 개체당 3회복 반복 측정 후 평균값을 사용하였다.
엽록소 함량은 동일한 대표엽의 중심부 및 엽맥 사이 영역에서 SPAD-502Plus (korica Minolta, Japan)를 이용해 비파괴 방식으로 측정하였으며 각 개체당 최소 3지점을 반복 측정하고 평균값을 대표값으로 사용하였다. 모든 측정은 실험이 진행되는 날의 18시에 수행하여 광도 및 온도 변화에 의한 오차를 최소화하였다.
4. 통계 분석
모든 생육 데이터는 IBM SPSS Statistics 26.0 소프트웨어를 사용하여 분석하였다. 압력 조건(101.3, 67, 33kPa)에 따른 생육 특성의 차이를 검정하기 위해 단일요인 분산분석을 하였으며 유의수준은 p<0.05로 설정하였다. 유의한 차이가 나타난 항목에 대해서는 처리 간 평균 차이를 명확히 구분하기 위해 Duncan의 다중 범위 검정을 사후검정으로 수행하였다. 분석 결과는 평균 ± 표준편차로 나타내었으며, 유의한 차이가 있는 경우 a, b, c로 서로 다른 영문을 추가하여 시각적으로 구분하였다.
결과 및 고찰
본 연구에서는 서로 다른 기압 조건(101.3, 67, 33kPa)에서의 케일 생육 반응을 분석하고자엽장, 엽폭, 엽록소 함량을 1일차, 9일차, 19일차에 걸쳐 측정하였다. 단일요인 분산분석을 실시하였으며 실험 초기인 1일차에는 세 그룹 간 모든 지표에서 유의수준은 p<0.05로 설정하여 실험군 간 동질성이 확보되었음을 확인할 수 있었으며 이후 관찰된 생육 변화는 기압 조건에 따른 차이로 해석할 수 있는 근거가 된다.
Table2와 Fig. 3, Fig. 4를 보면 9일차에는 A 그룹(101.3kPa)과 B 그룹(67kPa)에서 엽장과 엽폭의 유의한 증가가 관찰되었으며, 특히 B 그룹은 엽장 38.65 ± 4.15mm, 엽폭 32.85 ± 3.70mm로 C 그룹(33kPa)에 비해 유의한 생장 향상을 보였다. 이는 중간 수준의 저기압 조건이 일시적으로 케일의 엽 생장을 자극하는 효과를 가질 수 있음을 시사한다.
Table 2.
Changes in leaf length, leaf width, and chlorophyll content of kale over time (Day 1, 9, and 19) under different pressure conditions (A = 101.3 kPa, B = 67 kPa, C = 33 kPa). Values are expressed as mean ± standard deviation (n = 3). Different letters within the same column indicate significant differences among means (p < 0.05).
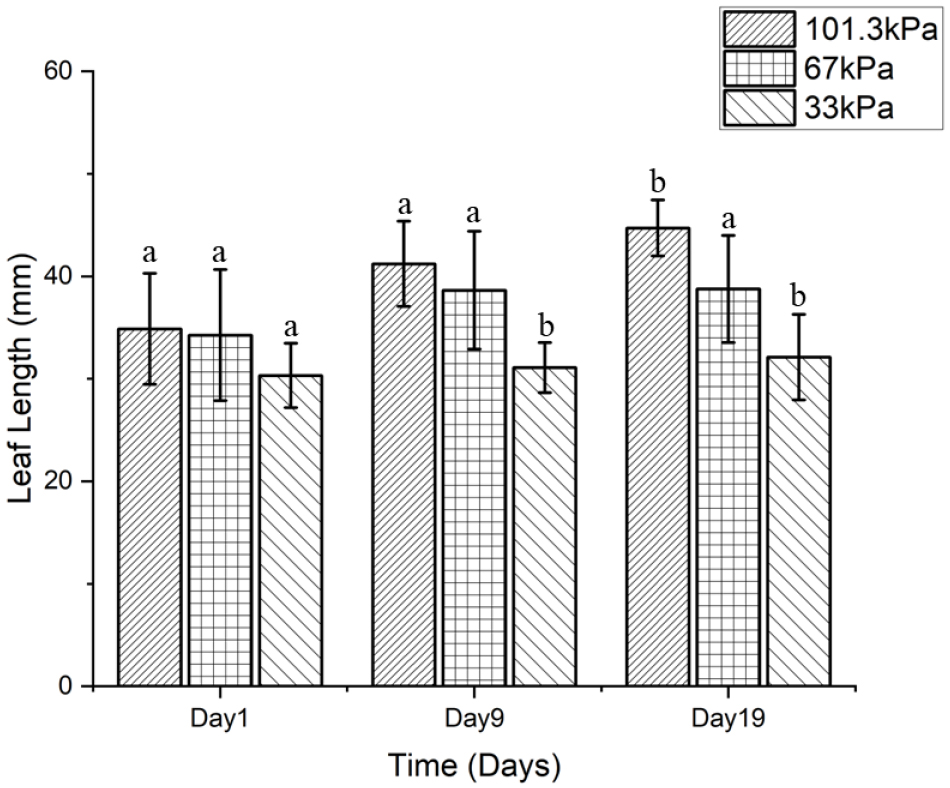
Fig. 3.
Changes in leaf length of kale under different pressure conditions. Leaf length was measured on Days 1, 9, and 19 after treatment. The experimental groups included atmospheric pressure (101.3 kPa), moderate hypobaric condition (67 kPa), and low pressure (33 kPa). Error bars represent mean ± standard deviation (n = 3).
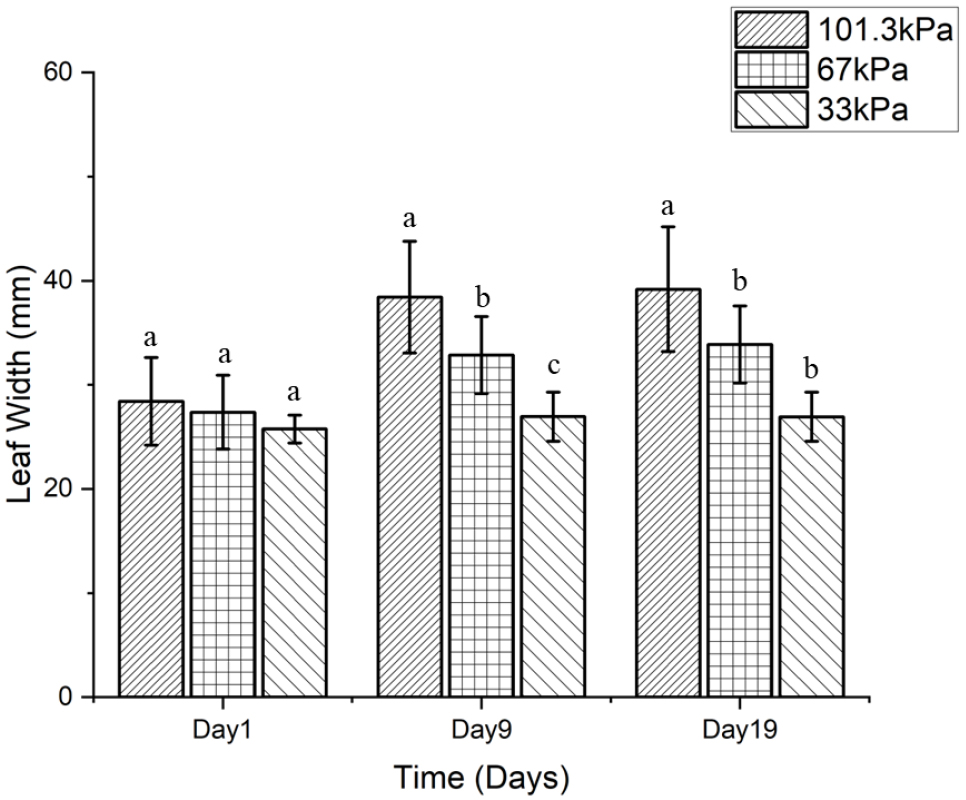
Fig. 4.
Changes in leaf width of kale under different pressure conditions. Leaf width was measured on Days 1, 9, and 19 after treatment under three atmospheric pressure conditions: ambient pressure (101.3 kPa), moderate low pressure (67 kPa), and low pressure (33 kPa). Error bars represent mean ± standard deviation (n = 3).
19일차에는 A 그룹에서 엽장이 44.72 ± 2.74mm, 엽폭이 39.19 ± 5.99mm로 가장 높았으며, B 그룹 또한 비교적 우수한 생장을 유지하였다. 반면, C 그룹은 엽장(32.11 ± 4.17mm)과 엽폭(27.36 ± 2.36mm)이 가장 낮은 수치를 기록하며, 저기압 환경에서의 생장이 장기적으로는 억제되는 경향을 보였다.
Table 2와 Fig.5를 보면 엽록소 함량(SPAD)은 실험 초기 단계에서 엽록소 함량이 증가하는 경향을 보였으며 특히 C 그룹(33kPa)에서 가장 높은 수치가 기록되었다. 이는 Tang 등(2010)의 연구 결과와도 부분적으로 일치하며 해당 연구에서는 상추를 40kPa의 저압 조건에서 35일간 재배한 결과 저압 처리구에서 잎의 황변이 적고 대기압 처리구에서는 엽색 황화가 나타났다고 보고하였다. 비록 본 연구에서 엽록소 함량이 직접 정량적으로 분석되지는 않았으나 잎 색의 유지 및 생육 안정성은 광합성 색소의 보존 및 축적과 밀접하게 관련될 수 있으며 이는 저기압 환경이 초기에는 광합성 활성을 촉진할 수 있음을 시사한다. 이러한 경향은 He 등(2003)에서 보고된 바와 같이 저기압 조건(50kPa)에서 상추의 생장이 촉진되고 엽면적과 생체량이 유의하게 증가했다는 결과와도 일치한다.
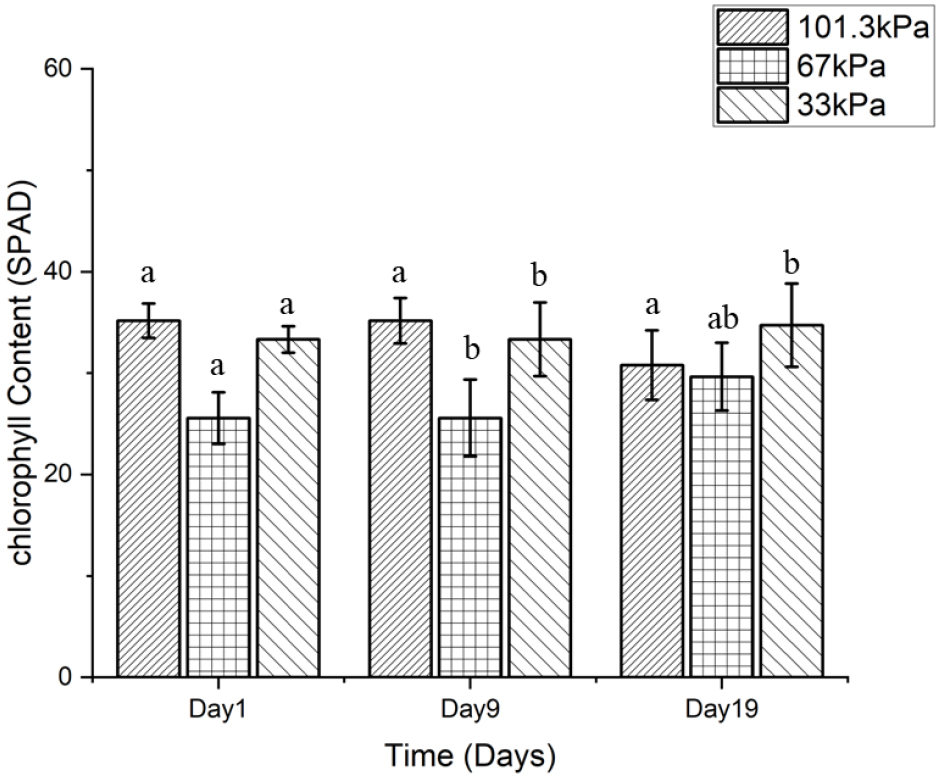
Fig. 5.
Changes in chlorophyll content (SPAD values) of kale under different pressure conditions. Chlorophyll content was measured on Days 1, 9, and 19 under three pressure treatments: atmospheric pressure (101.3 kPa), moderate low pressure (67 kPa), and low pressure (33 kPa). Error bars represent the mean ± standard deviation (n = 3).
본 실험에서 C 그룹의 엽록소 함량 증가는 이러한 단기 생리적 활력 촉진 반응의 일환으로 해석될 수 있으며 광합성 관련 지표와 생장 반응 간의 밀접한 연관성을 보여준다.
그러나 19일차에는 A 그룹(101.3kPa)에서 엽록소 함량이 30.33 ± 4.23 SPAD로 감소하였고 B 그룹(67kPa)도 일정 수준의 감소를 나타내며 전반적으로 하강하는 경향이 확인되었다. 반면, C 그룹(33kPa)은 실험 종료 시점까지 비교적 높은 엽록소 함량을 유지하였으며 초기의 생리적 활성이 지속되는 양상을 보였다. 이러한 결과는 Stutte 등(2022c)이 보고한 바와 같이 저기압 조건에서 엽록소 함량이 일시적으로 증가할 수 있으나 장기적으로는 생육이 억제되는 경향과 관련지어 해석할 수 있다. 비록 본 실험은 2주간의 단기 재배로 인해 C그룹에서의 엽록소 함량 감소는 관찰되지 않았으나 Stutte 등(2022c)의 보고에 따르면 장기 노출 시 광합성 효율 저하 및 엽록소 감소가 나타날 수 있음을 고려할 필요가 있다.
특히 C 그룹은 엽장과 엽폭의 증가가 둔화된 반면 엽록소 함량은 비교적 안정적으로 유지되었다. 이러한 결과는 생장이 억제된 조건에서도 광합성 관련 기작이 일정 수준 유지되었을 가능성을 시사한다. 하지만 에너지 재분배 또는 대사적 안정성과 같은 생리적 해석을 뒷받침하기 위해서는 추가적인 생체량, 광합성, 호흡 관련 지표가 필요하다. 이러한 경향은 Jagtap 등(2024)이 모사중력 환경에서 보고한 식물의 광합성 적응 및 에너지 분배 메커니즘과도 유사한 흐름을 보인다. 이러한 결과는 저압 환경이 단기적으로는 식물 생육 반응을 자극할 수 있지만 장기적으로는 광합성 능력 유지에 어려움이 있으며 생리 적 스트레스나 기질 제한 등의 요인으로 인해 생장이 억제될 수 있음을 시사한다.
한편, 본 연구에서는 생육 지표를 측정하는 데 버니어캘리퍼스를 사용하였으며 잎의 형태 변화, 처짐, 곡률 등으로 인해 측정 오차가 발생할 수 있는 한계가 존재한다. 따라서 향후 연구에서는 3D 스캐닝 기술이나 분광 광도계와 같은 정밀 계측 장비를 활용하여 생육 특성을 보다 정량적이고 일관되게 분석할 필요가 있다.
또한 본 연구는 습도, 온도, 광 등의 환경 요인을 일정하게 유지한 상태에서 기압만을 변수로 설정하였으나 실제 재배 환경에서는 다양한 환경 인자가 복합적으로 작용하므로 향후 연구에서는 기압과 광, 기압과 수분 등 복합 환경 요인에 따른 상호작용 효과를 함께 고려할 필요가 있다.
본 실험은 소규모 아크릴 챔버에서 수행되었으며 챔버 외부에 설치된 조명이 아크릴 벽면을 통과하고 식물체 상부를 직접 조명하는 방식이 아니기 때문에 이로 인해 일부 식물체는 동일 조건 내에서도 상대적으로 낮은 광량을 받을 가능성이 있다.
또한 본 챔버 시스템은 압력 조절 기능에 초점을 두고 설계되어 산소 및 이산화탄소의 정밀한 제어 기능이 포함되어 있지 않으며 기체 교환이 제한된 밀폐 구조로 인해 장기 실험에서는 기체 조성 변화가 식물 생리에 영향을 줄 수 있다. 따라서 향후 연구에서는 기체 조성, 조도 분포 등 환경 요소를 보다 정밀하게 제어할 수 있는 실험 시스템의 개발이 요구된다. 이러한 시스템은 장기 유인 우주 탐사 및 거주 미션에서 필수적인 생존 인프라 기술로 발전할 수 있으며, 우주 식량 생산 시스템의 자립성과 안정성 확보를 위한 기초자료로 활용될 것으로 기대된다.
선행 연구인 Chamberlain 등(2003)은 다양한 저기압 조건에서 피망(Capsicum annuum)을 대상으로 수분 포텐셜과 증산량을 측정한 결과 기압 저하가 수증기 확산 속도 및 VPD(증기압 포차)를 증가시켜 증산률을 유의하게 높였으며 10kPa 조건에서는 수분 포텐셜이 급격히 감소하는 생리적 스트레스 반응이 나타났다고 보고하였다. 이러한 결과는 기압 변화가 작물의 수분 대사 및 생장 안정성에 직접적인 영향을 줄 수 있음을 시사하며 본 연구에서 관찰된 저기압 조건에서의 생장 반응과도 연관 지어 해석될 수 있다.
결과적으로 밀폐된 환경에서의 압력 변화가 케일 생육에 미치는 영향을 분석한 본 연구에서는 대기압 조건(101.3kPa)에서 가장 안정적이고 지속적인 생장이 관찰되었으며 중간 수준의 저기압(67kPa)에서는 엽 생육이 일시적으로 증진되는 양상이 확인되었다. 반면, 저압(33kPa) 조건에서는 엽록소 함량 증가 등 일부 생리적 활성이 관찰되었으나, 엽장 및 엽폭의 생육은 현저히 저조하였고, 장기적으로는 엽록소 함량 감소 및 생장 저해가 나타날 가능성이 높은 것으로 판단된다. 이러한 경향은 Spanarkel과 Drew(2002)가 보고한 70kPa 조건에서의 상추 생육 안정화 사례와도 유사하며, 밀폐형 재배 시스템에서는 단순한 압력 조건뿐 아니라 노출 시간, 작물의 생리적 적응 과정 등을 종합적으로 고려해야 함을 시사한다.






