서 론
재료 및 방법
1. 식물재료
2. 재배조건
3. LED 처리
4. 조사항목
5. 통계처리
결과 및 고찰
1. LED 광질이 생장에 미치는 영향
2. LED 광질이 엽색에 미치는 영향
3. 생장과 엽색 간 상관관계 분석
서 론
바위솔속이라 불리는 Orostachys속 식물들은 예로부터 한방에서 약용식물로 활용되어져 왔다. 바위솔은 다량의 페놀을 함유하고 있고 항산화 효과가 있는 것으로 알려져 있으며(Yoo 등, 2006), 식물체를 있는 그대로 이용하거나 건조시킨 후 간염이나 지혈, 습진, 화상 및 항암 조절제로 활용해왔다(Shin 등, 1994). 또한 이와 유사하게 같은 돌나물과(Crassulaceae)과에 속해 있는 기린초(Sedum kamtschaticum)(Kim 등, 2004a), 속리기린초(S. zokuriense)(Lee 등, 2021b), 덴드로이데움(S. dendroideum)(De Melo 등, 2009)등도 약용식물로 이용된다. Orostachys속에는 공식적으로 전 세계에 12종이 있는 것으로 보고되었으며 추가 검토가 진행 중인 모든 종들을 합산할 경우 30여 종이 분포해 있는 것으로 알려져 있다(RBGK와 MBG, 2022). 이 중 바위솔(Orostachys japonica)은 화훼시장에서 주로 청와송, 와송 등의 이름으로 유통되며 자질연화바위솔(O. boehmeri)은 연화바위솔, 울릉연화바위솔 등의 이름으로 유통되고 있다. 이 두 종은 식물체가 작고 런너(runner)로 쉽게 번식하는 특성을 지녔으며, 밀식재배 시 우수한 관상 가치를 지녀 현대에 들어 이들은 약용식물로 활용되는 것만으로 그치는 것이 아니라 관상용식물로도 이용되고 있다. 바위솔속 식물들은 내건성이 우수하며(Chon 등, 2011), 암석원 및 옥상조경의 소재(Jeong 등, 2013) 등으로 사용하기 알맞으며 내음성 또한 준수하기 때문에 실내식물로도 활용이 가능할 것으로 전망된다.
일반적으로 바위솔속의 식물들은 2년생으로 이 중 바위솔과 먹바위솔(O. fimbriata)이 주로 국내에서 약용식물로 유통되며, 가을에 생체중이 가장 높은 시기에 시장에 출하된다. 그러나 이후 겨울철부터는 휴면에 들어가기 때문에 이 시기에는 지상부의 크기가 줄어들어 다시 일 년간 출하가 어렵게 된다. 특정 계절에 편중되어있는 바위솔의 출하를 조절하기 위해, 과거 일장조절에 따른 바위솔의 생장과 개화에 관한 연구(Kang 등, 2005b)가 있었다. 뿐만 아니라 바위솔의 차광 수준에 따른 생장과 개화에 관한 연구(Hong 등, 2006), 동절기 온도에 따른 바위솔의 생장과 개화 관한 연구(Kang 등, 2005a), 시비량에 따른 바위솔의 생장과 개화에 관한 연구(Lee 등, 2007) 등이 있었다. 바위솔속 식물들의 주년생산을 위해서는 일장효과에 대한 이해가 가장 중요하며 이와 밀접한 실내 light-emitting diode(LED) 재배에 관한 문제는 빼놓을 수 없다.
실내에서는 태양광만을 활용하여 식물을 생산하기는 어렵기 때문에 LED 등 인공광원이 이용되며 이러한 실내 재배시설에는 식물공장 시스템이 대표적이다. 식물공장은 외부환경과 관계없이 식물을 안정적으로 생산할 수 있다는 점에서 식량 확보와 자원 문제 해결, 희귀식물 자원의 보존과 같은 여러 가지 문제를 해결하는 데 기여할 수 있는 잠재력을 가지고 있다(Park과 Oh, 2021). 오늘날 적색, 녹색, 청색과 같은 단색광뿐만 아니라 2700, 3000, 4000, 4100, 5700, 6500K 등 다양한 백색광 LED가 시중에 폭넓게 보급되고 있으며, 비단 식물공장 시스템에서뿐만 아니라 각 개인 또한 실내에서 식물을 재배하기 위해 LED를 활용하기도 한다. 과거에는 주로 청색광 LED와 적색광 LED를 혼합하여 사용했으나, 보라색 LED를 사용하기도 하며(Xie 등, 2022), 최근에는 식물의 생장에 백색 LED가 더 우수하다는 실험 결과들이 보고되고 있어(Park과 Runkle, 2018; Phansurin 등, 2017), 백색 LED의 사용빈도가 많아지고 있는 추세다.
과거 LED 실험에서 돌나물과 식물과 석연화류(Echeveria spp.) 식물을 LED 하에서 다양한 광도로 재배했을 때 생장과 엽색의 변화에 관한 몇 가지 연구(Cabahug 등, 2017a; Cabahug 등, 2017b; Nam 등, 2016), LED 파장에 따른 석연화류의 엽삽에 관한 연구(Kim 등, 2018b), 오바타(Crassula ovata)의 동계기간 중 보광실험 등이 수행되었으나(Park 등, 2015), 아직 바위솔속 식물들의 LED 재배와 관련한 실험이나 LED 광질에 따른 다육식물의 생장과 관련된 실험은 부족한 실정이다. 주년생산을 위해서는 일장조절이 용이한 LED 재배가 필수적일 것으로 예상되기 때문에 이를 실현하기 위해서는 사전에 각기 다른 광질의 LED를 활용하여 광질에 따른 생장 정도를 평가하는 것이 시급할 것으로 판단된다.
이에 본 연구는 시중에 가장 많이 유통되는 바위솔과 자질연화바위솔을 대상으로 다양한 LED 광질이 생장과 엽색에 미치는 영향을 구명하고자 실시되었다.
재료 및 방법
1. 식물재료
식물재료는 국립농업과학원 농업유전자원센터의 식물유전자원 중 바위솔(Orostachys japonica,유전자원번호 IT317333)을 이용하였으며 그 중 1년생 모체의 런너 중 초장과 초폭이 각각 1cm인 균일한 것만을 채취하여 사용하였다. 자질연화바위솔(O. boehmeri)은 삼육대학교 환경원예학과 실험온실에서 35% 차광 수준 하에서 재배 중인 모체의 런너 중 초장과 초폭이 각각 1cm인 균일한 것만을 선발하여 활용하였다.
2. 재배조건
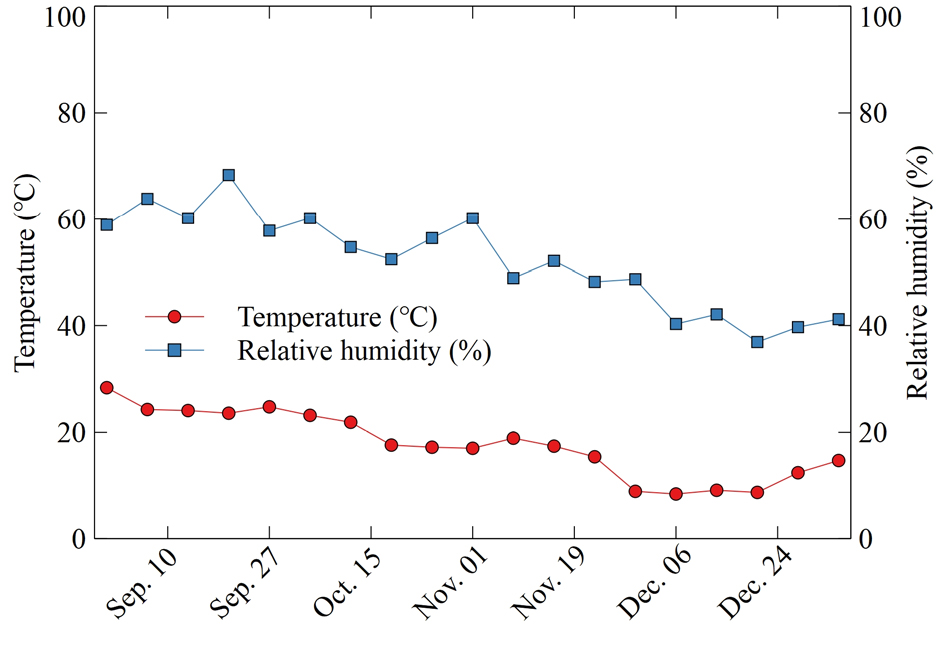
실험은 2021년 8월 30일부터 2022년 1월 3일까지 삼육대학교 환경원예학과 식물생장실험실에서 총 18주간 진행하였다. 식물은 내경의 가로×세로×높이가 각각 48.5×33×8cm인 삽목상자에 식재하였으며 배지는 다육식물용 배지를 조성해 사용하였다. 해당 배지의 재료로는 마사토, 강모래, 원예용 상토(Hanareumsangto, Shinsung Mineral, South Korea)를 사용하였고, 이때 배지의 혼합 비율은 마사토:강모래:원예용상토(60:30:10, v/v/v) 순으로 혼합하였다. 관수는 정수처리된 물을 매주 1회 500mL 만큼 관수하였다. 실험 기간 동안 식물생장실험실의 평균 온도와 평균 상대습도는 각각 17.6 ± 10.8°C, 52.1 ± 16.3%였으며(Fig. 1), 별도의 가온처리를 하지 않았다. 실험은 완전임의배치법(completely randomized design)으로 식물체를 각 처리당 종별로 15개체씩 배치하였다.
3. LED 처리
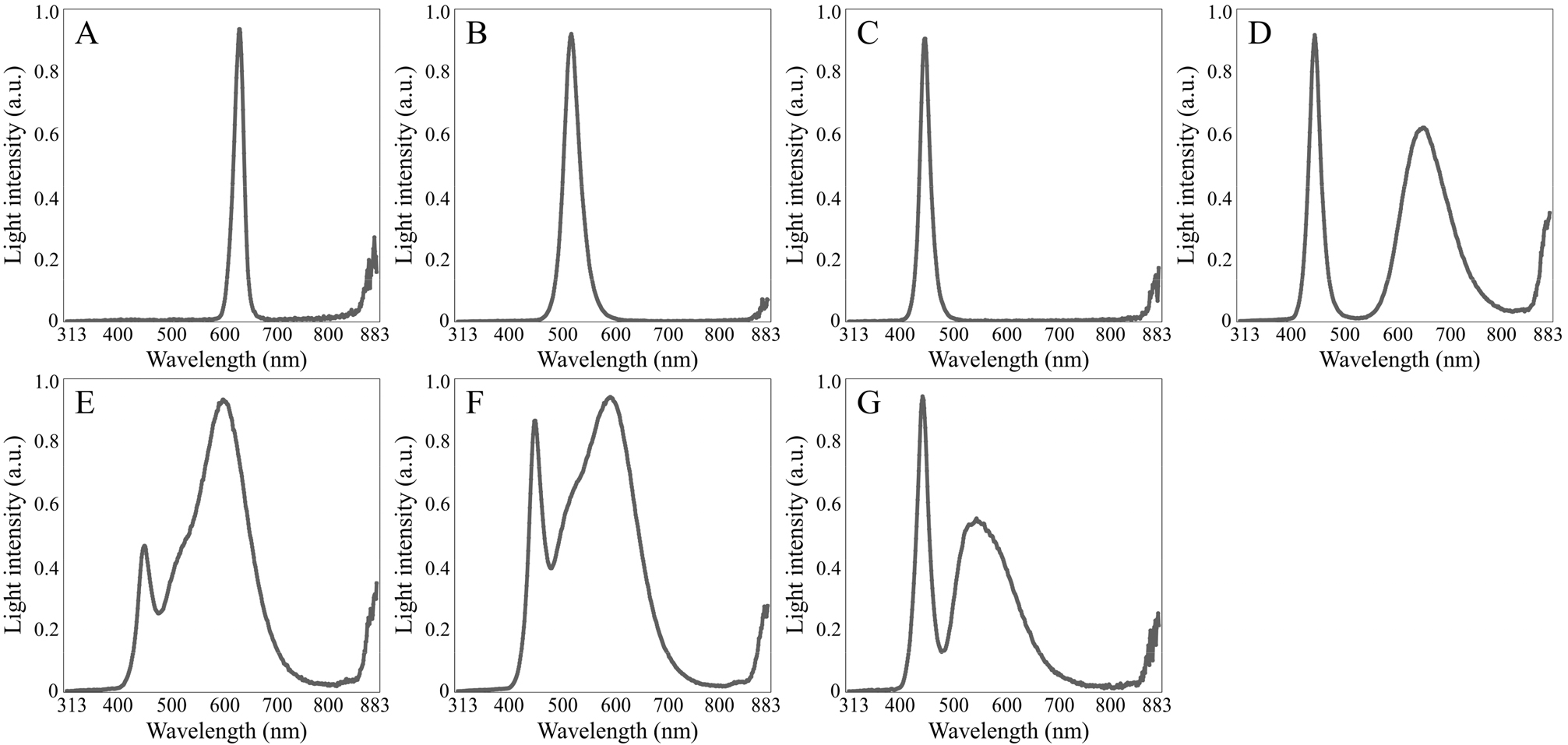
LED 광질에 따른 바위솔과 자질연화바위솔의 생장과 엽색 수준을 평가하기 위해 길이는 1.2m이며 20W의 동일한 전력량을 사용하는 T5 LED(Zhongshan Jinsheng Electronics, China)를 각 처리별로 2줄씩 설치하여 진행하였다. 각각 적색 LED(630nm), 녹색 LED(520nm), 청색 LED(450nm), 식물등 LED(보라색)(650, 450nm), 3000K 백색 LED(전구색)(455, 600nm), 4100K 백색 LED(주백색)(455, 590nm), 6500K 백색 LED(주광색)(450, 545nm)의 7가지 처리로 나누어 진행하였다. 식물과 LED 간의 거리는 28cm로 조절하였으며 이때 각 광질과 광도는 휴대용 분광복사계(SpectraPen mini, Photon Systems Instruments, Czech Republic)를 이용하여 측정하였다(Fig. 2 and Table 1). 추가로 광의 교섭을 차단하기 위해 각 처리 구간마다 암막을 설치하였다. 광주기는 명기/암기를 각각 12시간/12시간으로 설정한 후 실험을 진행하였다.
Table 1.
Photosynthetic photon flux density (PPFD) subjected to different LED light qualities.
4. 조사항목
바위솔과 자질연화바위솔의 생장 수준과 엽색을 평가하기 위해 각 식물의 초장, 초폭, 근장, 생체중, 건물중, CIELAB L*, a*, b* 값을 측정하였다. 초장은 지면에서부터 식물체의 정단부까지를 기준으로 측정하였으며 초폭은 Orostachys의 형태적 특성이 로제트형인 것을 감안하여 식물체의 지름으로 측정하였고, 근장은 식물의 뿌리 중 가장 긴 것의 길이를 기준으로 측정하였다. CIELAB 값은 분광광도계(CM-2600d, Konica Minolta, Japan)를 CIELAB(set to L*a*b*, ΔE*), UV 100% 그리고 D65 10°로 설정한 후 각 처리별 15반복만큼 정반사광(SCI)을 포함한 CIELAB L*, a*, b* 값을 얻었다. 색상은 각 L*, a*, b* 값을 Royal Horticultural Society Colour Chart 시스템(RHSCCS, 2022)의 차트에서 대응하는 색상과 대조하였고 가장 가까운 색상의 RHS 고유번호를 처리구별로 2개씩 선정해 평가하였다. 각 처리별 식물의 엽색은 Zettl(2022)이 설계한 Converting Colors를 활용하여 CIELAB L*, a*, b* 값을 평가 색상으로 변환하였다. 생체중 및 건물중은 전자저울(FA-2000, AND, Japan)을 이용하여 측정하였으며 건물중의 경우 전처리로 식물체를 85°C로 설정한 건조기(HK-DO135F, HANKUK S&I, South Korea)에 넣고 2일 간 건조시킨 뒤 측정하였다. 식물체가 가진 수분함량에 대한 분석은 각 개체별 생체중 및 건물중을 대조한 후 식 (1)과 같이 각각 계산한 뒤 통계분석을 실시하였다.
는 수분함량, 는 생체중, 는 건물중을 나타낸다.
실험 종료 후 LED 광질에 따른 식물의 엽색 변화를 알아보기 위해 실험 시작 전 식물의 CIELAB 값을 대조군(control) 및 참조(reference)로 설정하여 CIE76 ΔE*ab를 기준으로 각 처리별 색차를 계산하였다. CIE76 color-difference(ΔE*ab)에 관한 식 (2)은 다음과 같다(CIE, 2004).
이때, 이 실험에서 ΔE*ab≤1.5 수준은 색차 없음 혹은 미세한 색차, 1.6-3.0 수준은 아주 약간의 색차 있음, 3.1-6.0 수준은 약간의 색차 있음, 6.1-9.0 수준은 색차 있음, 9.1-12.0 수준은 큰 색차 있음, ≥12.1 수준은 매우 큰 색차 있음 혹은 완전히 다른 색상으로 간주한다.
5. 통계처리
실험 결과의 분석은 SAS 9.1(SAS Institute, USA)을 사용하여 분산분석(analysis of variance)을 수행하였다. 이때, 모든 조사 항목은 각각 15반복씩 측정되었다. 평균 간 비교는 던컨의 다중검정(Duncan's multiple range test)을 이용하여 p < 0.05 수준에서 각 LED 처리 간의 차이를 분석하였다. 추가로 피어슨 상관계수(Pearson correlation coefficients)을 통해 바위솔과 자질연화바위솔의 생체중, 건물중, CIELAB L*, a*, b* 값 간의 상관관계를 분석하였다.
결과 및 고찰
1. LED 광질이 생장에 미치는 영향
본 실험에서 바위솔은 모든 처리구에서 100%의 생존율을 나타내어 다양한 광 환경에 대해 뛰어난 적응력을 보인 반면 자질연화바위솔은 광질에 따라 각기 다른 결과를 나타내었다(Table 2). LED 광질에 영향을 받은 바위솔과 자질연화바위솔의 사진자료는 각각 Fig. 3과 Fig. 4에 나타내었다. 자질연화바위솔은 3000K LED 처리구와 4100K LED 처리구에서 100%의 생존율을 나타내었으나 녹색 LED 처리구와 청색 LED 처리구에서는 73.3%의 저조한 생존율을 나타내었다. 바위솔은 4100K LED 처리구에서 가장 건실하게 생장하였는데 초장과 초폭은 각각 2.71, 5.68cm로 나타났으며 근장은 6.09cm로 나타났다. 이어 생체중과 건물중의 경우에는 각각 6.90, 0.51g으로 나타나 적색 파장과 청색 파장이 비교적 균일한 광원 하에서는 생장에 이점이 있는 것으로 판단되었다.
Table 2.
Survival rate and plant growth of Orostachys japonica and O. boehmeri as affected by different LED light qualities.
| Species | Treatment |
Survival rate (%) | Plant size (cm) |
Fresh weight (g) |
Dry weight (g) |
Moisture content (%) | ||
| Shoot height | Shoot diameter | Root length | ||||||
| Orostachys japonica | Red | 100 | 2.37 bcz | 4.96 bc | 5.12 b | 5.39 abc | 0.28 c | 94.8 a |
| Green | 100 | 2.23 c | 4.51 c | 3.30 c | 3.44 d | 0.15 d | 95.4 a | |
| Blue | 100 | 2.42 bc | 4.94 bc | 4.47 b | 4.77 bcd | 0.31 c | 93.0 b | |
| Purple | 100 | 2.42 bc | 4.67 c | 5.15 b | 4.06 cd | 0.26 c | 93.3 b | |
| 3000 K | 100 | 2.30 bc | 5.46 ab | 5.95 a | 6.15 ab | 0.41 b | 93.0 b | |
| 4100 K | 100 | 2.71 a | 5.68 a | 6.09 a | 6.90 a | 0.51 a | 92.6 b | |
| 6500 K | 100 | 2.50 b | 5.00 bc | 4.49 b | 6.39 a | 0.33 bc | 94.6 a | |
| Orostachys boehmeri | Red | 80 | 4.75 b | 3.77 b | 5.01 abc | 1.91 bc | 0.08 b | 95.6 ab |
| Green | 73.3 | 7.31 a | 3.56 b | 3.86 cd | 0.89 c | 0.04 b | 94.9 ab | |
| Blue | 73.3 | 4.96 b | 4.54 a | 3.58 d | 2.52 ab | 0.12 a | 94.4 b | |
| Purple | 86.6 | 4.55 b | 4.26 ab | 5.83 a | 2.58 ab | 0.15 a | 93.0 c | |
| 3000 K | 100 | 5.26 b | 4.72 a | 5.30 ab | 3.31 a | 0.14 a | 95.5 ab | |
| 4100 K | 100 | 5.19 b | 4.69 a | 5.99 a | 3.06 ab | 0.15 a | 95.0 ab | |
| 6500 K | 86.6 | 4.58 b | 5.00 a | 4.53 bcd | 3.75 a | 0.14 a | 95.9 a | |
녹색 LED 처리구에서는 바위솔의 초장과 근장이 각각 2.23, 3.30cm로 처리구들 중 가장 낮게 나타났으나 본 연구에서 설정된 광도인 35.3μmol m-2 s-1보다 2배가량 높게 설정할 경우 69.2μmol m-2 s-1의 광도를 가진 청색광에 준하는 수준으로 생장할 것으로 예상된다. 한편 적색 LED 처리구는 37.6μmol m-2 s-1의 낮은 광도 수준에서도 평균적인 생장 수준을 나타내었는데 던컨의 다중검정에서 청색, 보라색 LED 처리구와 초폭, 근장, 건물중에서는 유의적 차이가 없는 것으로 나타났으며 반대로 생체중은 오히려 더 높게 나타나 적색 LED 처리구를 청색, 보라색 LED 처리구에 준하는 광도 수준으로 설정할 경우 앞서 언급 된 두 처리구보다 더 높은 생장 수준을 나타낼 수 있을 것으로 예측된다. Kim 등(2018a)의 연구에서 배초향(Agastache rugosa)은 백색 LED가 혼합된 처리구에서 가장 높은 지상부, 지하부 생체중을 나타내었으며 지하부 건물중 또한 가장 높게 나타난 것으로 보고되었다.
자질연화바위솔의 경우 광질에 따라 다양한 생장 수준의 차이를 나타내었는데 특히 바위솔과 반대로 녹색 LED 처리구에서 초장이 7.31cm로 가장 높게 나타났으며, 생체중과 건물중은 각각 0.89, 0.04g으로 모든 처리구 중 가장 낮게 나타나 식물체가 도장한 것으로 판단되었다. 과거 문헌에서 녹색 파장은 식물의 엽육조직에 더 잘 침투할 수 있고 잎 전체의 광화학적 효율을 증가시켜 식물의 생장을 증대시킬 수 있다고 보고되었으나(Kim 등, 2004b; Terashima 등, 2009), 본 연구에서 녹색 LED만을 단독으로 사용하였을 때 바위솔과 자질연화바위솔의 생장에 긍정적인 영향을 주지는 못한 것으로 나타났다. 그러나 녹색 LED를 본 연구에서 사용된 광도 수준보다 더 높은 수준으로 설정하거나 보광용 및 보조용으로 활용하는 등 다른 각도에서의 녹색 LED의 효용성에 관한 추가 검증실험이 필요할 것으로 판단된다. 6500K LED 처리구에서는 자질연화바위솔의 생체중이 3.75g으로 가장 높게 나타났고 그 다음으로는 3000K LED 처리구에서는 생체중이 3.31g으로 나타났다. 건물중은 보라색 LED와 4100K 처리구에서 0.15g으로 가장 높게 나타났으며 그 뒤로는 3000K와 6500K가 0.14g으로 뒤따랐다.
시금치의 ‘월드스타’ 품종(Spinacia oleracea ‘World Star’)은 적색 LED와 청색 LED가 혼합된 처리구에서 근장이 가장 높게 나타났는데(Lee 등, 2018), 이와 유사하게 자질연화바위솔은 보라색 LED 처리구에서 근장이 가장 높게 나타났다. 국화(Chrysanthemum morifolium)의 ‘백마(Baekma)’와 ‘핑크프라이드(Pink Pride)’의 절화 생체중과 엽수는 적색 LED와 청색 LED가 혼합된 처리구에서 가장 높게 나타낸 반면 ‘진바(Jinba)’와 ‘일월(Ilwol)’은 형광등 처리구에서 가장 높게 나타났다(Choi 등, 2012). 고구마(Ipomoea batatas)의 품종 중 ‘신황미(Shinhwangmi)’는 적색 LED 처리구에서 가장 높은 근장과 생체중을 나타내었고 ‘연황미(Yeonhwangmi)’는 적색 LED와 청색 LED 혼합 처리구에서 가장 높은 생체중을 나타내었다(Lee와 Lee, 2014).
다육식물의 경우 일반적으로 생장이 불량한 식물체는 건실하게 생장한 식물체에 비해 상대적으로 더 많은 수분함량을 나타내는 경향이 있다. 바위솔은 생장이 가장 건실했던 4100K LED 처리구에서는 수분함량이 92.6%로 가장 낮게 나타난 반면 생장 수준이 불량했던 녹색 LED에서는 95.4%로 가장 높게 나타났다. 그러나 자질연화바위솔은 이러한 일반적인 경향과 반대의 결과를 나타내었는데 생체중과 건물중이 가장 높게 나타난 6500K LED 처리구에서 동시에 가장 높은 수분함량(95.9%)을 나타내었다. 이를 미루어 보아 생장환경이 적합할 때 더 많은 런너를 생산하기 위해 수분을 체내에 비축하는 것으로 생각되었다.
2. LED 광질이 엽색에 미치는 영향
다양한 LED 광질은 바위솔과 자질연화바위솔의 엽색에 각기 다른 영향을 미쳤다(Table 3). CIELAB는 1976년 프랑스의 Commission Internationale de l'Eclairage(CIE)에서 정의한 색공간(color space)이다. 국내 농학 및 원예학과 관련한 학술지에서 일반적으로 사용되어 왔던 Hunter Lab는 L, a, b로 표기하는 반면 이와 구분하기 위해 CIELAB는 L*, a*, b*로 표기하는 것이 특징이다. L*은 명도를 나타내고 숫자가 커질수록 흰색에 가까운 색상을 나타낸다. a*는 음수인 경우 초록색, 양수인 경우 붉은색을 나타낸다. b*는 음수인 경우 푸른색 양수인 경우 노란색을 나타낸다. 바위솔과 자질연화바위솔은 모두 녹색 LED 처리구에서 가장 높은 L*과 b* 값을 나타내었는데 L* 값은 각각 38.89, 49.16, b* 값은 각각 18.44, 13.76을 나타내었다. 녹색 LED 하에서는 제대로 된 광합성이 어려웠을 것으로 생각되며 이로 인한 스트레스로 잎이 황화된 것으로 판단된다. L* 값이 가장 낮은 처리구는 바위솔의 경우 보라색 LED 처리구로 33.89로 나타났으며 자질연화바위솔의 경우에는 6500K LED 처리구에서 44.93로 나타났다.
Xie 등(2022)의 연구에서 백색, 적색, 청색 등의 LED에 비해 보라색 LED가 엽록소 분해와 관련된 유전자 발현을 억제함으로써 엽색의 황화 억제와 엽록소 함량 유지에 가장 좋은 효과를 나타내었다. De Keyser 등(2019)의 연구에서 구즈마니아 ‘테레사’ 품종(Guzmania lingulata ‘Theresa’)은 LED 파장 중 청색 계통의 파장이 없는 경우 엽색이 황색으로 변하는 것으로 나타났고 하이포에스테스 ‘데코핑크’ 품종(Hypoestes phyllostachya ‘Decor Pink’)은 적색광 파장에서는 생장이 불량해지는 것으로 나타났다.
일반적으로 식물은 일조량이 부족하거나 지속적인 스트레스 환경 속에서 잎이 황화하는 경향을 나타내는데 이때 황화 정도에 따라 L*과 b*는 비례하여 높아진다. Lee 등(2021a)의 연구에서 엽록소형광 측정 결과 실내 관엽식물은 연속광 조건 하에서는 광도가 상대적으로 높아질수록 더 많은 스트레스를 받는 것으로 보고되었는데 이때 L*과 b* 값은 스트레스 정도에 따라 동시에 비례하여 높아지는 것으로 나타났다. 바위솔과 자질연화바위솔은 상대적으로 적색과 청색 파장이 고르게 분포할 때 광합성이 활발한 것으로 생각되며 이로 인해 잎의 황화가 억제되어 상대적으로 잎의 L* 값이 낮아지는 것으로 판단된다.
Table 3.
Leaf color reading of CIELAB values, CIE76 color-difference (ΔE*ab), RHS values, and converted color of Orostachys japonica and O. boehmeri as affected by different LED light qualities.
| Species | Treatment | CIELAB values | ΔE*ab (CIE76) | RHS values |
Converted colorz | ||
| L* | a* | b* | |||||
| Orostachys japonica | Control | 36.42 | -6.57 | 14.92 | Reference | N137A, 147A |  |
| Red | 35.01 bcy | -6.48 bc | 13.57 d | 1.95 | N137A, 147A |  | |
| Green | 38.89 a | -7.97 d | 18.44 a | 4.52 | 146A, 147B |  | |
| Blue | 35.00 bc | -4.20 a | 15.49 bc | 2.82 | N137A, 147A |  | |
| Purple | 33.89 c | -5.82 b | 15.61 bc | 2.72 | N137A, 147A |  | |
| 3000 K | 36.87 ab | -7.03 c | 16.74 b | 1.93 | N137A, 147A |  | |
| 4100 K | 36.03 b | -6.35 bc | 13.62 d | 1.37 | N137A, 147A |  | |
| 6500 K | 37.08 ab | -6.70 c | 14.94 cd | 0.67 | N137A, 147A |  | |
| Orostachys boehmeri | Control | 45.04 | -5.94 | 5.87 | Reference | N138A, N138B |  |
| Red | 47.35 b | -6.67 d | 7.50 b | 2.91 | N138A, N138B |  | |
| Green | 49.16 a | -8.00 e | 13.76 a | 9.13 | 147B, 148A |  | |
| Blue | 47.14 bc | -4.52 a | 3.89 c | 3.21 | N138A, N138B |  | |
| Purple | 45.65 cd | -5.09 ab | 4.74 c | 1.53 | N138A, N138B |  | |
| 3000 K | 46.06 bcd | -6.40 cd | 6.94 b | 1.54 | N138A, N138B |  | |
| 4100 K | 45.45 d | -5.72 bc | 5.16 c | 0.84 | N138A, N138B |  | |
| 6500 K | 44.93 d | -5.68 bc | 5.34 c | 0.60 | N138A, N138B |  | |
색차 분석의 경우 바위솔은 녹색 LED 처리구에서 ΔE*ab가 4.52로 나타났는데 이는 ΔE*ab = 3.1-6.0 내 수준으로 ‘약간의 색차 있음’으로 평가되었다. 이와 반대로 태양빛과 비교적 유사한 색온도를 가진 6500K 처리구에서는 ΔE*ab가 0.67로 ‘색차 없음’으로 평가되어 태양광 하에서 재배한 식물에 준하는 엽색의 품질을 유지하고자 할 경우 6500K 백색 LED 하에서 재배하는 것이 가장 이상적인 것으로 판단된다. RHS 색상 값은 대부분의 처리구에서 모두 N137A, 147A로 평가되었으나 녹색 LED 처리구에서는 146A, 147B로 평가되어 다른 처리구들에 비해 엽색이 약간 황화된 것으로 판단되었다. 자질연화바위솔도 바위솔과 마찬가지로 녹색 LED 처리구에서 가장 높은 색차를 나타내었는데 이때 ΔE*ab가 9.13으로 나타났다. ΔE*ab = 9.1-12.0 내 수준으로 ‘큰 색차 있음’으로 평가되었다. 앞서 언급된 바위솔과 마찬가지로 태양광 하에 재배한 식물에 준하는 엽색 품질의 유지를 위해서는 6500K 백색 LED 하에서 재배하는 것이 바람직할 것으로 판단된다(ΔE*ab = 0.60). RHS 색상 값은 녹색 LED 처리구에서 특별히 147B, 148A로 평가되어 식물체가 황화한 것으로 판단되었다.
CIELAB는 Hunter LAB에 비해 상대적으로 엽색 및 화색을 평가하기에 좋은 방법으로 생각되어지며 오늘날에 이르러 다양한 원예학적 연구에서 색채 분석이 이루어지고 있다. 몇몇 연구자들에 의해 엽색 및 화색에 관한 ΔE*ab 색차 분석이 수행되기도 하였으며(Lee 등, 2017; Park과 Lee, 2021), 바이러스에 의한 병반 분석 등에 CIELAB(Sukmana와 Rahmanti, 2017), RGB image(Chaudhary 등, 2012)를 활용한 색채 분석이 수행되었다.
3. 생장과 엽색 간 상관관계 분석
바위솔의 시장 출하에 있어 높은 값을 받기 위해서는 생체중과 건물중이 가장 중요한 요소로 꼽힌다. 뿐만 아니라 수확 후 건조처리 없이 식물체를 그대로 판매하기도 하므로 소비자가 상품을 바라보는 시각과 관련되어 있는 엽색 또한 중요하다. 다양한 LED 광질 처리 하에서 생장뿐 아니라 CIELAB에서도 몇 가지 차이가 발생하였는데 생장과 엽색 간에 어떤 영향을 알아보기 위하여 서로 간의 상관관계를 분석하였다. 바위솔의 생장과 엽색 간의 상관관계를 분석한 결과 b*는 건물중과 음의 상관관계(r = −0.197)를 나타내었다(Table 4). 스트레스 환경으로 인해 엽색이 황화 될 경우 이는 엽록소 농도가 낮아졌다는 것을 암시하는 것으로 이에 따라 b* 값이 높게 나타나는 것으로 생각된다. 이에 따라 b* 값이 상대적으로 높게 나타날수록 그에 따라 생장이 그만큼 불량하다고 해석할 수 있겠다.
Table 4.
Correlation between fresh and dry weight, and leaf color values (CIELAB) of Orostachys japonica grown under various LED light qualities.
| Fresh weight | Dry weight | L* | a* | b* | |
| Fresh weight | 1 | ||||
| Dry weight | 0.849*** | 1 | |||
| L* | -0.106 | -0.124 | 1 | ||
| a* | 0.001 | 0.103 | -0.468*** | 1 | |
| b* | -0.152 | -0.197* | 0.449*** | -0.502*** | 1 |
Lee 등(2022)의 고온과 연속광 조건에서 광도별 실내 관엽식물의 생장 및 엽색 평가에 관한 연구에서 아이비(Hedera helix)와 스파티필름(Spathiphyllum wallisii)은 상관관계 분석에서 생체중과 건물중 등의 생장수준과 엽색의 L*, b* 값은상호 간 음의 상관관계를 가지는 것으로 나타나 엽색의 명도가 높아지거나 황색이 짙어지는 경우 생장에 악영향을 끼친다는 것을 암시하였다. 바위솔의 엽색 분석에서 L*과 b*는 상호 간에 양의 상관관계(r = 0.449)를 나타냈는데 이는 식물체가 스트레스 환경으로 인해 잎이 황화하는 경우 이 두 가지 값이 동시에 증가하는 것으로 보인다. 반대로 녹색과 직접적으로 연관되어 있는 a*의 경우 생장과는 무관한 것으로 나타났으나 L*과 b* 값과는 각각 r = −0.468, −0.502로 음의 상관관계를 나타내어 엽색의 황화와 반비례하여 대응하는 것으로 보인다. 자질연화바위솔은 생장과 엽색 간에서 일정한 상관관계를 나타내었는데 L*은 생체중과 건물중에 대해 각각 r = −0.272, −0.382 b*는 생체중과 건물중에 대해 각각 r = −0.300, −0.455로 나타났다(Table 5). a*는 바위솔과 유사하게 L*과 b*와 r = −0.525, −0.835로 음의 상관관계를 나타내었다. 그러나 바위솔과 반대되는 점은 생장과 a* 값 간에 양의 상관관계가 있는 것으로 나타났는데 a*와 생체중 간의 상관관계는 r = 0.345, 건물중 간의 상관관계는 r = 0.421로 나타났다.
Table 5.
Correlation between fresh and dry weight, and leaf color values (CIELAB) of Orostachys boehmeri grown under various LED light qualities.
| Fresh weight | Dry weight | L* | a* | b* | |
| Fresh weight | 1 | ||||
| Dry weight | 0.905*** | 1 | |||
| L* | -0.272* | -0.300** | 1 | ||
| a* | 0.345** | 0.421*** | -0.525*** | 1 | |
| b* | -0.382*** | -0.455*** | 0.611*** | -0.835*** | 1 |
따라서 우수한 생장과 엽색 수준을 유지하기 위해 바위솔은 4100K 백색 LED 하에서 재배할 것을, 자질연화바위솔은 3000, 4100, 6500K의 백색 LED 하에서 재배할 것을 권장한다.